Sinds de eerste publicatie van Wittich in 1941, waarin het succesvolle gebruik van ASIT (Allergie-specifieke immunotherapie) voor de behandeling van een allergie bij een hond werd beschreven, zijn er vele vorderingen gemaakt. Hoewel er veel studies bij mensen zijn die de effectiviteit van ASIT in verschillende allergische aandoeningen, zoals allergische rhinitis en astma, uitgebreid documenteren, blijven de gegevens met betrekking tot CAD paradoxaal genoeg fragmentarisch.
Stand van zaken over ASIT bij honden
Terwijl bij mensen sommigen de nut van ASIT bij atopisch eczeem in twijfel trekken, is deze controverse blijkbaar nooit opgetreden in de veterinaire geneeskunde, waarschijnlijk vanwege eerste veelbelovende rapporten over CAD. De afwezigheid van controverse in de veterinaire geneeskunde zou ook te maken kunnen hebben met factoren zoals het beperkte aantal rigoureuze klinische studies bij honden, de complexiteit van de evaluatie van de effectiviteit van ASIT in de context van CAD, en de variabiliteit van de therapeutische protocollen die tussen de verschillende studies worden gebruikt. Deze factoren bemoeilijken de directe vergelijking van de resultaten, waardoor globale conclusies over de effectiviteit van ASIT bij honden worden beperkt.
Studies, waaronder een placebo-gecontroleerde dubbelblinde studie bij 51 honden, hebben responspercentages (doorgaans gedefinieerd als het percentage honden dat ten minste 50% verbetering van de klinische symptomen vertoont) van 60 tot 70% aangetoond. Het is echter cruciaal op te merken dat zelfs in positieve gevallen een significant percentage honden (tot 65% in een studie) aanvullende medicamenteuze behandeling nodig had, wat twijfels oproept over het vermogen van eigenaren om de effectiviteit van ASIT objectief te beoordelen. De huidige richtlijnen voor de behandeling van CAD kwalificeren de kwaliteit van de gepubliceerde gegevens over de effectiviteit van ASIT als “beperkt”. Deze beperking van het bewijs is te wijten aan verschillende factoren, met inbegrip van de beperkte omvang van veel studies, het gebrek aan standaardisatie van protocollen, en de moeilijkheid om objectieve meetpunten van de effectiviteit van ASIT bij honden te verkrijgen. Het is belangrijk te benadrukken dat de beoordeling van de effectiviteit van ASIT vaak berust op subjectieve evaluaties door eigenaren, wat een vertekening in de resultaten kan veroorzaken. Meer objectieve evaluatiemethoden, zoals het gebruik van biomarkers of gevalideerde klinische scores, zijn nodig om de kwaliteit van de beschikbare gegevens te verbeteren.
De interpretatie van de resultaten van studies over ASIT bij honden wordt vaak bemoeilijkt door de variabiliteit van de gebruikte protocollen. Verschillen in dosering, samenstelling van allergene extracten, frequentie van injecties, gelijktijdige behandelingen en methoden voor resultaatbeoordeling maken directe vergelijking van de resultaten in de verschillende studies moeilijk. De heterogeniteit van de hondenpopulaties die in de studies zijn opgenomen, vormt een andere complexiteitsfactor. De variabiliteit in rassen, leeftijden, ernst van CAD en medische geschiedenis van de honden kan de respons op ASIT beïnvloeden, waardoor de analyse van de resultaten complexer wordt. Om de interpretatie van gegevens te verbeteren, moeten toekomstige studies zich richten op de standaardisatie van protocollen, de homogeniteit van de bestudeerde populaties en het gebruik van meer objectieve effectiviteitsmaatregelen.
Vergelijking met menselijke ASIT: Hoewel ASIT wordt gebruikt om verschillende allergieën bij mensen te behandelen, zijn de effectiviteit en werkingsmechanismen niet altijd volledig begrepen, en verschillen zij naargelang het type allergie en het individu. Er is controverse over het nut van ASIT bij atopisch eczeem bij mensen, waarbij sommige studies de effectiviteit ervan in twijfel trekken, terwijl andere positieve resultaten tonen. Deze nuance weerspiegelt de complexiteit van individuele immuunreacties en de heterogeniteit van atopisch eczeem. Vergelijking met menselijke ASIT kan onderzoekslijnen voor canine ASIT identificeren, maar het is belangrijk om deze vergelijkingen te nuanceren wegens de fysiologische en immunologische verschillen tussen soorten.
Werkingsmechanismen: het bekende en het onbekende
Het exacte werkingsmechanisme van ASIT bij honden is nog niet volledig opgehelderd. Toch is een parallel met menselijke mechanismen plausibel. Bij de mens wordt een initiële vermindering van de activiteit van effectorcellen (eosinofielen, basofielen, mestcellen) waargenomen, gevolgd door een immunologische verandering op lange termijn, van een Th2 (helper 2) naar een Th1 (helper 1) cellulaire respons en de ontwikkeling van immuuntolerantie. Dit complexe en multifactoriale proces omvat verschillende stappen en celpopulaties.
- Initiële fase: Blootstelling aan allergenen in lage concentraties veroorzaakt een modulatie van de onmiddellijke ontstekingsreactie. Dit uit zich in een vermindering van de afgifte van histamine en andere ontstekingsmediatoren door mestcellen en basofielen, wat de onmiddellijke allergiesymptomen vermindert. De degranulatie van mestcellen, een sleutelproces in de onmiddellijke allergische respons, wordt geremd of verminderd.
- Late fase: De immuunreactie verschuift geleidelijk naar een Th1-profiel, met een toename van Th1-helper T-cellen die pro-inflammatoire cytokines zoals interferon-gamma (IFN-γ) produceren en een afname van Th2-helper T-cellen en geassocieerde cytokines (IL-4, IL-5, IL-13). Deze Th1/Th2 verschuiving draagt bij aan de regulatie van de langdurige ontstekingsrespons.
- Rol van regulerende T-cellen (Treg): Treg-cellen met markers zoals FOXP3 spelen een cruciale rol in de verworven immuuntolerantie door ASIT. Deze cellen onderdrukken de activiteit van effector T-cellen, wat bijdraagt aan de verzachting van de allergische ontstekingsreactie. De toename van het aantal en de activiteit van Treg-cellen wordt in verband gebracht met een betere respons op ASIT.
- Productie van IgG: De productie van IgG-immunoglobulinen, met name IgG4, specifiek voor het allergeen, neemt toe na langdurige behandeling. Deze blokkerende IgG-antilichamen kunnen de binding van IgE aan allergenen verminderen, waardoor hun vermogen om een ontstekingsreactie te veroorzaken, afneemt. De impact van IgG op de vermindering van de allergische respons blijft echter onzeker volgens studies.
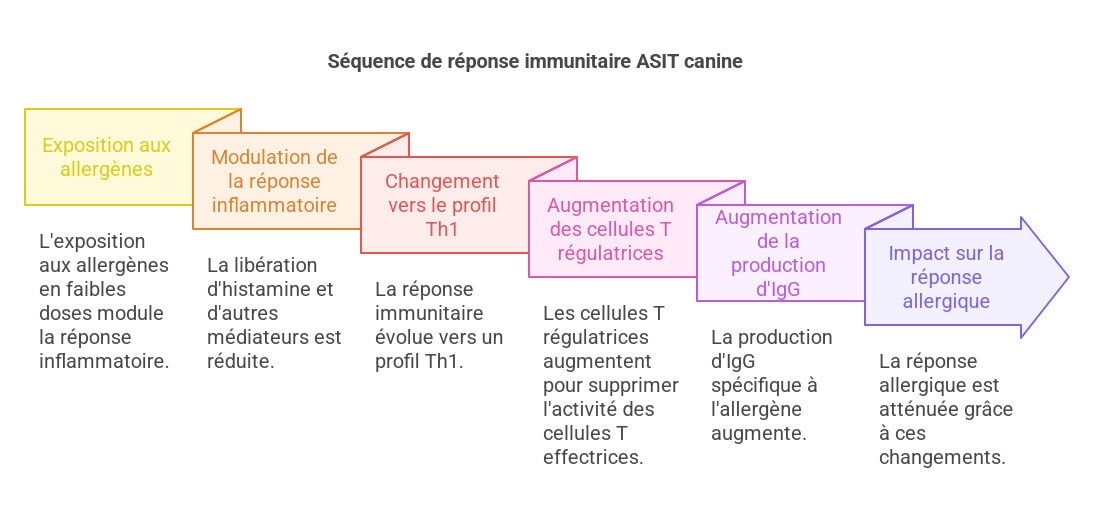
Deze veranderingen gaan gepaard met een toename van cytokines zoals transformatieve groeifactor bèta (TGFβ) en interleukine (IL)-10, anti-inflammatoire cytokines die een rol spelen bij het behoud van immuuntolerantie. Dit resulteert in een toename van immunoglobulinen (IgG) specifiek voor het allergeen, vooral IgG4, en bij langdurige behandeling in een afname van IgE specifiek voor het allergeen. Bij honden, hoewel de kennis minder uitgebreid is, zijn een verschuiving naar een Th1-reactie, een toename van IgG-niveaus, het optreden van meer Treg-cellen en verhogingen van IL-10-spiegels allemaal aangetoond, waardoor parallellen met menselijke ASIT worden getrokken. Echter, studies bij honden zijn minder talrijk en minder diepgaand dan bij mensen, waardoor extra onderzoek naar de werkingsmechanismen van ASIT bij honden nodig is voor een betere begrip. Het gebruik van diermodellen (zoals muizen) kan sommige mechanismen helpen ophelderen, maar extrapolatie naar de hondensoort moet voorzichtig gebeuren.
Sublinguale toediening heeft een extra effect door oromucosale dendritische cellen. Bij de mens spelen deze cellen een belangrijke rol bij de inductie van orale tolerantie, een immunologisch proces waarmee het immuunsysteem geprogrammeerd wordt om niet te reageren op stoffen die in de mond worden ingebracht (bijvoorbeeld voeding). De precieze rol van deze cellen bij ASIT bij honden moet nog verder onderzocht worden.
Huidige benaderingen van ASIT bij honden: effectiviteit en verbeterpunten
De huidige benaderingen van ASIT voor CAD zijn gebaseerd op twee voornaamste toedieningswegen: subcutaan (SCIT) en sublinguaal (SLIT). SCIT, dat al decennialang wordt uitgevoerd, gebruikt in Noord-Amerika fenol-geconserveerde en in Europa aluin-geprecipiteerde allergene extracten. De bezorgdheden over de potentiële langdurige nadelige effecten van aluminium, ondanks de voordelen van minder frequente injecties, nemen toe. Die bezorgdheden hebben betrekking op chronische blootstelling aan aluminium. Diepgaande studies naar de lange-termijn toxiciteit van aluminium zijn nodig om de implicaties van het gebruik in vaccins en allergiebehandelingen volledig te evalueren. Alternatieven voor aluminiumgebaseerde adjuvanten worden momenteel onderzocht, waaronder meer biocompatibele en minder toxische adjuvanten.
SLIT, vaker gezien bij mensen, is recentelijker verschenen in de diergeneeskunde en is controversieel bij mensen wat betreft de betrouwbaarheid van veel oude studies met zeer variabele protocollen. Recente analyses en standpunten van de Wereldorganisatie voor Allergie concluderen dat het effectief is en een gunstiger veiligheidsprofiel heeft in vergelijking met SCIT. Echter, gegevens over canine SLIT zijn nog beperkt en vereisen verdere studies om de effectiviteit en veiligheid ervan in deze soort te valideren. Studies bij mensen suggereren dat SLIT een praktischer en veiliger aanpak kan zijn dan SCIT. Echter, de variabiliteit van de protocollen gebruikt in menselijke studies maakt het moeilijk om optimale protocollen te bepalen voor canine SLIT, en er zijn toekomstige studies nodig voor de validatie van het gebruik bij honden. Evenzo zijn vergelijkende studies tussen SCIT en SLIT bij CAD essentieel om hun relatieve effectiviteit en de voor- en nadelen van elke methode te evalueren.
Belangrijke overwegingen met betrekking tot de kwaliteit van de gebruikte extracten beïnvloeden de effectiviteit. Allergene extracten voor veterinair gebruik zijn decennia geleden gelicenseerd door het Amerikaanse ministerie van Landbouw (USDA), op basis van veiligheids-, zuiverheids-, steriliteit- en productconsistentiecriteria, en niet op basis van rigoureuze langetermijn effectiviteitsstudies. Deze situatie onderstreept de behoefte aan nieuwe regelgeving en strengere normen om de kwaliteit en effectiviteit van allergene extracten die in de diergeneeskunde worden gebruikt, te waarborgen.
De wetenschappelijke literatuur over canine ASIT lijdt onder een gebrek aan standaardisatie van protocollen, met een grote variabiliteit in doseringsschema’s, allergenische extracten, hun samenstelling en potentie tussen fabrikanten, toedieningsprogramma’s, gelijktijdige behandelingen en mengmethoden van extracten. Dit gebrek aan standaardisatie beperkt de vergelijkbaarheid van studies en de interpretatie van resultaten. De afwezigheid van gestandaardiseerde protocollen maakt het moeilijk om de werkelijke effectiviteit van ASIT te evalueren en de optimale parameters voor de behandeling van CAD te bepalen.
Details over de verschillende benaderingen:
- SCIT (Subcutaan): Het allergeen wordt onder de huid geïnjecteerd. Er bestaan verschillende benaderingen, met een geleidelijke verhoging van de doses (inductie) en een langetermijn onderhoudsschema. De extracten kunnen waterig zijn (Noord-Amerika) of aluin-precipiteerde (Europa) voor een langzamere afgifte. Het gebruik van aluin roept vragen op over de langetermijntoxiciteit van aluminium, die studies en evaluatie van de voor- en nadelen vereisen.
- SLIT (Sublinguaal): Het allergeen wordt onder de tong toegediend, een minder invasieve aanpak die mogelijk beter is voor de therapietrouw van de eigenaar. Meer studies en een betere standaardisatie zijn echter nodig voor de kalibratie ervan in veterinaire klinieken.
- RIT (Versnelde immunotherapie): Snelle toediening van toenemende doses allergeen over een korte periode, vereisend nauwe monitoring. Er is een verhoogd risico op ongewenste effecten, maar het kan handiger zijn voor sommige honden.
Verbetering van de standaardisatie van canine ASIT
Het vaststellen van de belangrijkste allergene epitopen bij honden, vooral voor veelvoorkomende allergenen, zou een standaardisatie van extracten, een uniforme dosering, de productie van recombinante allergenen en het gebruik van peptide-immunotherapie mogelijk maken. De identificatie van belangrijke allergene epitopen bij honden maakt het mogelijk specifiekere en meer gereinigde extracten te creëren. Deze gestandaardiseerde extracten bieden een betere reproduceerbaarheid van resultaten tussen verschillende studies, waardoor de betrouwbaarheid van de gegevens wordt verbeterd. Bovendien laat de kennis van epitopen de ontwikkeling van in het laboratorium gesynthetiseerde recombinante allergenen toe, wat resulteert in zuiverder en homogener allergenenpreparaten.
De dosering van het allergeen is fundamenteel. Bij mensen beïnvloeden de dosis en het injectie-interval de effectiviteit. Deze parameters zijn niet voldoende bestudeerd bij honden. Dosering-responsstudies zijn cruciaal om de optimale dosis allergeen te bepalen die de effectiviteit maximaliseert terwijl ongewenste effecten worden geminimaliseerd. De identificatie van voorspellende biomarkers van de ASIT-respons zou ook de personalisering van de behandeling op basis van de individuele respons van de hond mogelijk maken.
Evenzo biedt versnelde immunotherapie (RIT) voordelen qua aantal injecties thuis, maar ook verhoogde veiligheidsrisico’s en een hogere kost door de benodigde ziekenhuisopname. Versnelde immunotherapie (RIT) is een benadering waarmee doses allergeen sneller kunnen worden toegediend. Dit kan de behandelingsduur verminderen en de therapietrouw van de eigenaar verbeteren, maar verhoogt het risico op ongewenste effecten. Om het gebruik van RIT te optimaliseren, moet de veiligheid en effectiviteit van deze methode beter worden gedocumenteerd en mogelijk minder intensieve protocollen worden ontworpen om de risico’s te verminderen terwijl de effectiviteit behouden blijft. Vergelijkende studies tussen RIT en conventionele immunotherapie zijn nodig.
Optimalisatie van canine ASIT protocollen
De homogenisatie van canine ASIT-protocollen vertegenwoordigt een belangrijke uitdaging. Het optimale aantal extracten in een mengsel moet nog worden gedefinieerd, evenals de manier om extracten te beheren die proteasen bevatten, zoals schimmels. De standaardisatie van protocollen vereist een multifactoriele aanpak. Het is noodzakelijk om de optimale behandelingsparameters te definiëren, namelijk:
- Aantal en type allergenen: Bepaal het aantal allergenen dat in het mengsel moet worden opgenomen. Studies suggereren dat één dominant allergeen voldoende kan zijn, zelfs bij polysensibilisatie, hoewel deze benadering minder gebruikelijk is in Noord-Amerika dan in Europa.
- Beheer van proteasen: Schimmels bevatten proteasen die andere allergenen kunnen afbreken. Dit kan de effectiviteit van het allergenemengsel aantasten. Het beheer van dit probleem vereist aanvullende studie.
- Methoden voor selectie van allergenen: Gebruik intradermale testen, serologische testen, of een combinatie van beide. De beperkingen van elke methode moeten in overweging worden genomen. Er is aanvullend onderzoek nodig om de beste methode voor de selectie van allergenen voor canine ASIT te bepalen.
- Formulering van het allergenemengsel: Meer studies zijn nodig om de beste aanpak te bepalen, wat zal leiden tot een verbetering van de reproduceerbaarheid van studies.
Officiële richtlijnen raden aan om schimmel- en pollenextracten niet in dezelfde flacon te mengen vanwege de afbraak van pollenallergenen door schimmelproteasen tijdens de opslag. Vergelijkbare, maar minder doorslaggevende gegevens zijn beschikbaar voor honden. Deze aanbevelingen benadrukken de noodzaak om de interacties tussen de verschillende allergenen in het mengsel beter te begrijpen. Het is belangrijk om rekening te houden met potentiële enzymatische degradatie van de verschillende componenten in het mengsel en zo de optimale formulering te bepalen om een langdurige effectiviteit te waarborgen.
Biomarkers voor therapeutisch succes en nieuwe benaderingen
Het gebruik van biomarkers voor de objectieve evaluatie van het succes van canine ASIT is essentieel om klinische studies te verbeteren, het gebrek aan reproduceerbare gegevens te verhelpen en het belangrijke placebo-effect te overwinnen. Hoewel er toenames in totale serumconcentraties van IgG1, specifieke IgG-reacties op huisstofmijt- immunotherapie, en wijzigingen in verschillende niveaus van Treg-cellen bij honden zijn waargenomen, zijn deze ontdekkingen niet voldoende verdiept om te dienen als een middel voor objectieve en snelle evaluatie van het succes van ASIT. De identificatie van betrouwbare biomarkers zou een betere evaluatie van de effectiviteit van de behandeling en een betere voorspelling van de individuele respons op ASIT mogelijk maken.
Potentiële biomarkers die verder verkend moeten worden, omvatten:
- Serumconcentraties van IgG (vooral IgG4): De toename van specifieke IgG voor het allergeen kan correleren met een klinische verbetering. Het meten van IgG4 is bijzonder veelbelovend, omdat deze IgG-subklasse speciaal gerelateerd is aan de inductie van tolerantie.
- Regulatoire T-cellen (Treg): Het aantal en de activiteit van Treg-cellen zijn belangrijke indicatoren van de immunologische tolerantie. Het meten van circulerende Treg-cellen of in de weefsels kan nuttig zijn om de respons op ASIT te monitoren.
- Anti-inflammatoire cytokines (IL-10, TGF-β): De toename van deze cytokines kan wijzen op een afname van allergische ontsteking.
- Activiteit van effectorcellen (eosinofielen, basofielen, mestcellen): Een vermindering van de activiteit kan worden gecorreleerd met een betere klinische respons.
- Objectieve metingen van jeuk: Bijvoorbeeld het gebruik van versnellingsmeters om krabactiviteit te kwantificeren.
Het gebruik van gecombineerde biomarkers kan een vollediger beeld geven van de respons op ASIT, waardoor de interpretatie van klinische onderzoeksresultaten wordt verbeterd.
Nieuwe therapeutische benaderingen
De ontwikkeling van gemodificeerde allergeenpreparaten (allergoïden, recombinante allergenen of peptiden) en de verbetering van de effectiviteit van allergenen via adjuvantia (IL-10 inductoren, inkapseling in virusachtige deeltjes (VLPs) of in het geval van SLIT, mucoadhesieve polymeren) vertegenwoordigen veelbelovende voortgangspaden. Deze gemodificeerde preparaten bieden verschillende voordelen:
- Allergoïden: Chemisch gemodificeerde allergenen om hun vermogen om een onmiddellijke allergische reactie te veroorzaken te verminderen, terwijl hun immunogene capaciteit behouden blijft. Dit zou het risico op ongewenste effecten verminderen.
- Recombinante allergenen: In het laboratorium geproduceerde allergenen die een hogere zuiverheid en homogeniteit bieden dan natuurlijke extracten.
- Allergene peptiden: Kleine fragmenten van allergenen die specifieke epitopen voor T-lymfocyten bevatten, waardoor de risico’s op anafylaxie worden geminimaliseerd.
Het toevoegen van immunomodulators (CpG-oligodeoxynucleotiden, specifieke monoklonale antilichamen) zou de immuunrespons kunnen sturen naar specifieke tolerantie en tegelijkertijd de “cytokine storm” in actieve ontsteking matigen. Deze immunomodulators maken manipulatie van de immuunrespons mogelijk, bevorderen anti-inflammatoire reacties en immuuntolerantie. CpG ODN stimuleren de aangeboren immuniteit door het activeren van dendritische cellen en NK-cellen, en monoklonale antilichamen kunnen specifieke pro-inflammatoire cytokines targeten.
Onderzoeken naar alternatieve toedieningswegen (epicutane of intralymfatische immunotherapie) blijken veelbelovend. Epicutane immunotherapie, lokaal op de huid aangebracht, zou een lokale en systemische tolerantie voor allergenen kunnen induceren. Intralymfatische immunotherapie, waarbij het allergeen direct in de lymfeklieren wordt geïnjecteerd, zou het contact met immuuncellen die betrokken zijn bij de ontwikkeling van tolerantie kunnen optimaliseren. Hoewel er studies bestaan over intralymfatische immunotherapie bij honden, is aanvullend onderzoek nodig om de optimale protocollen te verduidelijken en de effectiviteit en veiligheid op lange termijn te evalueren. Bovendien zou intralymfatische immunotherapie minder belastend kunnen zijn voor de eigenaar in vergelijking met klassieke subcutane immunotherapie, wat de therapeutische naleving zou verbeteren.
Bovendien zouden de vorderingen in immunotherapie voor menselijke voedselallergieën, met name het gebruik van moleculaire diagnostiek en alternatieve toedieningsmethoden, innovatieve benaderingen voor DAC kunnen inspireren. De optimalisatie van de diagnose van voedselallergieën bij honden is een belangrijke onderzoeksspeerpunt. Nauwkeuriger moleculaire diagnostische methoden zouden de specifieke voedselallergenen kunnen identificeren die reacties veroorzaken. Nieuwe toedieningsmethoden, zoals orale behandelingen, zouden de tolerantie van honden voor voedselallergenen kunnen verbeteren. De vorderingen bij de mens zouden als inspiratie kunnen dienen voor het aanpassen van deze benaderingen in de context van DAC.
ASIT in het licht van nieuwe behandelingen
Ten slotte is het belangrijk om te onthouden dat, gezien de effectiviteit van nieuwe behandelingen zoals ciclosporine, oclacitinib of anti-IL-31 monoklonale antilichamen, de plaats van ASIT in de multimodale behandeling van allergieën bij honden constante reflectie vereist. Niettemin blijft ASIT de enige therapie die in staat is om tenminste een deel van de pathogenese te wijzigen of om te keren, en biedt het vooruitzicht op een definitieve genezing. Het is dus essentieel dat ASIT wordt beschouwd, niet als een laatste redmiddel, maar als een haalbare eerste behandelingsoptie. ASIT kan een voorkeursbehandelingsoptie zijn in eerste instantie, met name bij honden die niet goed reageren op conventionele medicamenteuze behandelingen of bijwerkingen van deze medicijnen vertonen. De combinatie van ASIT met andere behandelingen kan de algehele effectiviteit in de behandeling van DAC verbeteren. Het is belangrijk om rekening te houden met het veiligheidsprofiel en de relatieve effectiviteit van de verschillende beschikbare behandelingen.
Vergelijking met alternatieve behandelingen: Ciclosporine, oclacitinib en anti-IL-31 monoklonale antilichamen zijn effectieve behandelingen om de symptomen van DAC te verlichten, maar ze veranderen de pathogenese van de ziekte niet en langdurige toediening is noodzakelijk. ASIT daarentegen richt zich op de onderliggende oorzaak van de allergie, door de immuunrespons van de hond te wijzigen. Hoewel ASIT enige tijd kan duren voordat het effect heeft, biedt het volledig herstel op termijn, in tegenstelling tot symptomatische behandelingen. Het gecombineerd gebruik van ASIT en symptomatische behandelingen is een mogelijke aanpak.
Conclusie en vooruitzichten
Concluderend kan worden gesteld dat hoewel ASIT een veelbelovende therapeutische optie is voor atopische dermatitis bij honden, de effectiviteit ervan formeel moet worden aangetoond door middel van rigoureus en beter gestandaardiseerd klinisch onderzoek. De werkingsmechanismen blijven raadselachtig en aanvullende onderzoekspaden zijn nodig. Meer en strengere studies zijn essentieel om de huidige kennislacunes te overbruggen. Het is met name nodig om de werkingsmechanismen beter te begrijpen, de optimale behandelingsparameters te bepalen en betrouwbare biomarkers te identificeren om de effectiviteit te evalueren en de respons te voorspellen.
Toekomstige studies moeten zich richten op:
- Precieze identificatie van hondenallergenen: Ontwikkeling van nauwkeurigere en gestandaardiseerde diagnostische tests om de betrokken allergenen te identificeren.
- Optimalisatie van toedieningsprotocollen: Standaardisatie van protocollen en vergelijking van verschillende toedieningsmethoden (SCIT, SLIT, RIT, ILIT). Strikte vergelijkende studies zijn nodig.
- Identificatie van voorspellende biomarkers voor therapeutisch succes: Bepalen van markers die de respons op de behandeling kunnen voorspellen voordat deze wordt toegediend. Dit zal helpen bij het personaliseren van de behandeling.
- Verkenning van gemodificeerde allergeenpreparaten: Test de effectiviteit van recombinante allergenen, peptiden en allergoïden. Deze zuiverdere formuleringen kunnen de veiligheid en effectiviteit verbeteren.
- Immunomodulatorische strategieën: Test de toepassing van immunomodulators om de immuunrespons te beïnvloeden en tolerantie te optimaliseren.
- Langetermijnstudies: Evalueer de langetermijneffecten van verschillende protocollen om een beter begrip te krijgen van de duurzaamheid van de effectiviteit van de behandeling.
ASIT kan zo een eerstelijnsbehandeling worden bij de behandeling van DAC, in plaats van beperkt te blijven tot een tweede optie. De verbetering van protocollen, standaardisatie, en de ontwikkeling van nieuwe diagnostische en therapeutische middelen zullen van ASIT een voorkeursinstrument maken bij de behandeling van atopische dermatitis bij honden.
FAQs
Q1: Wat zijn de beperkingen van intradermale en serologische tests voor de diagnose van DAC?
Intradermale tests (IDT) en serologische tests voor de bepaling van specifieke IgE voor allergenen (ASIS) hebben beperkingen. De IDT meten niet de gevoeligheid van alle allergieroutes en vals-positieve reacties bij niet-allergische honden worden beschreven. Vals-positieve reacties komen vaker voor bij hogere concentraties, en positieve resultaten kunnen verband houden met een niet-specifieke gevoeligheid van IgE (kruisreacties met andere allergenen). De ASIS meten alleen de circulerende IgE die specifiek zijn voor het allergeen en houden geen rekening met andere allergieroutes, en vals-positieve reacties zijn ook waargenomen. Bovendien ontbreekt bij beide tests de standaardisatie en zijn fout-positieve en fout-negatieve resultaten mogelijk. De gevoeligheid kan van laboratorium tot laboratorium variëren.
Het wordt geschat dat tussen de 10 en 30 % van de honden met klinisch bevestigde DAC een negatieve IDT kunnen vertonen, als gevolg van verschillende factoren zoals de techniek, de concentratie van allergenen, medicamenteninterferenties, intrinsieke factoren van de gastheer of een onjuiste keuze van allergenen. De beperkingen van intradermale tests omvatten ook de noodzaak van een specifieke voorbereiding van de hond (scheren, enz.), het risico op lokale reacties en de subjectiviteit bij de interpretatie van de resultaten. Serologische tests (ASIS) vermijden deze nadelen, maar hebben beperkingen wat betreft gevoeligheid en specificiteit; positieve reacties kunnen worden waargenomen bij niet-allergische honden.
Op het einde hebben deze allergietests alleen nut bij het bepalen van de allergenen die in de desensibilisatie moeten worden opgenomen, en in geen geval voor de diagnose van atopische dermatitis bij honden.
Q2: Hoe de allergenen kiezen voor een ASIT-protocol?
De keuze van allergenen voor een ASIT-protocol moet gebaseerd zijn op de klinische voorgeschiedenis van het dier, in combinatie met de positieve reacties op intradermale of serologische tests. Vertrouw echter niet alleen op de tests, want positieve reacties kunnen worden waargenomen bij gezonde honden, waarbij de reacties niet noodzakelijkerwijs een klinische overgevoeligheid weerspiegelen. Een zorgvuldige interpretatie van de klinische voorgeschiedenis en correlatie met de testresultaten maakt het mogelijk om de relevante allergenen voor het opstellen van het therapeutische protocol te identificeren. In sommige gevallen kan provocatietests worden overwogen.
Q3: Wat zijn de voor- en nadelen van versnelde immunotherapie (RIT)?
Versnelde immunotherapie (RIT) vermindert de inductieduur in vergelijking met conventionele immunotherapie. Bij honden wordt RIT goed verdragen, met zeldzaam belangrijke neveneffecten, voornamelijk jeuk. Echter, klinische ziekenhuisbewaking is vereist, en dit type benadering brengt grotere veiligheidsrisico’s met zich mee, evenals hogere kosten. RIT kan worden overwogen bij honden met een laag risico op anafylaxie, wat tijdwinst oplevert als de tolerantie goed is. Optimalisatie van de protocollen zal een diepere evaluatie vereisen om optimale veiligheidsparameters te identificeren en ongewenste reacties te voorkomen. Vergelijking met klassieke RIT is noodzakelijk.
Q4: Wat zijn de nieuwe onderzoeksrichtingen betreffende canine ASIT?
Meerdere onderzoeksrichtingen verdienen verdere exploratie: het gebruik van gemodificeerde allergeenpreparaten (allergoïden, recombinante allergenen, peptiden), de ontwikkeling van nieuwe adjuvantia om de effectiviteit en veiligheid van de behandeling te verbeteren, de identificatie van biomarkers voor therapeutisch succes en de standaardisatie van protocollen. Het verkennen van innovatieve toedieningstechnieken, zoals intralymfatische, epicutane of orale immunotherapie, is ook veelbelovend. Onderzoek naar canine ASIT is een voortdurend ontwikkelend veld, en nieuwe onderzoekspistes worden altijd verkend. Een standaardisatie-inspanning om de betrouwbaarheid van studies te verbeteren is van wezenlijk belang.
Q5: Zijn er medicijninteracties waarmee rekening moet worden gehouden voordat huidtests worden uitgevoerd?
De toediening van medicijnen kan de resultaten van IDT beïnvloeden. Sommige medicijnen, zoals antihistaminica, glucocorticoïden, ciclosporine en tricyclische antidepressiva kunnen interfereren met IDT. Een stopzettingsperiode van sommige medicijnen kan nodig zijn voordat een IDT wordt uitgevoerd. Mogelijke medicamenteuze interacties moeten overwogen worden voor aanvang van de behandeling. Het effect van de medicijnen moet in overweging worden genomen voordat de tests worden uitgevoerd. Een overleg met de dierenarts is essentieel om eventuele stopzetting van bepaalde medicijnen vóór de uitvoering van de tests te bepalen. Er moet rekening worden gehouden met een mogelijke interactie met het medicijn gebruikt bij de behandeling van de ziekte.
Referenties
Hensel P, Santoro D, Favrot C, Hill P, Griffin C. Canine atopische dermatitis: gedetailleerde richtlijnen voor diagnose en allergeenidentificatie. BMC Veterinary Research 2015; 11:196. DOI: 10.1186/s12917-015-0515-5.
Mueller RS. Update over Allergen Immunotherapie. Vet Clin Small Anim 2019; 49: 1–7. DOI: 10.1016/j.cvsm.2018.08.001.
DeBoer DJ. De toekomst van immunotherapie voor canine atopische dermatitis: een overzicht. Vet Dermatol 2017; 28: 25–66. DOI: 10.1111/vde.12416.
Pinto MSN, Gil SJRC, Ramió-Lluch L, et al. De norm uitdagen: Epicutane immuuntherapie voor dermatitis atopica bij honden. Allergy 2023; 78: 255–257. DOI: 10.1111/all.15946.
Gerelateerde zoekopdrachten
atopische dermatitis hond, atopische dermatitis, allergische aandoening, honden atopie, atopische hond, allergische reacties, bepaalde rassen gevoeliger, allergie opwekkende stof, bepaalde allergenen, atopie hond, bepaalde rassen, atopie bij honden, genetische aanleg, droge huid, allergenen waarvoor, chronische huidziekte, allergische reacties veroorzaakt, symptomatische behandeling, meest voorkomende oorzaken, bloedonderzoek gedaan, secundaire infecties, ernstige jeuk, hond gaat, honden, duitse herder, normaal gesproken, vroegtijdige behandeling, allergenen, belangrijkste symptomen, allergie, huid, klachten verminderen, iedere hond, dermatitis bij de hond, klachten veroorzaakt, kale plekken, opwekkende stof, lichaam beschermt, west highland white terriër, langdurige achtergrondbehandeling, uitgebreide huidtest, algemeen seizoensgebonden, jonge leeftijd, helaas veroorzaakt, symptomen, dierenarts, zwart verkleuren, atopie, pollen, heftige reactie, controle houden, jeuk, grootste orgaan, bloed gekeken, vlooien, kleine hoeveelheid, schimmels, gebruik gemaakt, hond met atopie, hierdoor went, diagnose, huisstofmijt, oorzaak, immuunsysteem, huidproblemen, roodheid, ziekte, graspollen, aandoening, bloedonderzoek