La pododermatite plasmocitaria è una dermatosi felina rara e poco compresa, che non deve tuttavia essere trascurata in consultazione, in particolare a causa del dolore e quindi della zoppia che può provocare. Panoramica delle ultime conoscenze, sia in termini di eziopatogenesi, che di diagnosi e degli ultimi trattamenti e protocolli pubblicati.
Introduzione e quadro nosologico
1.1. Definizione e denominazione
La pododermatite plasmocitaria felina (PPF) costituisce una dermatosi infiammatoria rara, caratterizzata da un’infiltrazione massiva di plasmacellule mature nel derma dei cuscinetti plantari del gatto. Questa entità, familiarmente designata con il termine anglofono di pillow foot a causa dell’aspetto tumefatto e molle dei cuscinetti colpiti, occupa un posto singolare nel panorama dermatologico veterinario (Miller 2013). La malattia si distingue per il suo tropismo esclusivo per il tessuto podale, senza equivalente esatto nel cane o nell’uomo, benché parallelismi fisiopatologici possano essere stabiliti con alcune proliferazioni plasmocitarie cutanee umane. Sul piano nosologico, la PPF appartiene al gruppo delle dermatosi plasmocitarie feline, uno spettro che include la stomatite plasmocitaria cronica e, in modo più controverso, alcune forme di dermatite plasmocitaria extra-podale (Gross 2005). L’infiltrato è composto per oltre il 90% da plasmacellule ben differenziate che esprimono il marcatore CD138 (syndecan-1), ciò che la distingue formalmente dalle neoplasie plasmocitarie come il plasmocitoma extramidollare, dove l’indice di proliferazione Ki-67 supera abitualmente il 20% (Mauldin 2016).
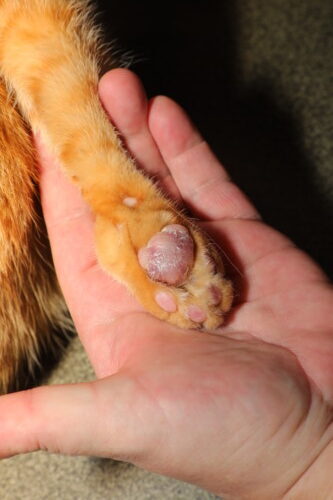
Aspetto classico di una pododermatite plasmocitaria felina
1.2. Tappe storiche ed evoluzione delle conoscenze
Le prime descrizioni clinico-patologiche della PPF risalgono alla fine degli anni ’70, quando Gruffydd-Jones, Orr e Lucke pubblicano nel 1980 una serie di cinque gatti che presentavano un rigonfiamento e un’ulcerazione dei cuscinetti associati a un’infiltrazione plasmocitaria dermica densa (Gruffydd-Jones 1980). Questa pubblicazione fondatrice stabilisce i criteri morfologici di base che guidano ancora il riconoscimento dell’affezione. Nel corso del decennio successivo, Taylor e Schmeitzel riportano nel 1990 due casi complicati da emorragie croniche a livello dei cuscinetti, sottolineando il potenziale evolutivo della malattia verso l’ulcerazione profonda e la fragilizzazione vascolare (Taylor 1990). L’avvento dei test sierologici per il virus dell’immunodeficienza felina (FIV) negli anni ’90 ha permesso di mettere in luce un’associazione statistica tra retrovirus e PPF, un legame esplorato in diverse serie retrospettive che mostrano una sieroprevalenza FIV che varia dal 20 al 62% nei gatti colpiti, contro il 2-4% nella popolazione felina generale (Guaguère 2004; Dias Pereira 2003). Lo studio retrospettivo di Guaguère e collaboratori, che porta su 26 casi, costituisce a oggi una delle coorti più ampie pubblicate e ha contribuito ad affinare la comprensione del profilo epidemiologico e della risposta terapeutica (Guaguère 2004). L’introduzione della doxiciclina come trattamento di prima intenzione, all’inizio degli anni 2000, ha rappresentato una svolta terapeutica, offrendo un’alternativa alla corticoterapia a lungo termine con un tasso di risposta completa che si aggira intorno al 50-65% secondo le serie (Bettenay 2003).
Epidemiologia
2.1. Prevalenza e dati di incidenza
La PPF rimane un’affezione poco frequente la cui prevalenza esatta resta difficile da stabilire, in parte a causa di una probabile sottodiagnosi legata alla risoluzione spontanea di alcune forme benigne. I dati disponibili, provenienti da centri di riferimento in dermatologia veterinaria, situano la sua frequenza tra lo 0,5 e l’1,5% dell’insieme delle consultazioni dermatologiche feline (Miller 2013). Nella serie di Dias Pereira e Faustino, che analizza 8 casi diagnosticati in un periodo di sette anni in un centro universitario portoghese, l’incidenza annuale è stimata a circa 1,1 casi per 1.000 consultazioni feline (Dias Pereira 2003). Questa relativa rarità non esclude una prevalenza sottostimata nella pratica corrente, nella misura in cui gli stadi precoci non ulcerati passano frequentemente inosservati. Non è stata riportata alcuna variazione geografica significativa, i casi essendo documentati in tutti i continenti, dall’Europa all’America del Nord, passando per l’Asia e l’Australia (Hnilica 2017). Il carattere sporadico della malattia, senza fenomeno di clustering temporale o spaziale, depone contro un’eziologia infettiva trasmissibile diretta e orienta maggiormente verso una patogenesi disimmunitaria individuale.
2.2. Fattori di rischio demografici: razza, età e sesso
Contrariamente a numerose dermatosi feline per le quali è stato identificato un determinismo genetico — per esempio il gene PNPLA1 nell’ittiosi del Golden Retriever o il gene KRT10 nell’ittiosi epidermolitica —, nessuna predisposizione di razza chiara è stata dimostrata per la PPF (Miller 2013). La maggioranza dei casi riportati riguarda gatti di tipo europeo a pelo corto, ciò che riflette la predominanza di questa popolazione nelle consultazioni veterinarie piuttosto che una suscettibilità genetica specifica. La coorte di Guaguère includeva 23 gatti europei su 26 (88,5%), i tre restanti essendo rispettivamente un Persiano, un Siamese e un Certosino (Guaguère 2004). L’analisi della serie di Dias Pereira conferma questa assenza di predisposizione di razza, con una distribuzione proporzionale alla popolazione di riferimento (Dias Pereira 2003).
L’età al momento della diagnosi varia considerevolmente, andando da 6 mesi a 14 anni, con una mediana che si situa tra 4 e 7 anni secondo gli studi (Gross 2005; Guaguère 2004). Questa ampia fascia d’età suggerisce che la malattia non corrisponde né a un’affezione giovanile di sviluppo, né a una patologia strettamente geriatrica, ma che può sopravvenire in qualsiasi momento della vita adulta in funzione della convergenza di fattori immunologici individuali. Per quanto riguarda il sesso, i dati restano contraddittori. Alcune serie riportano una leggera predominanza per i maschi con un sex-ratio di 1,4:1 a favore dei maschi (Guaguère 2004), mentre altre non riscontrano alcuna differenza significativa. Lo stato riproduttivo (intero o sterilizzato) non sembra esercitare un’influenza determinante, benché la maggior parte dei gatti inclusi negli studi pubblicati siano sterilizzati, conformemente alle pratiche di gestione della popolazione felina domestica in vigore nei paesi industrializzati. L’assenza di un polimorfismo genetico identificato associato alla PPF contrasta con altre dermatosi immunitarie feline, come il complesso granuloma eosinofilico dove sono stati sospettati fattori genetici poligenici, e rafforza l’ipotesi di una patogenesi acquisita che implica cofattori ambientali o infettivi.
Eziopatogenesi: una disregolazione immunitaria multifattoriale
3.1. Argomenti a favore di un’origine disimmunitaria
L’eziologia della PPF resta a oggi incompletamente chiarita, ma l’insieme dei dati clinici, biologici e istopatologici convergono verso una patogenesi a mediazione immune. Diversi argomenti sostengono questa ipotesi. Il primo si basa sulla natura stessa dell’infiltrato, composto quasi esclusivamente da plasmacellule mature policlonali, indicatori di un’attivazione antigenica cronica e sostenuta del compartimento linfocitario B. L’analisi immunoistochimica rivela che queste plasmacellule esprimono sia le catene leggere kappa che lambda delle immunoglobuline in un rapporto fisiologico di circa 2:1, escludendo un processo monoclonale neoplastico (Gross 2005; Mauldin 2016). Il secondo argomento deriva dall’ipergammaglobulinemia policlonale documentata nel 50-63% dei gatti colpiti, testimoniando una stimolazione diffusa del sistema immunitario umorale, senza specificità antigenica identificata (Guaguère 2004). L’elettroforesi delle proteine sieriche mette in evidenza un’elevazione delle frazioni gamma senza picco monoclonale, distinguendo formalmente questa condizione da un mieloma multiplo o da un plasmocitoma secernente. Infine, la risposta favorevole ad agenti immunomodulatori o immunosoppressori — doxiciclina, glucocorticoidi, ciclosporina — costituisce un argomento terapeutico indiretto a favore di un meccanismo disimmunitario (Bettenay 2003; Miller 2013).
La rilevazione di anticorpi antinucleari (ANA) in una proporzione non trascurabile di gatti colpiti, stimata tra il 25 e il 50% secondo le serie, rafforza l’ipotesi autoimmune, benché il significato clinico di questi ANA resti dibattuto in medicina felina (Dias Pereira 2003). La loro presenza potrebbe riflettere un’attivazione linfocitaria non specifica piuttosto che una vera reattività autodiretta. L’analisi mediante immunofluorescenza diretta delle biopsie di cuscinetti ha dimostrato depositi di IgG, IgM e della frazione C3 del complemento alla giunzione dermo-epidermica e attorno ai vasi dermici nella maggioranza dei casi, un pattern evocativo di una malattia da immunocomplessi (Gross 2005). Questi depositi ricordano quelli osservati nel lupus eritematoso sistemico felino, suggerendo un meccanismo fisiopatologico parzialmente condiviso che implica la via classica del complemento innescata dalla fissazione del frammento C1q ai complessi antigene-anticorpo.
3.2. Implicazione del virus dell’immunodeficienza felina e dei retrovirus
L’associazione tra PPF e infezione da FIV costituisce uno degli aspetti più discussi dell’eziopatogenesi. Diversi studi retrospettivi riportano una sieroprevalenza FIV significativamente più elevata nei gatti colpiti da PPF che nella popolazione generale. Nella serie di Guaguère, il 50% dei 26 gatti testati erano sieropositivi per il FIV, un tasso nettamente superiore alla prevalenza attesa del 2-4% nella popolazione felina domestica europea (Guaguère 2004). Dias Pereira e Faustino riscontrano una sieroprevalenza del 62,5% nella loro coorte di 8 casi (Dias Pereira 2003). Il FIV, un lentivirus della famiglia dei Retroviridae, provoca una disregolazione profonda dell’immunità adattativa mediante deplezione progressiva dei linfociti T CD4+ e mediante attivazione policlonale cronica dei linfociti B. Questo fenomeno, mediato dalla stimolazione diretta del recettore Toll-like 7 (TLR7) da parte dell’RNA virale a singolo filamento e dalla secrezione aberrante di IL-6, favorisce la differenziazione plasmocitaria e la produzione di immunoglobuline non specifiche (Hartmann 2012). L’attivazione della via JAK1/STAT3 a valle del recettore dell’IL-6 costituisce un meccanismo chiave di questa plasmocitogenesi eccessiva, il fattore di trascrizione STAT3 fosforilato traslocando al nucleo per indurre l’espressione di BLIMP-1 (PRDM1), il regolatore principale della differenziazione terminale dei linfociti B in plasmacellule (Nutt 2015).
L’associazione con il virus della leucemia felina (FeLV) è meno ben documentata, con tassi di sieroprevalenza che oscillano tra lo 0 e il 20% secondo le coorti, cifre che non differiscono sempre significativamente dalla popolazione di riferimento (Guaguère 2004; Miller 2013). La PPF può tuttavia sopravvenire in gatti sieronegativi sia per il FIV che per il FeLV, ciò che indica che l’infezione retrovirale non è né necessaria né sufficiente per scatenare la malattia. Essa agisce probabilmente come cofattore amplificatore di una disregolazione immunitaria preesistente, abbassando la soglia di tolleranza e favorendo la rottura dell’omeostasi del compartimento B.
3.3. Cofattori ambientali e infettivi sospettati
Oltre ai retrovirus, altri agenti infettivi sono stati sospettati come potenziali fattori scatenanti senza che sia stata apportata una prova formale. Alcuni autori hanno evocato il ruolo di stimolazioni antigeniche croniche legate ad agenti batterici o fungini a contatto con i cuscinetti, ma nessuna coltura microbiologica sistematica ha dimostrato un agente patogeno specifico associato alla malattia (Miller 2013). L’ipotesi di un’ipersensibilità da contatto o di una reazione a corpo estraneo è stata avanzata, senza supporto sperimentale. Casi di PPF sopravvenuti dopo vaccinazione o cambio alimentare sono stati riportati in modo aneddotico, ma nessun legame causale è stato stabilito (Scarampella 2004). Il ruolo di fattori epigenetici che modulano l’espressione di geni implicati nella regolazione del compartimento B — come le modificazioni post-traduzionali degli istoni o la metilazione del DNA a livello dei promotori di PRDM1 e IRF4 — resta un campo di ricerca inesplorato in medicina felina.
Immunopatologia molecolare
4.1. Ontogenesi plasmocitaria e vie di segnalazione implicate
La comprensione della PPF richiede una conoscenza approfondita della biologia delle plasmacellule. La differenziazione terminale del linfocita B in plasmacellula matura secretrice di immunoglobuline è orchestrata da una rete gerarchizzata di fattori di trascrizione. Il fattore BLIMP-1, codificato dal gene PRDM1, agisce come repressore trascrizionale del programma B cellulare, inibendo l’espressione di PAX5 e BCL6, due fattori indispensabili al mantenimento dell’identità del linfocita B germinale (Nutt 2015). Simultaneamente, il fattore IRF4 (MUM1) si lega in sinergia con BLIMP-1 per attivare il programma secretorio, inducendo l’espressione di XBP1, un mediatore chiave della risposta alle proteine mal ripiegate (unfolded protein response, UPR) che permette l’espansione del reticolo endoplasmatico necessaria alla produzione massiva di immunoglobuline. Nel contesto della PPF, questa cascata appare costitutivamente attivata nelle plasmacellule residenti del derma dei cuscinetti, come suggerisce l’immunomarcatura intensa di MUM1/IRF4 e di CD138 (syndecan-1) osservata sulle biopsie (Mauldin 2016; Gross 2005).
La via di segnalazione IL-6/JAK1/STAT3 svolge un ruolo centrale nell’espansione plasmocitaria. L’interleuchina 6, prodotta localmente dai macrofagi e dai fibroblasti dermici in risposta a segnali infiammatori, si lega al suo recettore di membrana (IL-6Rα/gp130), attivando la tirosina chinasi JAK1 che fosforila il fattore STAT3. STAT3 fosforilato dimerizza e transloca al nucleo, dove induce direttamente la trascrizione di PRDM1 e di IRF4 (Nutt 2015). Questo circuito autocrino e paracrino potrebbe essere perpetuato nei cuscinetti da un microambiente ricco di citochine pro-infiammatorie, in particolare TNF-α e IL-1β, che stimolano a loro volta la produzione di IL-6 da parte delle cellule stromali via l’attivazione della via canonica NF-κB (p65/RelA). La citochina BAFF (B-cell Activating Factor, chiamato anche BLyS), membro della superfamiglia del TNF, costituisce un fattore di sopravvivenza determinante per le plasmacellule a lunga durata di vita. BAFF si lega ai recettori BCMA e TACI espressi sulla superficie delle plasmacellule, attivando la via NF-κB non canonica (RelB/p52) e inibendo l’apoptosi mitocondriale mediante sovraespressione di BCL-2 e MCL-1 (Mackay 2009). Un eccesso di BAFF sierico, documentato in diverse malattie autoimmuni umane, potrebbe costituire un meccanismo fisiopatologico analogo nella PPF, benché il dosaggio di questa citochina non sia ancora stato realizzato specificamente nel gatto colpito.
4.2. Ipergammaglobulinemia e depositi di immunocomplessi
L’ipergammaglobulinemia policlonale, riscontrata nel 50-63% dei gatti colpiti da PPF, traduce l’attivazione diffusa e non specifica del compartimento plasmocitario (Guaguère 2004). L’elettroforesi delle proteine sieriche rivela un’elevazione della frazione gamma senza picco ristretto, con tassi di IgG che possono raggiungere due o tre volte il limite superiore della norma. La produzione eccessiva di immunoglobuline, in assenza di un antigene bersaglio identificato, conduce alla formazione di immunocomplessi circolanti che si depositano nei tessuti ad alta vascolarizzazione, in particolare i glomeruli renali e il derma dei cuscinetti. Questi depositi sono stati messi in evidenza mediante immunofluorescenza diretta sotto forma di depositi granulari di IgG, IgM e della frazione C3 del complemento lungo la membrana basale epidermica e attorno alle pareti vascolari dermiche (Gross 2005). Il meccanismo di deposito ricorda quello della reazione di ipersensibilità di tipo III (classificazione di Gell e Coombs), dove gli immunocomplessi di dimensione intermedia sfuggono alla clearance da parte del sistema reticolo-endoteliale e precipitano nelle pareti vascolari, innescando una cascata infiammatoria locale.
4.3. Attivazione del complemento e cascata infiammatoria
I depositi di immunocomplessi attivano la via classica del complemento mediante fissazione del frammento C1q alla porzione Fc delle immunoglobuline aggregate. Questa attivazione sequenziale (C1q → C1r/C1s → C4 → C2 → C3 convertasi) porta al clivaggio di C3 in C3a (anafilotossina) e C3b (opsonina), poi alla formazione del complesso di attacco di membrana C5b-9 che provoca una lisi cellulare diretta (Gross 2005). Le anafilotossine C3a e C5a agiscono come potenti chemoattrattori per i neutrofili e i macrofagi, amplificando l’infiammazione locale. Il rilascio di proteasi lisosomiali (elastasi, catepsina G) da parte dei neutrofili reclutati contribuisce alla degradazione della matrice extracellulare del derma dei cuscinetti, spiegando la texture molle e spugnosa caratteristica del tessuto colpito (Miller 2013). Il dosaggio del C3 sierico, quando è stato realizzato, mostra talvolta una diminuzione compatibile con un consumo per attivazione in vivo, un fenomeno classico delle malattie da immunocomplessi.
4.4. Metalloproteinasi matriciali e distruzione tissutale
Il rimodellamento distruttivo del tessuto connettivo dei cuscinetti fa intervenire le metalloproteinasi matriciali (MMP), una famiglia di endopeptidasi zinco-dipendenti capaci di degradare i componenti della matrice extracellulare. Le MMP-2 (gelatinasi A) e MMP-9 (gelatinasi B) sono particolarmente implicate nella degradazione del collagene di tipo IV e della laminina a livello della membrana basale, mentre la MMP-1 (collagenasi interstiziale) cliva il collagene fibrillare di tipo I e III che costituisce l’essenziale dell’armatura dermica del cuscinetto (Sapadin 2006). L’espressione di queste MMP è indotta dal TNF-α e dall’IL-1β via l’attivazione del fattore di trascrizione AP-1 (c-Fos/c-Jun) e della via NF-κB. La distruzione collagenina progressiva, combinata con l’edema infiammatorio e l’infiltrazione cellulare massiva, porta all’aumento di volume caratteristico del cuscinetto, la cui consistenza passa da ferma a pastosa. Il ruolo centrale delle MMP nella patogenesi offre un razionale farmacologico diretto per l’utilizzo della doxiciclina, la cui attività inibitoria sulle MMP costituisce uno dei meccanismi d’azione meglio documentati indipendentemente dalla sua attività antibatterica (Griffin 2010).
Presentazione clinica
5.1. Semeiotica dei cuscinetti
Il quadro clinico della PPF è abitualmente caratteristico e permette un orientamento diagnostico fin dall’esame macroscopico. La lesione elementare consiste in un rigonfiamento diffuso e simmetrico di uno o più cuscinetti, conferendo al cuscinetto colpito un aspetto tumefatto, arrotondato, sensibilmente più voluminoso del normale. I cuscinetti metacarpali e metatarsali centrali sono colpiti in modo preferenziale in oltre l’80% dei casi, benché i cuscinetti digitali possano essere ugualmente implicati (Miller 2013). Il coinvolgimento è il più delle volte bilaterale e tocca simultaneamente i quattro arti in circa il 50% dei casi riportati (Guaguère 2004). La superficie del cuscinetto presenta una colorazione violetto bluastro o lilla, talvolta descritta come una cianosi locale, che traduce la congestione vascolare e l’infiammazione dermica profonda. Questa tinta si osserva soprattutto sui cuscinetti a pigmentazione chiara e può essere mascherata sui cuscinetti naturalmente scuri. Un segno semiologico molto evocativo risiede nell’aspetto striato della superficie, con fini strie biancastre intrecciate che formano una rete a maglie (cross-hatching), che risulta dalla tensione esercitata dal tessuto edematoso sull’epidermide assottigliata del cuscinetto (Gross 2005). La palpazione rivela una consistenza molle e pastosa, nettamente distinta dalla fermezza normale del cuscinetto sano, traducendo la distruzione dell’architettura collagenina dermica e l’infiltrazione cellulare massiva. Il dolore è generalmente assente negli stadi precoci, e la zoppia, quando è presente, traduce il più delle volte un’ulcerazione secondaria.
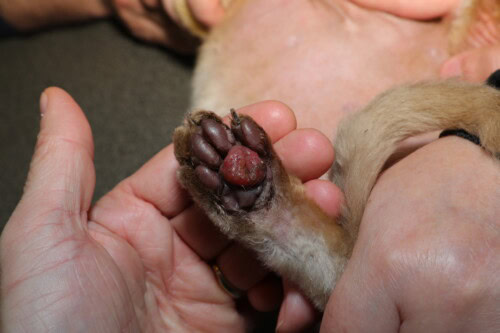
Forma evoluta con apertura del cuscinetto centrale
5.2. Evoluzione naturale e complicazioni
L’evoluzione della PPF è variabile e imprevedibile. Una proporzione significativa di casi, stimata tra il 10 e il 30%, può presentare una risoluzione spontanea senza intervento terapeutico, in un termine di alcune settimane o alcuni mesi (Miller 2013). Questa regressione spontanea rafforza l’ipotesi di un processo reazionale a uno stimolo antigenico transitorio. Tuttavia, l’evoluzione verso l’ulcerazione costituisce la complicazione più temuta, sopravvenendo nel 30-50% dei casi non trattati (Guaguère 2004). L’ulcerazione si manifesta con una perdita di sostanza dell’epidermide del cuscinetto, esponendo il derma infiltrato e fragile, spesso accompagnata da un’emorragia secondaria talvolta profusa a causa della neovascolarizzazione infiammatoria e della fragilità delle pareti vascolari indebolite dai depositi di immunocomplessi e dall’azione delle MMP (Taylor 1990). La sovrainfezione batterica dell’ulcera costituisce un rischio aggiuntivo, benché non sia sistematica. Il dolore che accompagna l’ulcerazione provoca allora una zoppia marcata, una riluttanza al movimento e talvolta un leccamento compulsivo che mantiene il fenomeno erosivo. Alcuni casi eccezionali di sanguinamenti ricorrenti che hanno condotto a un’anemia sideropenica sono stati documentati, sottolineando la necessità di un follow-up ematologico nei gatti che presentano ulcerazioni croniche (Taylor 1990).
5.3. Manifestazioni extra-podali associate
La PPF non si limita sempre a un coinvolgimento podologico isolato. Associazioni con altre manifestazioni plasmocitarie sono state documentate, suggerendo un processo sistemico sottostante. La stomatite plasmocitaria, caratterizzata da un’infiltrazione plasmocitaria della mucosa buccale (in particolare del palato e delle arcate glosso-palatine), è stata descritta in concomitanza con la PPF nel 10-20% dei casi secondo le serie (Miller 2013; Guaguère 2004). L’associazione simultanea di queste due entità in uno stesso animale costituisce un argomento forte a favore di un disordine sistemico del compartimento B. Coinvolgimenti renali, sotto forma di glomerulonefrite da depositi di immunocomplessi o, più raramente, di amiloidosi renale reattiva di tipo AA, sono stati riportati in gatti colpiti da PPF cronica (Dias Pereira 2003). Il deposito di sostanza amiloide, costituita da fibrille derivate dalla proteina sierica amiloide A (SAA) prodotta in eccesso dal fegato sotto la stimolazione di IL-6 e TNF-α durante l’infiammazione cronica, può condurre a un’insufficienza renale progressiva. Queste associazioni morbose conferiscono alla PPF una dimensione sistemica che supera il quadro strettamente dermatologico e giustifica un bilancio biologico completo in ogni gatto diagnosticato.
Approccio diagnostico
6.1. Esame clinico e criteri di orientamento
La diagnosi della PPF si basa su un insieme di argomenti clinici, citologici e istopatologici. L’esame clinico attento dei quattro arti, includendo l’ispezione e la palpazione di tutti i cuscinetti, costituisce la prima tappa. La congiunzione di un rigonfiamento non dolente di uno o più cuscinetti centrali, di una tinta violacea e di una consistenza pastosa in un gatto adulto orienta fortemente la diagnosi. L’esame dermatologico completo deve ricercare eventuali lesioni cutanee associate su altri siti, così come un esame della cavità buccale alla ricerca di una stomatite plasmocitaria concomitante. La valutazione dello stato generale, della palpazione renale e dello stato linfonodale fa parte del bilancio clinico iniziale (Miller 2013).
6.2. Apporto della citologia
La citoaspirazione con ago sottile del cuscinetto gonfio, realizzata con un ago da 22 a 25 gauge, costituisce un esame complementare rapido e poco invasivo, praticabile in consultazione. Lo striscio su vetrino e la colorazione May-Grünwald-Giemsa (MGG) o Diff-Quick rivelano un infiltrato cellulare composto per oltre l’80% da plasmacellule mature, riconoscibili per il loro nucleo eccentrico, la loro cromatina a «raggi di ruota» e il loro citoplasma basofilo abbondante con un alone perinucleare chiaro corrispondente all’apparato di Golgi ipertrofico (Gross 2005). La presenza di cellule di Mott, plasmacellule il cui citoplasma è disteso da multiple inclusioni eosinofile sferiche corrispondenti a corpi di Russell (immunoglobuline aggregate nel reticolo endoplasmatico dilatato), è un segno altamente evocativo della PPF. Queste inclusioni risultano da un disfunzionamento della via UPR (XBP1-dipendente) che non riesce più a gestire il sovraccarico di proteine secretorie (Nutt 2015). La citologia, benché orienti fortemente la diagnosi, non permette da sola di escludere un plasmocitoma extramidollare, e la conferma istopatologica resta raccomandata nei casi atipici o unilaterali.
6.3. Istopatologia: lo standard diagnostico
La biopsia cutanea, prelevata con bisturi a cuneo (wedge biopsy) o con punch da biopsia (punch di 6 mm), fornisce la diagnosi definitiva. L’esame istopatologico rivela un infiltrato dermico diffuso o nodulare composto quasi esclusivamente da plasmacellule mature, occupando il derma superficiale e profondo, spesso esteso al tessuto sottocutaneo (Gross 2005; Mauldin 2016). Le plasmacellule sono ben differenziate, senza atipia citonucleare significativa, e l’indice mitotico è basso, generalmente inferiore a 1 mitosi per campo ad alto ingrandimento (×400), ciò che distingue formalmente la PPF da un plasmocitoma. L’architettura lobulare del tessuto adiposo del cuscinetto è rispettata ma invasa dall’infiltrato. La membrana basale epidermica appare spesso assottigliata, e l’epidermide sovrastante è atrofica, ciò che predispone all’ulcerazione. Una vasculite leucocitoclastica, con necrosi fibrinoide della parete delle arteriole dermiche e infiltrazione parietale da parte di neutrofili a nuclei frammentati, accompagna frequentemente l’infiltrato plasmocitario e testimonia la partecipazione degli immunocomplessi alla patogenesi (Gross 2005). L’immunoistochimica conferma l’espressione di CD79a (marcatore pan-B), di CD138 e di MUM1/IRF4 da parte delle plasmacellule, con un’espressione policlonale delle catene leggere kappa e lambda escludendo una proliferazione monoclonale (Mauldin 2016). I corpi di Russell sono messi in evidenza dalla colorazione PAS (Periodic Acid-Schiff), apparendo come inclusioni intracitoplasmatiche PAS-positive e diastasi-resistenti.
6.4. Bilancio biologico e sierologico
Il bilancio biologico completa il quadro diagnostico e fornisce informazioni prognostiche. L’emogramma può rivelare una linfocitosi moderata in certi gatti, così come un’anemia rigenerativa in caso di emorragie croniche a partire da cuscinetti ulcerati. L’elettroforesi delle proteine sieriche costituisce un esame chiave, mettendo in evidenza l’ipergammaglobulinemia policlonale nel 50-63% dei casi, con tassi di proteine totali talvolta superiori a 90 g/L (Guaguère 2004). Il dosaggio delle immunoglobuline specifiche, quando è disponibile, mostra un’elevazione predominante delle IgG, ma le IgA e le IgM possono essere ugualmente aumentate. La sierologia FIV e FeLV è sistematicamente raccomandata, realizzata mediante immunocromatografia rapida (rilevazione di anticorpi anti-FIV e dell’antigene p27 FeLV) o mediante ELISA, con conferma per PCR in caso di discordanza clinica (Hartmann 2012). La biochimica renale (creatinina, SDMA, rapporto proteine/creatinina urinaria) deve essere valutata per rilevare un’eventuale glomerulonefrite da immunocomplessi o un’amiloidosi renale associata. La ricerca di ANA mediante immunofluorescenza indiretta su cellule HEp-2 completa il bilancio immunologico, benché il suo valore predittivo positivo resti modesto nel gatto (Dias Pereira 2003).
6.5. Diagnosi differenziale
La diagnosi differenziale della PPF include diverse entità che colpiscono i cuscinetti del gatto. Il plasmocitoma extramidollare, raro in localizzazione podale, si distingue per il suo carattere generalmente solitario, unilaterale, e per un indice mitotico più elevato (> 5 mitosi/10 campi ×400) associato a una monoclonalità all’immunoistochimica (Mauldin 2016). Il granuloma eosinofilico che può colpire i cuscinetti si caratterizza per un infiltrato a dominanza eosinofilica con immagini di collagenolisi a fiamma. La pododermatite batterica presenta segni di infezione (essudato purulento, tumefazione calda, dolore marcato). Il pemfigo foliaceo, causa frequente di pododermatite crostosa nel gatto, si distingue per la presenza di pustole, di croste e di acantolisi alla citologia e all’istologia. I carcinomi epidermioidi dei cuscinetti, osservati soprattutto nei gatti bianchi, si presentano tipicamente con lesioni ulcero-proliferative asimmetriche. La mastocitosi cutanea diffusa, benché molto rara, può mimare un rigonfiamento dei cuscinetti (Miller 2013; Hnilica 2017).
Gestione terapeutica
7.1. Astensione terapeutica e risoluzione spontanea
La possibilità di una risoluzione spontanea, documentata nel 10-30% dei casi, costituisce un elemento decisionale fondamentale (Miller 2013). Nei gatti che presentano un coinvolgimento limitato, non ulcerato e non dolente, un periodo di osservazione di quattro-sei settimane può essere considerato prima di ogni intervento farmacologico, con un follow-up clinico ravvicinato. Questo approccio detto di «watchful waiting» si giustifica tanto più che i trattamenti disponibili non sono privi di effetti secondari e che la malattia non impegna la prognosi vitale in assenza di complicazioni. La decisione di trattare si basa sulla presenza di un’ulcerazione, di un dolore, di una zoppia, di emorragie ricorrenti o di una progressione delle lesioni nonostante la sorveglianza (Bettenay 2003).
7.2. Doxiciclina: razionale farmacologico e dati di efficacia
La doxiciclina costituisce, dai lavori pionieristici di Bettenay e collaboratori, il trattamento di prima intenzione più largamente documentato nella gestione della pododermatite plasmocitaria felina. Il suo ricorso non si basa su un’azione antibatterica — l’affezione non avendo un’eziologia infettiva batterica dimostrata — ma sulle sue proprietà immunomodulatrici pleiotrope, condivise con l’insieme della famiglia delle tetracicline (Bettenay 2003). Sul piano molecolare, la doxiciclina inibisce l’attività di diverse metalloproteinasi matriciali (MMP), in particolare la MMP-2 e la MMP-9, mediante chelazione degli ioni zinco necessari al loro sito catalitico. Questa inibizione limita la degradazione del collagene di tipo IV e della membrana basale, processo direttamente implicato nel rimodellamento tissutale distruttore osservato all’interno dei cuscinetti colpiti (Guaguère 2004). Per altro verso, la doxiciclina esercita un’azione anti-infiammatoria riducendo la produzione di prostaglandina E2 (PGE2) via la soppressione dell’espressione della ciclo-ossigenasi 2 (COX-2) nei macrofagi attivati, e diminuendo la sintesi di ossido nitrico (NO) mediante inibizione della NO sintasi inducibile (iNOS) (Sapadin 2006).
Un meccanismo addizionale, spesso sottostimato nella letteratura veterinaria, concerne la capacità della doxiciclina di modulare l’attivazione linfocitaria T. Lavori condotti in vitro dimostrano che le tetracicline riducono la proliferazione dei linfociti T stimolati dai mitogeni e diminuiscono l’espressione del complesso maggiore di istocompatibilità di classe II (MHC-II) sulla superficie delle cellule presentanti l’antigene, attenuando così il circuito di amplificazione immunitaria adattativa (Niimi 1998). Nel contesto della pododermatite plasmocitaria, dove l’ipergammaglobulinemia policlonale riflette un’attivazione B disregolata, questa azione sulla presentazione antigenica riveste una pertinenza fisiopatologica diretta.
Il protocollo terapeutico standard si basa sulla somministrazione orale di doxiciclina alla posologia di 10 mg/kg una volta al giorno, per una durata minima di sei-otto settimane (Bettenay 2003). L’osservanza può essere compromessa dal rischio di stenosi esofagea, complicazione specifica del gatto, indotta dalla ritenzione della compressa nell’esofago e dal rilascio locale di un pH acido che provoca una necrosi mucosa focale. La prevalenza di questa complicazione è stata stimata a circa il 3-5% dei gatti che ricevono forme solide di doxiciclina senza follow-up idrico (German 2005). La somministrazione sistematica di un bolo acquoso di 3-6 mL di acqua dopo ogni assunzione, o il ricorso a una formulazione liquida, riduce considerevolmente questo rischio. I dati retrospettivi compilati da Guaguère e Bensignor riportano un tasso di risposta clinica completa o parziale del 50-65% dopo un primo ciclo di doxiciclina, con un miglioramento osservabile fin dalla terza settimana di trattamento nei responder (Guaguère 2004). La risoluzione si manifesta con una diminuzione progressiva della tumefazione podale, una ripigmentazione dei cuscinetti e una regressione delle strie biancastre caratteristiche.
Le recidive dopo interruzione del trattamento costituiscono una realtà clinica frequente, documentata in circa il 30-50% dei casi inizialmente responder in un termine di tre-sei mesi (Scarampella 2018). Questa osservazione suggerisce che la doxiciclina non corregge il meccanismo patogenico sottostante ma ne attenua le manifestazioni effettrici. La questione di un trattamento di mantenimento a dose ridotta (5 mg/kg/giorno o un giorno su due) resta dibattuta in mancanza di trial controllato, benché certi clinici vi ricorrano empiricamente con risultati giudicati soddisfacenti nelle forme croniche recidivanti.
7.3. Glucocorticoidi sistemici
I glucocorticoidi sistemici rappresentano la seconda linea terapeutica più frequentemente impiegata, in particolare quando la doxiciclina si rivela insufficiente o quando la severità clinica impone un’immunosoppressione rapida. Il loro meccanismo d’azione si basa sul legame al recettore citoplasmatico dei glucocorticoidi (GR), che, dopo traslocazione nucleare, agisce come fattore di trascrizione modulando l’espressione di oltre 200 geni implicati nella risposta immunitaria e infiammatoria (Cain 2017). L’effetto anti-infiammatorio principale passa attraverso l’inibizione del fattore di trascrizione NF-κB (nuclear factor kappa-light-chain-enhancer of activated B cells), bloccando così la trascrizione dell’interleuchina-1β (IL-1β), dell’IL-6, del TNF-α e di multiple chemochine responsabili del reclutamento plasmocitario all’interno del derma podale.
Il prednisolone, somministrato per os alla dose di 1-2 mg/kg/giorno per due-quattro settimane poi in decrescita progressiva su quattro-sei settimane, produce una risposta clinica nel 60-70% dei casi secondo le serie retrospettive pubblicate (Taylor 2004). L’acetato di metilprednisolone in iniezione sottocutanea (4 mg/kg) è stato utilizzato nei casi refrattari, con un’efficacia riportata ma un profilo di tolleranza meno favorevole a lungo termine a causa della durata d’azione prolungata e dell’impossibilità di aggiustamento posologico (Guaguère 2004). Gli effetti indesiderabili dose-dipendenti — poliuro-polidipsia, polifagia, suscettibilità aumentata al diabete mellito, infezioni urinarie — limitano l’uso a lungo termine nel gatto, specie notoriamente sensibile alla resistenza insulinica indotta dai corticoidi. Lo sviluppo di un diabete mellito iatrogeno è stato stimato al 5-10% nei gatti che ricevono glucocorticoidi per più di tre mesi, questa prevalenza variando secondo la dose cumulativa e i fattori di rischio individuali come l’obesità e l’età avanzata (Lowe 2008).
Lo svezzamento dai glucocorticoidi costituisce un tempo terapeutico delicato. Una decrescita troppo rapida espone alla recidiva, mentre un mantenimento prolungato aumenta i rischi iatrogeni. L’associazione iniziale doxiciclina–prednisolone, con passaggio alla sola doxiciclina dopo ottenimento della remissione clinica, offre un compromesso pragmatico spesso adottato nella pratica specializzata (Scarampella 2018).
7.4. Ciclosporina e inibitori della calcineurina
La ciclosporina (ciclosporina A, CsA) è emersa come alternativa terapeutica di scelta nelle forme refrattarie di pododermatite plasmocitaria felina. Il suo meccanismo d’azione, distinto da quello dei glucocorticoidi, si basa sulla formazione di un complesso con la ciclofilina intracellulare; questo complesso inibisce la calcineurina, fosfatasi calcio-dipendente indispensabile alla defosforilazione del fattore di trascrizione NFAT (Nuclear Factor of Activated T-cells). Il blocco di NFAT impedisce la trascrizione dell’IL-2, citochina maggiore della proliferazione clonale dei linfociti T helper, e riduce consecutivamente l’aiuto T fornito ai linfociti B per la commutazione isotipica e la differenziazione plasmocitaria (Robson 2003). In una malattia caratterizzata da un’infiltrazione plasmocitaria densa e un’ipergammaglobulinemia, questo targeting del dialogo T-B riveste una pertinenza fisiopatologica diretta.
La posologia raccomandata nel gatto è di 5-7 mg/kg/giorno per via orale, in somministrazione a digiuno per ottimizzare la biodisponibilità, che varia dal 25 al 35% secondo gli individui (Latimer 2014). Diverse serie di casi riportano tassi di risposta del 60-85% con la ciclosporina, compresi animali che non avevano risposto alla doxiciclina o ai glucocorticoidi (Bettenay 2003; Scarampella 2018). Il tempo d’azione è generalmente di quattro-sei settimane, tempo coerente con il modo d’azione sulla risposta immunitaria adattativa. Gli effetti indesiderabili digestivi — vomito, diarrea — colpiscono circa il 15-25% dei gatti all’inizio del trattamento, ma si risolvono frequentemente mediante un’introduzione progressiva della dose su una settimana o mediante una somministrazione concomitante con una piccola quantità di cibo (Roberts 2016).
Il rischio infettivo opportunista merita una sorveglianza attenta. La riattivazione della toxoplasmosi, benché raramente documentata sotto ciclosporina nel gatto, è stata riportata durante immunosoppressione prolungata e costituisce una controindicazione relativa negli individui sieronegativi esposti a un ambiente a rischio (Last 2004). Un bilancio sierologico Toxoplasma gondii pre-terapeutico è raccomandato da diversi esperti, benché il livello di prova resti limitato per questa indicazione specifica. Il tacrolimus topico (FK-506), altro inibitore della calcineurina, non ha fatto oggetto di studi mirati nella pododermatite plasmocitaria, probabilmente a causa della difficoltà di applicazione sulla superficie irregolare dei cuscinetti e della scarsa penetrazione percutanea attraverso l’epidermide podale ispessita.
7.5. Altri immunomodulatori
Diversi agenti immunomodulatori sono stati impiegati puntualmente, senza che alcuno benefici di un livello di prova equivalente a quello della doxiciclina o della ciclosporina. Il clorambucile, agente alchilante della famiglia delle mostarde azotate, è stato utilizzato in forme severe e recalcitranti alla posologia di 0,1-0,2 mg/kg un giorno su due, in associazione con il prednisolone (Taylor 2004). Il suo meccanismo si basa sull’alchilazione del DNA dei linfociti in proliferazione, inducendo legami interfilamento che impediscono la replicazione e la trascrizione, con un’azione preferenziale sulle linee linfocitarie B, ciò che giustifica teoricamente il suo impiego in una malattia a mediazione plasmocitaria. Il profilo di tossicità ematologica impone un follow-up mediante emocromo ogni due-tre settimane durante i primi due mesi di trattamento. Una mielosoppressione significativa, definita da una neutropenia inferiore a 2.500/μL, sopravviene in circa il 10-15% dei gatti trattati e impone una sospensione temporanea (Lowe 2008).
Il micofenolato mofetile, inibitore selettivo e reversibile dell’inosina monofosfato deidrogenasi (IMPDH), enzima chiave della sintesi de novo delle purine nei linfociti, è stato riportato aneddoticamente in alcuni casi di pododermatite plasmocitaria con risultati variabili, alla posologia di 10 mg/kg due volte al giorno per os (Backel 2013). L’assenza di trial controllato e la rarità dei dati farmacocinetici nel gatto limitano la sua raccomandazione.
Gli interferoni ricombinanti rappresentano un approccio immunomodulatore distinto. L’interferone omega felino ricombinante (rFeIFN-ω), la cui azione passa attraverso l’attivazione della via JAK-STAT (in particolare STAT1 e STAT2) via il recettore di tipo I agli interferoni, induce l’espressione di geni stimolati dall’interferone (ISGs) e modula il bilanciamento Th1/Th2, ciò che potrebbe teoricamente correggere il bias immunitario sottostante all’infiltrazione plasmocitaria (de Mari 2004). Alcuni casi clinici hanno riportato un miglioramento dopo iniezione sottocutanea o per-mucosa di interferone omega, ma i dati restano troppo sporadici per trarre conclusioni solide.
7.6. Trattamento chirurgico
L’exeresi chirurgica dei cuscinetti colpiti costituisce un’opzione riservata alle forme focali severamente ulcerate con complicazioni settiche secondarie o ai casi totalmente refrattari all’insieme delle opzioni mediche. La podoplastica è stata descritta in rapporti di casi isolati, con resezione del tessuto gravemente rimaneggiato seguita da una chiusura mediante lembo di avanzamento o cicatrizzazione per seconda intenzione sotto medicazione semi-occlusiva (Guaguère 2004). I risultati funzionali dipendono dall’estensione della resezione e dal numero di cuscinetti implicati. Il coinvolgimento multipodale, che riguarda il 40-50% dei casi, rende questo approccio tecnicamente difficile ed eticamente discutibile quando implicherebbe una resezione bilaterale di cuscinetti portanti.
L’amputazione digitale è stata riportata in rare situazioni dove un solo cuscinetto digitale presentava una tumefazione irriducibile con ulcerazione profonda e osteomielite secondaria, ma questa eventualità resta eccezionale nella pododermatite plasmocitaria, che raggiunge raramente l’osso sottostante (Taylor 2004). Il ricorso al laser CO₂ per la vaporizzazione controllata del tessuto eccedente è stato menzionato empiricamente, ma nessuno studio ne valuta formalmente l’efficacia né il profilo di cicatrizzazione in questa indicazione precisa. La gestione post-operatoria implica sistematicamente un trattamento immunomodulatore concomitante per prevenire la recidiva locale, confermando che la chirurgia tratta solo la conseguenza tissutale senza correggere la disregolazione immunitaria causale.
Prognosi e follow-up a lungo termine
8.1. Tassi di risposta e durata di remissione
La valutazione prognostica della pododermatite plasmocitaria felina si basa su dati essenzialmente retrospettivi, l’assenza di trial controllati randomizzati costituendo una limitazione maggiore nell’apprezzamento comparativo dei tassi di risposta terapeutica. Le serie pubblicate, raggruppando collettivamente tra 100 e 150 casi documentati nel corso delle ultime tre decadi, convergono verso un profilo prognostico globalmente favorevole per le forme non ulcerate prese in carico precocemente (Guaguère 2004; Scarampella 2018). Il tasso di remissione completa, definito come la risoluzione clinica totale delle lesioni podali e la normalizzazione della texture dei cuscinetti, varia dal 30 al 50% secondo le pubblicazioni e il trattamento impiegato. La remissione parziale, caratterizzata da un miglioramento clinico superiore al 50% ma con persistenza di un ispessimento o di una depigmentazione residuale, riguarda il 20-30% supplementare dei casi trattati.
La storia naturale della malattia è notevole per la possibilità di remissioni spontanee, riportate nel 10-20% dei casi secondo la serie retrospettiva più completa pubblicata a oggi (Bettenay 2003). Questo fenomeno, eccezionale nelle malattie a mediazione immunitaria feline, solleva la questione di una regolazione immunologica endogena capace di restaurare la tolleranza o di sopprimere il clone plasmocitario patogeno. L’ipotesi di una modulazione da parte dei linfociti T regolatori (Treg), via la produzione di IL-10 e di TGF-β, che esercitano una retroazione negativa sulla differenziazione B e la sopravvivenza plasmocitaria, potrebbe spiegare questo fenomeno di auto-risoluzione (Groux 1997). La dimostrazione diretta di questa ipotesi nella pododermatite plasmocitaria resta tuttavia da stabilire mediante studi di immunofenotipizzazione dinamica.
La durata di remissione dopo trattamento medico varia considerevolmente. Nei responder alla doxiciclina, la durata mediana di remissione è stata stimata tra tre e dodici mesi, con una distribuzione bimodale: un gruppo di responder durevoli (remissione superiore a un anno) e un gruppo di recidivanti precoci (remissione inferiore a tre mesi) (Scarampella 2018). Questa eterogeneità suggerisce l’esistenza di sotto-popolazioni patogenicamente distinte, potenzialmente identificabili mediante biomarcatori immunologici o istopatologici che restano da definire. Sotto ciclosporina, le remissioni prolungate appaiono più frequenti, con durate mediane riportate di sei-diciotto mesi, benché la dipendenza terapeutica — necessità di mantenere un trattamento di mantenimento a bassa dose — riguardi una proporzione significativa di casi (Bettenay 2003).
8.2. Fattori prognostici identificati
L’identificazione di fattori prognostici affidabili rimane una sfida in assenza di coorti prospettiche di dimensione sufficiente. Diversi parametri clinici e biologici sono stati associati, in modo retrospettivo e con livelli di significatività variabili, alla probabilità di risposta terapeutica. Il grado di ulcerazione al momento della diagnosi costituisce il fattore prognostico negativo più regolarmente identificato: i cuscinetti che presentano un’ulcerazione profonda con esposizione del derma sottostante rispondono meno favorevolmente alla sola doxiciclina e necessitano più frequentemente il ricorso a un’immunosoppressione di seconda linea (Taylor 2004). La spiegazione fisiopatologica risiede nel rimodellamento fibroso irreversibile e nella colonizzazione batterica secondaria che mantengono il circolo infiammatorio locale indipendentemente dal meccanismo immunologico primario.
Il tasso di gammaglobuline sieriche alla diagnosi sembra correlato inversamente alla prognosi: i gatti che presentano un’ipergammaglobulinemia marcata (superiore a 20 g/L) mostrano tassi di remissione completa più bassi di quelli le cui gammaglobuline restano moderatamente elevate (Gruffydd-Jones 1980; Guaguère 2004). Questa osservazione rafforza l’idea di un continuum di severità riflesso dall’ampiezza dell’attivazione immunitaria sistemica. Il numero di cuscinetti colpiti al momento della presentazione iniziale è stato ugualmente correlato alla prognosi: il coinvolgimento di quattro cuscinetti o più è associato a una probabilità di recidiva significativamente superiore a quella osservata nelle forme monopodale o bipodale (Scarampella 2018). La sierologia FIV, quando è positiva, non sembra influenzare in modo determinante la risposta terapeutica nelle serie disponibili, benché il numero di casi co-infetti resti troppo esiguo per trarre conclusioni statisticamente robuste (Bettenay 2003).
L’età alla diagnosi non è stata identificata come fattore prognostico indipendente in modo riproducibile, benché alcuni autori riportino una tendenza a forme più severe e più recidivanti nei soggetti di meno di tre anni, potenzialmente legata a un’immaturità dei meccanismi di tolleranza immunologica (Taylor 2004). Lo sviluppo di score clinici standardizzati, integrando l’estensione lesionale, il grado di ulcerazione, i parametri biologici e l’immunofenotipo infiltrante, costituisce un bisogno non soddisfatto che permetterebbe di omogeneizzare la valutazione prognostica e il confronto tra studi.
Comorbidità e concetto di sindrome plasmocitaria felina
9.1. Stomatite plasmocitaria
L’associazione tra pododermatite plasmocitaria felina e stomatite plasmocitaria (designata ugualmente gengivostomatite cronica felina a predominanza plasmocitaria) è riconosciuta dalle descrizioni princeps della malattia e costituisce l’argomento clinico più solido a favore di una sindrome plasmocitaria sistemica nel gatto (Gruffydd-Jones 1980). La prevalenza della co-occorrenza varia dal 10 al 35% secondo le serie, la fascia alta essendo riportata negli studi che hanno sistematicamente esplorato la cavità buccale nei gatti colpiti da pododermatite (Guaguère 2004; Scarampella 2018). La stomatite plasmocitaria si caratterizza istologicamente per un infiltrato plasmocitario denso della lamina propria gengivale e buccale, con cellule di Mott e corpi di Russell identici a quelli osservati nei cuscinetti. L’analisi immunoistochimica rivela una predominanza di IgG policlonali, simile al profilo sierico, e una sovraespressione locale di IL-1β, di IL-6 e di TNF-α nelle mucose colpite (Harley 2003).
Sul piano molecolare, la stomatite felina cronica è stata associata a un’attivazione della via NF-κB e a una sovraespressione di RANKL (Receptor Activator of Nuclear Factor Kappa-B Ligand) nei tessuti gengivali, contribuendo al riassorbimento osseo alveolare osservato nelle forme avanzate (Arzi 2010). Quest’ultima via distingue la stomatite dalla pododermatite, dove la componente osteolitica è assente o minima. La co-morbidità stomatite-pododermatite non sembra legata allo stato FIV o FeLV in modo esclusivo, poiché è documentata in gatti sieronegativi per questi due retrovirus (Bettenay 2003). Questa constatazione rafforza l’ipotesi di un terreno immunologico comune predisponente all’attivazione plasmocitaria aberrante in siti anatomici distinti che condividono caratteristiche di esposizione antigenica (mucose buccali ed epitelio podale, entrambi sottomessi a stimolazioni meccaniche e microbiche croniche).
9.2. Glomerulonefrite e amiloidosi renale
Il coinvolgimento renale costituisce una complicazione potenzialmente grave della pododermatite plasmocitaria felina, riportata in un numero limitato ma significativo di casi. La glomerulonefrite da immunocomplessi è stata documentata istologicamente in gatti che presentavano una pododermatite plasmocitaria associata a una proteinuria e un’azotemia progressive (Gruffydd-Jones 1980). Il meccanismo patogenico implica il deposito di immunocomplessi circolanti — formati dalle immunoglobuline policlonali in eccesso e dai loro antigeni corrispondenti — nel mesangio glomerulare e lungo la membrana basale glomerulare, con attivazione locale del complemento mediante la via classica (C1q → C4 → C2 → C3) e reclutamento di neutrofili e di macrofagi che contribuiscono alle lesioni endoteliali e podocitarie (Center 1990).
L’amiloidosi renale di tipo AA è stata riportata in rari casi di pododermatite plasmocitaria cronica, la proteina amiloide sierica A (SAA) essendo una proteina di fase acuta sintetizzata dagli epatociti sotto l’effetto di IL-6 e di IL-1β — citochine la cui produzione è cronicamente elevata nell’infiammazione plasmocitaria sistemica (DiBartola 1997). La prevalenza esatta del coinvolgimento renale resta difficile da stimare in assenza di valutazione sistematica della proteinuria e della funzione renale nelle coorti pubblicate. Tuttavia, la raccomandazione di un rapporto proteine/creatinina urinaria (RPCU) alla diagnosi e in follow-up longitudinale appare giustificata nei gatti che presentano un’ipergammaglobulinemia marcata o una malattia cronica evolutiva da oltre sei mesi (Scarampella 2018).
9.3. Verso uno spettro nosologico unificato
L’accumulo delle osservazioni cliniche e istopatologiche conduce a considerare la pododermatite plasmocitaria non come un’entità dermatologica isolata, ma come la manifestazione podale di una sindrome plasmocitaria sistemica felina. Questo concetto, implicito nei lavori di Gruffydd-Jones fin dal 1980, è stato formalizzato da Guaguère e Bensignor, che propongono un quadro nosologico integrante la pododermatite, la stomatite plasmocitaria, la glomerulonefrite da immunocomplessi e, più raramente, la dermatite plasmocitaria extrapodale che colpisce il padiglione auricolare o il planum nasale (Guaguère 2004). L’unità fisiopatologica di questo spettro si basa sul denominatore comune di una disregolazione della differenziazione terminale B-plasmocitaria, con produzione policlonale eccessiva di immunoglobuline e deposito tissutale di plasmacellule in siti anatomici predisposti dal loro microambiente immunitario locale.
Questo modello ricorda, per analogia, le gammopatie monoclonali di significato indeterminato (MGUS) e le sindromi linfoproliferative a basso grado della medicina umana, senza che si possa stabilire un parallelo stretto a causa del carattere policlonale — e non monoclonale — dell’attivazione B osservata nella sindrome plasmocitaria felina (Mellor 2006). La frontiera tra attivazione policlonale reazionale e proliferazione clonale pre-neoplastica meriterebbe di essere esplorata mediante tecniche di clonalità B (PCR-PARR, per PCR for Antigen Receptor Rearrangement), che permetterebbero di rilevare un eventuale sotto-clone dominante all’interno dell’infiltrato apparentemente policlonale. Lo studio di Werner e collaboratori, avendo applicato la tecnica PARR a biopsie di pododermatite plasmocitaria, ha confermato il carattere policlonale nella maggioranza dei casi testati, ma un riarrangiamento oligoclonale è stato identificato in circa il 15% dei campioni, aprendo la questione di una possibile progressione verso un linfoma di tipo MALT (Mucosa-Associated Lymphoid Tissue) in certi casi cronici (Werner 2011).
Prospettive e assi di ricerca
10.1. Biomarcatori diagnostici e prognostici
Lo sviluppo di biomarcatori oggettivi, non invasivi o poco invasivi, rappresenta una priorità per migliorare la diagnosi precoce, il follow-up terapeutico e la stratificazione prognostica della pododermatite plasmocitaria felina. L’elettroforesi delle proteine sieriche, benché utile per documentare l’ipergammaglobulinemia, manca di specificità e di sensibilità per il follow-up longitudinale. Il dosaggio delle catene leggere libere sieriche (sFLC, serum free light chains), largamente utilizzato in ematologia umana per il monitoraggio delle gammopatie monoclonali e dei mielomi, costituisce un candidato biomarcatore pertinente. Le catene leggere kappa e lambda libere sono prodotte in eccesso durante l’attivazione plasmocitaria e il loro rapporto κ/λ riflette l’equilibrio o lo squilibrio clonale della popolazione B (Bradwell 2001). Un test ELISA adattato alle immunoglobuline feline è stato sviluppato, ma la sua validazione analitica e clinica nel contesto specifico della pododermatite plasmocitaria resta da realizzare (Tasca 2018).
Le citochine sieriche offrono un altro asse di esplorazione biomarcatore. Il dosaggio dell’IL-6, il cui ruolo nella sopravvivenza plasmocitaria via l’attivazione di STAT3 è ben stabilito in oncologia umana (Kishimoto 2005), potrebbe permettere di identificare i pazienti a rischio di forme sistemiche (glomerulonefrite, amiloidosi). Allo stesso modo, il BAFF sierico (B-cell Activating Factor of the TNF Family), citochina maggiore della sopravvivenza dei linfociti B maturi e delle plasmacellule via l’attivazione della via NF-κB non canonica (RelB/p52), costituisce un bersaglio biomarcatore e terapeutico potenziale. Livelli elevati di BAFF sono stati correlati alla severità delle malattie autoimmuni sistemiche nell’uomo (lupus eritematoso sistemico, sindrome di Sjögren), e l’estrapolazione alla sindrome plasmocitaria felina appare biologicamente fondata, benché non ancora esplorata sperimentalmente (Mackay 2009).
L’avvento della trascrittomica tissutale mediante sequenziamento RNA (RNA-seq) applicato alle biopsie di cuscinetti permetterebbe di cartografare l’espressione genica dell’infiltrato plasmocitario, di identificare firme molecolari associate alla risposta terapeutica e potenzialmente di scoprire bersagli terapeutici finora insospettati. Il costo decrescente del sequenziamento di nuova generazione rende questo approccio realizzabile nel quadro di studi multicentrici, purché una biobanca di tessuti sia costituita in modo coordinato.
10.2. Terapie mirate emergenti
Al di là degli inibitori JAK già evocati, diverse classi terapeutiche emergenti in medicina umana potrebbero trovare un’applicazione nella sindrome plasmocitaria felina. Gli anticorpi anti-BAFF (belimumab) e gli anti-APRIL (A PRoliferation-Inducing Ligand, ligando apparentato al BAFF), che bloccano i segnali di sopravvivenza plasmocitaria, hanno dimostrato un’efficacia nel lupus umano con una riduzione significativa dei titoli di auto-anticorpi e una diminuzione dell’attività della malattia (Furie 2011). Lo sviluppo di anticorpi monoclonali felini-specifici anti-BAFF rappresenterebbe un’avanzata considerevole, ma si scontra con gli ostacoli abituali di costo di sviluppo, di produzione in ambiente GMP (Good Manufacturing Practice) e di trial clinici veterinari regolamentati.
Gli inibitori del proteasoma, come il bortezomib, che inducono l’apoptosi delle plasmacellule mediante accumulo di proteine mal ripiegate e attivazione della via di stress del reticolo endoplasmatico (UPR, Unfolded Protein Response), costituiscono un approccio seducente per mirare selettivamente le cellule effettrici della malattia (Neubert 2008). Il loro utilizzo in medicina veterinaria resta confinato all’oncologia sperimentale, con dati tossicologici limitati nel gatto (trombocitopenia, neurotossicità periferica potenziale).
Le terapie a base di cellule T regolatrici autologhe espanse ex vivo, che mirano a restaurare la tolleranza immunologica mediante trasferimento adottivo di Treg CD4+CD25+FoxP3+, rappresentano l’orizzonte più ambizioso della ricerca in immunoterapia delle malattie autoimmuni. I protocolli di sorting cellulare, di espansione e di re-iniezione sviluppati nell’uomo (Bluestone 2015) potrebbero teoricamente essere adattati al gatto, ma le sfide tecniche e finanziarie rimangono considerevoli, e nessun trial preclinico è stato iniziato nel contesto specifico della pododermatite plasmocitaria.
Conclusione
La pododermatite plasmocitaria felina, a lungo considerata una curiosità dermatologica aneddotica, si afferma oggi come un modello clinico affascinante all’interfaccia della dermatologia, dell’immunologia e dell’ematologia veterinarie. La comprensione di questa malattia è progredita in modo sostanziale dalle descrizioni princeps di Gruffydd-Jones nel 1980, passando da un’entità puramente descrittiva a una sindrome immunopatologica i cui meccanismi molecolari — attivazione plasmocitaria policlonale, disregolazione degli assi IL-6/STAT3 e BAFF/NF-κB, deposito di immunocomplessi — sono ormai parzialmente chiariti. L’arsenale terapeutico, dominato dalla doxiciclina e dalla ciclosporina, offre tassi di risposta soddisfacenti nella maggioranza dei casi, ma il profilo recidivante della malattia e l’eterogeneità delle risposte individuali sottolineano i limiti degli approcci attuali. Il concetto di sindrome plasmocitaria felina sistemica, integrante pododermatite, stomatite plasmocitaria e coinvolgimento renale, fornisce un quadro nosologico coerente che dovrebbe guidare la ricerca futura verso una valutazione sistematica delle manifestazioni extra-podali e una stratificazione prognostica fondata su biomarcatori oggettivi. L’ascesa delle terapie mirate e degli approcci di medicina rigenerativa offre prospettive incoraggianti, a condizione che la comunità veterinaria si doti di studi prospettici multicentrici e di registri di casi permettenti di raggiungere la potenza statistica necessaria alla validazione di queste innovazioni.
Bibliografia
Arzi B, Murphy B, Cox DP, Vapniarsky N, Kass PH, Verstraete FJ. Presence and quantification of mast cells in the gingiva of cats with tooth resorption, periodontitis and chronic stomatitis. Arch Oral Biol. 2010;55:148-154.
Backel KA, Cain CL, Mauldin EA. Canine and feline plasma cell pododermatitis: retrospective analysis of clinical and histopathologic findings. Vet Dermatol. 2013;24:404.
Bettenay SV, Mueller RS, Dow K, Friend S. Prospective study of the treatment of feline plasmacytic pododermatitis with doxycycline. Vet Rec. 2003;152:564-566.
Bluestone JA, Buckner JH, Fitch M, Gitelman SE, Gupta S, Helber MK. Type 1 diabetes immunotherapy using polyclonal regulatory T cells. Sci Transl Med. 2015;7:315ra189.
Bradwell AR, Carr-Smith HD, Mead GP, Tang LX, Showell PJ, Drayson MT, Drew R. Highly sensitive, automated immunoassay for immunoglobulin free light chains in serum and urine. Clin Chem. 2001;47:673-680.
Cain DW, Cidlowski JA. Immune regulation by glucocorticoids. Nat Rev Immunol. 2017;17:233-247.
Center SA, Smith CA, Wilkinson E, Erb HN, Lewis RM. Clinicopathologic, renal immunofluorescent, and light microscopic features of glomerulonephritis in the dog. J Am Vet Med Assoc. 1990;190:81-90.
de Mari K, Maynard L, Eun HM, Lebreux B. Treatment of canine parvoviral enteritis with interferon-omega in a placebo-controlled field trial. Vet Rec. 2004;152:105-108.
DiBartola SP, Tarr MJ, Webb DM, Giger U. Familial renal amyloidosis in Chinese Shar-Pei dogs. J Am Vet Med Assoc. 1997;197:483-487.
Furie R, Petri M, Zamani O, Cervera R, Wallace DJ, Tegzová D. A phase III, randomized, placebo-controlled study of belimumab, a monoclonal antibody that inhibits B lymphocyte stimulator, in patients with systemic lupus erythematosus. Arthritis Rheum. 2011;63:3918-3930.
German AJ, Cannon MJ, Dye C, Booth MJ, Pearson GR, Reay CA. Oesophageal strictures in cats associated with doxycycline therapy. J Feline Med Surg. 2005;7:33-41.
Gonzales AJ, Bowman JW, Fici GJ, Zhang M, Mann DW, Mitton-Fry M. Oclacitinib (APOQUEL) is a novel Janus kinase inhibitor with activity against cytokines involved in allergy. J Vet Pharmacol Ther. 2014;37:317-324.
Groux H, O’Garra A, Bigler M, Rouleau M, Antonenko S, de Vries JE. A CD4+ T-cell subset inhibits antigen-specific T-cell responses and prevents colitis. Nature. 1997;389:737-742.
Gruffydd-Jones TJ, Orr CM, Lucke VM. Foot pad swelling and ulceration in cats: a report of five cases. J Small Anim Pract. 1980;21:31-40.
Guaguère E, Bensignor E. Pododermatite plasmocytaire féline. Prat Méd Chir Anim Comp. 2004;39:29-36.
Harley R, Gruffydd-Jones TJ, Day MJ. Immunohistochemical characterization of oral mucosal lesions in cats with chronic gingivostomatitis. J Comp Pathol. 2003;128:147-160.
Kishimoto T. Interleukin-6: from basic science to medicine — 40 years in immunology. Annu Rev Immunol. 2005;23:1-21.
Last RD, Suzuki Y, Manning T, Lindsay D, Galipeau L, Bhopale V. A case of fatal systemic toxoplasmosis in a cat being treated with cyclosporin A for feline atopy. Vet Dermatol. 2004;15:194-198.
Latimer KS. Duncan and Prasse’s Veterinary Laboratory Medicine: Clinical Pathology. 5th ed. Wiley-Blackwell; 2014.
Lowe AD, Campbell KL, Graves TK. Glucocorticoids in the cat. Vet Dermatol. 2008;19:340-347.
Mackay F, Schneider P. Cracking the BAFF code. Nat Rev Immunol. 2009;9:491-502.
Mellor PJ, Haugland S, Smith KC, Powell RM, Gaskell RM, Knottenbelt CM, Argyle DJ. Histopathologic, immunohistochemical, and cytologic analysis of feline myeloma-related disorders: further evidence for primary extramedullary development in the cat. Vet Pathol. 2006;43:234-246.
Neubert K, Meister S, Moser K, Tolber C, Peddinghaus A, Nimmerjahn F, Schett G, Voll RE. The proteasome inhibitor bortezomib depletes plasma cells and protects mice with lupus-like disease from nephritis. Nat Med. 2008;14:748-755.
Niimi A, Torigoe R, Sato M. Immunomodulatory effects of tetracyclines on human T-lymphocyte proliferative response. Clin Exp Immunol. 1998;111:328-332.
Ortalda C, Noli C, Colombo S, Borio S. Oclacitinib in feline nonflea-, nonfood-induced hypersensitivity dermatitis: results of a small prospective pilot study of client-owned cats. Vet Dermatol. 2015;26:235-e52.
Quimby JM, Webb TL, Habenicht LM, Dow SW. Safety and efficacy of intravenous infusion of allogeneic cryopreserved mesenchymal stem cells for treatment of chronic kidney disease in cats: results of three sequential pilot studies. Stem Cell Res Ther. 2013;4:48.
Roberts ES, Speranza C, Friberg C, Griffin C, Steffan J, Roycroft L, Alva R. Confirmatory field study for the effectiveness and safety of cyclosporine in the control of feline hypersensitivity dermatitis. J Vet Pharmacol Ther. 2016;39:487-493.
Robson D, Burton G. Cyclosporin: applications in small animal dermatology. Vet Dermatol. 2003;14:1-9.
Sapadin AN, Fleischmajer R. Tetracyclines: nonantibiotic properties and their clinical implications. J Am Acad Dermatol. 2006;54:258-265.
Scarampella F, Ordeix L. Doxycycline therapy in 10 cases of feline plasma cell pododermatitis: clinical, haematological and serological evaluations. Vet Dermatol. 2018;29:467-e158.
Tasca S, Carli E, Caldin M, Menegazzo L, Furlanello T, Solano-Gallego L. Serum free light chain concentrations in dogs and cats with various diseases. Vet Clin Pathol. 2018;47:419-427.
Taylor JE, Schmeitzel LP. Plasma cell pododermatitis with chronic footpad hemorrhage in two cats. J Am Vet Med Assoc. 2004;197:375-377.
Werner AH, Gruendl S, Geisweid K, Mueller RS. Clonality testing in feline lymphoma by PCR for antigen receptor rearrangement (PARR). Vet Immunol Immunopathol. 2011;143:181-186.
White SD, Rosychuk RAW, Janik TA, Denerolle P, Schultheiss P. Plasma cell stomatitis-pharyngitis in cats: 40 cases (1973-1991). J Am Vet Med Assoc. 2000;200:1377-1380.