Le recenti Giornate annuali del GEDAC, che si sono svolte ad Ajaccio, hanno offerto al nostro collega Vincent Bruet l’opportunità di fare il punto sulle fistole perianali, la loro patogenesi, le manifestazioni cliniche e gli attuali approcci terapeutici.
Le fistole perianali nei cani rappresentano una condizione dermatologica potenzialmente debilitante che, in assenza di un trattamento appropriato e tempestivo, può portare a modifiche irreversibili del retto e dell’ano, a volte culminando nell’eutanasia. Questa patologia, nota anche come foruncolosi anale, colpisce principalmente i cani di razza Pastore Tedesco ma può interessare altre razze e si manifesta con tratti fistolosi o ulcerazioni intorno all’ano.
A lungo considerata legata a fattori anatomici, la patogenesi delle fistole perianali è oggi riconosciuta come prevalentemente immuno-mediata. Anche la gestione terapeutica si è evoluta, passando da un approccio essenzialmente chirurgico a una strategia prevalentemente medica. Questo articolo propone una sintesi delle attuali conoscenze su questa affezione e presenta le raccomandazioni terapeutiche basate su un’analisi metodica della letteratura scientifica.
Patogenesi e aspetti clinici delle fistole perianali canine
Un’eziologia complessa e multifattoriale
La patogenesi esatta delle fistole perianali rimane parzialmente sconosciuta, nonostante numerosi studi. Storicamente, diverse ipotesi sono state avanzate per spiegare l’insorgenza di questa condizione. L’elevata incidenza nei Pastori Tedeschi inizialmente ha fatto sospettare un legame genetico, ma ad oggi non è stato identificato alcun marcatore genetico specifico. Allo stesso modo, la coda bassa è stata considerata un fattore predisponente, una teoria oggi confutata poiché altre razze sono colpite e l’amputazione della coda non è efficace come trattamento.
Le ricerche recenti indirizzano verso una patogenesi immuno-mediata. Sono state evidenziate modificazioni della risposta infiammatoria locale, con in particolare un’infiltrazione da parte di linfociti T CD31+ e un aumento dell’espressione di citochine associate ai linfociti T helper di tipo 1 nella cute lesionale. Questi meccanismi implicano probabilmente:
- Un’infiammazione locale mediata dai linfociti T
- Un’attivazione anomala dei macrofagi, con sovraespressione delle metalloproteinasi di matrice MMP-9 e MMP-13
- Una risposta immunitaria disfunzionale ai microbi della regione perianale
- Possibili anomalie di cicatrizzazione a livello perianale
- Una potenziale reazione di ipersensibilità alimentare, sebbene questa ipotesi debba ancora essere confermata
Uno studio genetico ha evidenziato un’associazione tra l’allele di classe II del CMH DLA-DRB1*00101 e un aumentato rischio di sviluppare fistole perianali nei Pastori Tedeschi. Le molecole di classe II del complesso maggiore di istocompatibilità partecipano alla presentazione di antigeni e all’attivazione dei linfociti T, il che rafforza l’ipotesi di una patogenesi immuno-mediata. Un altro studio ha rivelato una potenziale associazione con le regioni geniche ADAMTS16 e CTNND2, quest’ultima essendo anche associata alla malattia di Crohn e alla colite ulcerosa nell’uomo.
Presentazione clinica e segnalamento
Predisposizione razziale ed età di comparsa
Le fistole perianali colpiscono principalmente i cani di razza Pastore Tedesco, che rappresenterebbero oltre l’80% della popolazione colpita secondo alcuni studi. Tuttavia, diverse altre razze possono essere interessate, tra cui:
- Beagles
- Border Collies
- Pastori Australiani
- Setter Irlandesi
- Retrievers della Baia di Chesapeake
- Leonberger
- Staffordshire Bull Terriers
- Shih Tzu
- Welsh Corgis Pembroke
- Boxer
- Labrador Retrievers
- Cani meticci
L’età di comparsa si situa generalmente tra il giovane adulto e l’età media, con un intervallo da 2 a 9 anni per la maggior parte dei pazienti. Non è stata chiaramente stabilita alcuna predisposizione legata al sesso o allo stato di sterilizzazione, sebbene uno studio abbia suggerito un rischio maggiore nei Pastori Tedeschi maschi interi rispetto ai maschi castrati.
Aspetti lesionali e manifestazioni cliniche
Le lesioni caratteristiche delle fistole perianali comprendono:
- Seno o tratti fistolosi intorno all’ano
- Ulcerazioni perianali
- Erosioni
- Pustole nei casi meno gravi
- Fistole rettali più raramente
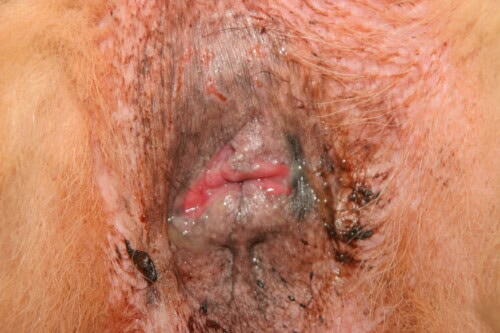
Lesioni di fistole perianali moderate
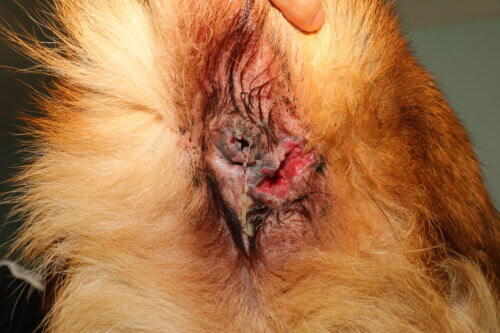
Gravi lesioni che occupano essenzialmente il quadrante inferiore destro
È importante notare che, a differenza di quanto suggerisce il termine “fistola perianale”, i tratti sinusali cutanei non comunicano generalmente con il lume rettale, a differenza delle fistole osservate nella malattia di Crohn nell’uomo. Queste lesioni possono essere singole o multiple, e la loro gravità varia da lieve a grave, con un dolore associato spesso significativo.
I segni clinici riportati dai proprietari includono:
- Tenesmo (sforzi di defecazione)
- Ematochezia (presenza di sangue nelle feci)
- Dischezia (dolore durante la defecazione)
- Emissione di piccoli volumi di feci frequenti
- Leccamento perianale eccessivo
- Secrezione purulenta
- Stitichezza
- Coprografia
- Anoressia
- Diarrea
- Incontinenza fecale
- Perdita di peso
- Letargia
Queste manifestazioni cliniche possono essere fortemente invalidanti e avere un impatto significativo sulla qualità di vita dell’animale. È stata dimostrata un’associazione tra fistole perianali e colite, e alcuni cani affetti presentano anche feci molli o mucoidi, diarrea e un aumento della frequenza delle defecazioni.
Approccio diagnostico
Esame clinico e diagnosi differenziale
La diagnosi delle fistole perianali si basa principalmente sulla presentazione clinica e sull’esame fisico, in particolare nei Pastori Tedeschi. Un esame approfondito della regione perianale e una rettoscopia sono essenziali per valutare l’estensione delle lesioni e identificare eventuali anomalie associate. A causa del dolore e del disagio causati da questa affezione, può essere necessaria una sedazione per eseguire un esame rettale completo.
L’esplorazione dei tragitti fistolosi con l’ausilio di un applicatore con punta cotonata o di uno strumento simile permette di determinarne la profondità. Il monitoraggio clinico può essere effettuato misurando le profondità di questi tragitti. A seconda della gravità e della durata della malattia, l’esame rettale può rivelare un’assenza di anomalie interne o una fibrosi grave, identificabile da un ispessimento della regione perianale con possibile stenosi anale.
Per tutti i pazienti, una palpazione approfondita e l’espressione delle sacche anali devono essere eseguite al fine di escludere un ascesso della ghiandola anale e di determinare se le fistole perianali comunicano con le sacche anali. Inoltre, i tragitti fistolosi possono essere irrigati con un catetere e soluzione fisiologica sterile per determinare se comunicano tra loro o se vi è un coinvolgimento delle sacche anali.
La diagnosi differenziale varia considerevolmente a seconda dei segni clinici presenti:
- In caso di prurito perianale: dermatite allergica (dermatite atopica e reazione alimentare avversa), ascesso delle sacche anali
- In caso di tenesmo ed ematochezia senza tragitti fistolosi visibili: affezioni gastrointestinali (malattia infiammatoria intestinale, parassiti intestinali, stenosi rettali)
- Neoplasia perianale ulcerata (adenoma o adenocarcinoma perianale)
- Lupus eritematoso cutaneo (LECM)
È importante notare che i Pastori Tedeschi sono anche predisposti al LECM, che può presentare lesioni anali o perianali. Le fistole perianali si distinguono generalmente dal LECM per i tratti sinusali o le ulcere crateriformi ben delimitate, mentre il LECM è associato a erosioni, ulcere, eritemi e croste più confluenti.
Se la differenziazione clinica tra fistole perianali e LECM è difficile, le biopsie cutanee per l’esame istopatologico possono essere utili. Similmente, se il cane appartiene a una razza meno comunemente colpita, altre cause basate sui segni clinici devono essere escluse per prime.
Valutazione istopatologica
Sebbene l’istopatologia sia raramente eseguita per la diagnosi delle fistole perianali canine, può essere considerata in casi di presentazione clinica insolita o in una razza meno classicamente colpita. Le caratteristiche istopatologiche includono:
- Infiammazione periaddessale con o senza foruncolosi
- Idradenite pronunciata
- Fibrosi periaddessale
- Ulcerazione
- La formazione di tratti sinusali rivestiti di epitelio nel derma
Gli infiltrati infiammatori, composti da neutrofili, linfociti, plasmacellule e macrofagi, possono essere osservati nei tratti sinusali. Le lesioni più profonde possono anche essere associate a celluliti piogranulomatose e a follicoli linfoidi.
Le biopsie coliche di cani affetti da fistole perianali possono mostrare segni istopatologici di colite; uno studio ha rilevato modificazioni istopatologiche compatibili con una diagnosi di colite in 9 cani su 18 affetti da fistole perianali.
Approcci terapeutici delle fistole perianali
Gestione chirurgica: un ruolo limitato
Evoluzione delle pratiche chirurgiche
La gestione delle fistole perianali si è evoluta considerevolmente nel tempo. Dagli anni ’40 agli anni ’70, queste lesioni erano considerate una patologia esclusivamente chirurgica. Gli interventi includevano generalmente la resezione di tutti i tessuti colpiti, con o senza asportazione delle sacche anali. Questa procedura poteva comportare una resezione focale o estendersi fino a una resezione circonferenziale completa (360 gradi) con anoplastica.
Diverse tecniche chirurgiche sono state descritte:
- Escissione a blocchi seguita da ricostruzione chirurgica
- Escissione laser (in particolare laser ND:YAG)
- Crioterapia per distruggere il tessuto malato
- Amputazione della base della coda (quando le fistole erano considerate associate alla postura della coda bassa)
Tipicamente, i pazienti ricevevano un emolliente fecale dopo l’operazione per diminuire la pressione durante i movimenti intestinali e consentire la cicatrizzazione della zona.
Limiti e complicazioni dell’approccio chirurgico
L’uso della chirurgia come terapia esclusiva presenta diversi problemi maggiori:
- Elevato tasso di recidive (riportato in più del 50% dei cani in uno studio)
- Assenza di risoluzione completa in molti casi
- Complicazioni chirurgiche significative:
- Deiscenza delle ferite
- Flatulenza
- Incontinenza fecale
- Diarrea
- Tenesmo
- Stitichezza
- Stenosi rettali
I risultati degli studi variano, ma la chirurgia è stata segnalata come inefficace nel 6% al 21% dei cani, alcuni dei quali sono stati abbandonati o euthanasiati di conseguenza.
Approccio chirurgico complementare
Più recentemente, diversi studi hanno descritto l’uso della chirurgia dopo che l’efficacia delle terapie immunosoppressive aveva raggiunto un plateau. Questo approccio combinato, in cui il trattamento medico precede l’intervento chirurgico, sembra dare risultati migliori rispetto alla sola chirurgia.
In questa strategia, il trattamento chirurgico interviene:
- Quando il miglioramento medico ha raggiunto un plateau
- Per gestire le lesioni persistenti dopo un miglioramento ottenuto con il trattamento medico
- Negli animali che presentano ancora disagio o dolore (qualità di vita alterata)
- Per ragioni economiche, quando il trattamento medico a lungo termine è troppo costoso
Le procedure chirurgiche eseguite in questo contesto comprendono:
- L’escissione delle fistole persistenti
- La sacculectomia
- La criptactomia
- La sutura di eventuali fistole rettali
Terapie immunomodulatrici: pietra angolare del trattamento
Inibitori della calcineurina
Ciclosporina A
La ciclosporina A è considerata uno dei trattamenti di riferimento per le fistole perianali canine. Il suo meccanismo d’azione implica il legame alla proteina intracellulare ciclofilina-1, inibendo la calcineurina. Questa inibizione impedisce la defosforilazione del fattore nucleare dei linfociti T attivati e la successiva produzione di citochine pro-infiammatorie, in particolare l’IL-2. La riduzione della produzione di IL-2 porta a una diminuzione della crescita e dell’attivazione dei linfociti T.
Diversi studi, inclusi studi clinici randomizzati e controllati, hanno dimostrato l’efficacia della ciclosporina A. In uno studio clinico randomizzato che confrontava la ciclosporina A con un placebo in pastori tedeschi affetti da fistole perianali, una risoluzione completa delle lesioni è stata riportata in 17 dei 20 cani (85%) che ricevevano ciclosporina A dopo 16 settimane di trattamento. La superficie totale media e la profondità delle lesioni sono diminuite rispettivamente del 78% e del 62% dopo 4 settimane di terapia.
Le dosi di ciclosporina A studiate per il trattamento delle fistole perianali variano considerevolmente, da 1,5 mg/kg ogni 24 ore a 10 mg/kg ogni 12 ore. In generale, le dosi più elevate sono associate a migliori risultati, con l’efficacia dose-dipendente. Le formulazioni modificate o microemulsionate di ciclosporina A hanno una biodisponibilità superiore nei cani e dovrebbero essere preferibilmente utilizzate. La biodisponibilità della ciclosporina A è anche ridotta dalla presenza di cibo; è quindi meglio somministrarla a stomaco vuoto (2 ore prima o dopo un pasto).
Il costo della ciclosporina A, in particolare a dosi elevate o per cani di taglia grande, può essere proibitivo. La somministrazione concomitante di ciclosporina A e ketoconazolo può inibire il metabolismo della ciclosporina A da parte dei microenzimi epatici del citocromo P450 e migliorarne la biodisponibilità tramite l’inibizione della P-glicoproteina intestinale (riducendo così il trasporto della ciclosporina A verso il lume intestinale). La co-somministrazione dei due farmaci può migliorare la biodisponibilità della ciclosporina A del 75% o più, a seconda della dose di ketoconazolo, e consentire una riduzione della dose di ciclosporina A.
L’associazione di ciclosporina A (a dosi da 1 mg/kg/die a 5,5 mg/kg/die) e ketoconazolo (a dosi da 5,1 mg/kg/die a 11 mg/kg/die) si è dimostrata efficace in studi clinici con una risoluzione completa delle lesioni nel 93% dei cani in 16 settimane, nel 100% dei cani in 3-10 settimane e nel 67% dei cani con un tempo medio di risoluzione di 13,9 settimane.
Le recidive possono verificarsi quando il trattamento immunomodulatore viene interrotto. Per questo motivo, dopo la risoluzione completa delle lesioni (che richiede generalmente 8-12 settimane di trattamento), si raccomanda di ridurre gradualmente le dosi di ciclosporina A e di ketoconazolo fino alla posologia e alla frequenza di somministrazione efficaci più basse.
Tacrolimus
Il tacrolimus in pomata allo 0,1% si è anche dimostrato efficace nel trattamento delle fistole perianali canine, sebbene non siano stati condotti studi clinici randomizzati e controllati. In uno studio su 10 cani trattati con una pomata di tacrolimus allo 0,1% applicata sulla cute perianale due volte al giorno per 16 settimane, 5 cani hanno ottenuto una risoluzione completa delle lesioni.
Il tacrolimus è più adatto per l’applicazione topica rispetto alla ciclosporina A a causa del suo peso molecolare inferiore, che consente un migliore assorbimento attraverso l’epidermide. A causa del potenziale disagio associato all’applicazione, la pomata di tacrolimus è generalmente raccomandata per i cani con lesioni lievi o per quelli con lesioni più gravi dopo la risoluzione completa o parziale con ciclosporina A orale (più spesso in associazione con ketoconazolo).
Alcuni cani possono passare alla pomata di tacrolimus topica da sola per il mantenimento e la prevenzione delle recidive di fistole perianali. Il vantaggio principale di questo trattamento topico è quello di evitare l’immunosoppressione sistemica.
Uno studio più ampio ha mostrato una remissione completa in 16 settimane nel 15 dei 19 pazienti (79%) e un miglioramento marcato nei restanti 4 pazienti quando il tacrolimus è stato usato in associazione con prednisolone, una dieta a base di nuove proteine e un breve ciclo di metronidazolo. Quando il tacrolimus è somministrato da solo, la remissione completa è stata riportata solo nel 50% dei pazienti.
Glucocorticoidi
Dosi immunosoppressive di prednisolone (2-4 mg/kg PO ogni 24 ore) sono state descritte come efficaci, con il 33,3% dei pazienti che ha ottenuto una remissione completa, il 33,3% che ha mostrato un miglioramento dei segni clinici e il 33,3% che non ha mostrato alcun miglioramento. Un vantaggio della terapia con prednisolone è la sua rapida azione rispetto ad altre terapie immunosoppressive; il problema con la terapia con prednisolone risiede negli effetti collaterali a lungo termine.
A causa della necessità di una somministrazione continua di agenti immunomodulatori per la gestione, così come del rischio di effetti collaterali con l’amministrazione a lungo termine di corticosteroidi, i corticosteroidi non vengono generalmente utilizzati da soli per la gestione delle fistole perianali canine. Essi possono tuttavia essere utili nell’ambito di una gestione multimodale, in particolare nella fase iniziale per la loro rapida azione antinfiammatoria.
Altri immunomodulatori
Azatioprina
L’azatioprina, in associazione con il metronidazolo, si è dimostrata efficace nel ridurre le dimensioni delle fistole perianali prima dell’ablazione chirurgica della malattia residua. Nei casi riportati, l’azatioprina è stata continuata per 2-6 settimane dopo l’intervento chirurgico. Un altro studio ha mostrato che la monoterapia con azatioprina portava a una remissione completa in poco più della metà dei cani che la ricevevano. Tuttavia, l’azatioprina può causare effetti collaterali significativi (ad esempio, mielosoppressione grave, epatotossicità, pancreatite), che devono essere presi in considerazione quando si utilizza questo farmaco.
In uno studio di Harkin e collaboratori, 14 cani affetti da fistole perianali sono stati trattati con azatioprina da sola. Dopo 16 settimane di trattamento, 8 dei 14 cani (57%) hanno ottenuto una risoluzione completa delle lesioni.
Micofenolato mofetile
Al meglio delle conoscenze dell’autore, esiste un solo rapporto sull’uso del micofenolato mofetile per la gestione delle fistole perianali nella letteratura veterinaria; questo cane è stato trattato per 4 settimane senza miglioramento delle lesioni.
Terapie alternative ed emergenti
Iniezioni di cellule staminali mesenchimali
Le iniezioni di cellule staminali mesenchimali, somministrate direttamente nelle fistole, si sono dimostrate efficaci nell’uomo affetto da malattia di Crohn fistolizzata. Le cellule staminali mesenchimali hanno un’attività immunomodulatrice, diminuendo la proliferazione e l’attivazione dei linfociti T e delle cellule dendritiche e aumentando la produzione di cellule T regolatorie.
L’efficacia delle iniezioni di cellule staminali mesenchimali per le fistole perianali canine è stata riportata per un piccolo numero di cani. Sei cani affetti da fistole perianali che non avevano risposto alla terapia con ciclosporina A a dosaggio standard per almeno 6 mesi di somministrazione sono stati inclusi in uno studio aperto e hanno ricevuto una singola iniezione di cellule staminali mesenchimali derivate da cellule staminali embrionali umane nelle lesioni perianali. I cani sono stati seguiti per 6 mesi dopo l’iniezione; tutti i cani hanno presentato una risoluzione dei tragitti sinusali o delle ulcere 3 mesi dopo l’iniezione di cellule staminali. Due cani hanno presentato una recidiva delle fistole perianali 6 mesi dopo l’iniezione.
Dopo 1-2 mesi, la dose media di ciclosporina è potuta essere diminuita a 3,59 mg/kg/giorno (a 3 mesi) contro gli 8,22 mg/kg/giorno iniziali. Sebbene le iniezioni di cellule staminali mesenchimali siano un’opzione di trattamento promettente per le fistole perianali canine, sono necessari ulteriori studi controllati per applicare questi risultati a popolazioni più ampie di cani affetti e per determinare la frequenza ottimale delle iniezioni.
Altre terapie innovative
Diversi approcci terapeutici alternativi che mirano alla guarigione delle ferite sono diventati popolari come opzioni di trattamento per le fistole perianali.
-
Plasma ricco di piastrine: Una monoterapia con plasma ricco di piastrine somministrata sotto forma di iniezioni intralesionali in un cane ha portato a una remissione completa senza recidive dopo un anno.
-
Energia luminosa fluorescente: Questa terapia richiede un trattamento settimanale per aiutare a diminuire l’infiammazione e aumentare la guarigione delle ferite. Uno studio su 4 casi ha mostrato una diminuzione del 74,3% della superficie lesa dopo 6 settimane, sebbene non sia stata osservata alcuna guarigione completa. La recente commercializzazione dell’energia luminosa fluorescente l’ha resa più facilmente disponibile per i veterinari.
-
Oclacitinib: Una serie di casi recente ha riportato l’uso di oclacitinib a dosi superiori a quelle utilizzate per la dermatite atopica (1,125 mg/kg BID e 0,88 mg/kg BID) con una guarigione completa in entrambi i casi dopo 1 mese di trattamento. Questo farmaco agisce bloccando l’azione degli interferoni e della via JAK-STAT, il che potrebbe renderlo un trattamento eziologico pertinente data l’attivazione degli interferoni nelle lesioni da fistola perianale.
Trattamenti adiuvanti e considerazioni complementari
Gestione delle infezioni secondarie
Le infezioni secondarie possono accompagnare le fistole perianali e devono essere trattate in modo appropriato, sia con farmaci sistemici che con applicazioni topiche (clorexidina). Le cure igieniche di routine della regione perianale possono essere benefiche (ad esempio, bagni antisettici 2-3 volte a settimana, o anche quotidianamente, a seconda della gravità delle lesioni).
È importante notare che gli antibiotici da soli non sembrano efficaci per la gestione delle fistole perianali nei cani. Molti cani vengono trattati con antimicrobici al momento della comparsa dei segni clinici di fistole perianali ma continuano a presentare una progressione della malattia.
Alcuni studi hanno riportato l’uso del metronidazolo in combinazione con altre terapie (azatioprina, pomata di tacrolimus, prednisolone e una dieta a base di nuove proteine) per il trattamento dei cani affetti da fistole perianali. Oltre alla sua attività contro i batteri anaerobi e i protozoi, il metronidazolo può anche avere un’attività antinfiammatoria, in particolare favorendo la differenziazione delle cellule T regolatorie. Questa attività antinfiammatoria può aiutare nel trattamento delle malattie immuno-mediate, ma l’efficacia del metronidazolo da solo per il trattamento delle fistole perianali è sconosciuta ad oggi.
Gestione del dolore e del comfort
I cani con fistole perianali attive possono soffrire, in particolare durante la defecazione. Gli emollienti fecali dovrebbero essere considerati e, in alcuni casi, i clisteri possono essere necessari per alleviare il tenesmo. L’analgesia dovrebbe essere una priorità per i cani con lesioni attive, ma il potenziale di stitichezza con l’uso di alcuni analgesici, come gli agonisti oppioidi, deve essere preso in considerazione quando si sviluppa un piano di gestione del dolore.
Considerazioni alimentari
È stato identificato un legame tra fistole perianali e reazioni alimentari avverse. In uno studio, il 18,8% dei cani con fistola perianale soffriva anche di allergie alimentari. Non è chiaro se esista una correlazione diretta tra queste malattie o se i cani avessero semplicemente due malattie concomitanti. In ogni caso, l’uso di una dieta a base di proteine nuove o di una dieta idrolizzata è stato benefico per alcuni pazienti.
Tre studi hanno riportato una risposta clinica positiva a una dieta a base di nuove proteine in cani con fistole perianali. In uno studio, una dieta a base di pesce e patate è stata somministrata a lungo termine dopo l’escissione chirurgica dei tratti sinusali e la sacculectomia anale bilaterale. Nel secondo studio, i cani hanno ricevuto una dieta esclusiva a base di cervo e patate o pesce e patate, ma hanno anche ricevuto inizialmente metronidazolo, oltre a pomata di tacrolimus allo 0,1% topica e un ciclo decrescente di prednisolone orale per 16 settimane. Nel terzo studio, i cani hanno ricevuto una dieta commerciale a base di agnello e riso o vegetariana, ma hanno anche ricevuto simultaneamente un ciclo decrescente di prednisolone orale a una dose immunosoppressiva iniziale.
Sebbene l’attuazione di una dieta di eliminazione che utilizzi un alimento a base di nuove proteine o di proteine idrolizzate sia raccomandata nell’ambito della valutazione diagnostica dei cani affetti da fistole perianali, non è chiaro, dalla letteratura disponibile, quanti cani possano ottenere una remissione a lungo termine con il solo controllo alimentare.
Raccomandazioni consensuali per la gestione delle fistole perianali
Metodologia di elaborazione del consenso
Di fronte all’assenza di consenso sulla gestione delle fistole perianali, il consiglio scientifico del GEDAC (Gruppo di Studio in Dermatologia degli Animali da Compagnia) ha intrapreso l’elaborazione di un quadro della letteratura al fine di giungere a raccomandazioni per la gestione medica.
La metodologia adottata si basa sulla tassonomia della forza di raccomandazione (SoRT) sviluppata dagli editori di riviste di medicina generale e di pronto soccorso negli Stati Uniti. Il livello di prova (LoE) è stato classificato secondo una scala a tre livelli:
- LoE 1: Prove di buona qualità (meta-analisi, studio prospettico controllato randomizzato di buona qualità)
- LoE 2: Prove di qualità limitata (studio prospettico controllato randomizzato di bassa qualità, studio controllato, studio di caso versus un gruppo di controllo, studio prospettico di buona qualità)
- LoE 3: Altre prove, inclusi linee guida di consenso, opinioni, studi di caso
È stata effettuata una ricerca sistematica della letteratura pubblicata tra il 1980 e l’ottobre 2023 nel database PubMed. Gli articoli in inglese e francese sono stati ricercati utilizzando parole chiave specifiche, e i seguenti tipi di studi sono stati inizialmente selezionati: studi controllati randomizzati, studi clinici, studi di coorte e serie di casi.
Per l’elaborazione delle raccomandazioni è stata utilizzata una scala a tre livelli:
- Livello A: Raccomandazione forte, basata su prove di buona qualità, coerenti
- Livello B: Raccomandazione moderata, basata su prove incoerenti o di qualità limitata
- Livello C: Raccomandazione debole, basata principalmente sull’opinione di esperti
Raccomandazioni terapeutiche principali
Ciclosporina A
- L’efficacia della ciclosporina è reale (livello di raccomandazione A)
- L’efficacia è dose-dipendente e indipendente dalla gravità clinica
- La dose minima raccomandata è di 5 mg/kg/giorno, potendo arrivare a 10 mg/kg due volte al giorno
- La dose efficace deve essere mantenuta fino al raggiungimento della guarigione clinica (livello C)
- Potrebbe essere necessario un periodo di tre mesi per osservare la guarigione sotto ciclosporina
Associazione ciclosporina-ketoconazolo
- Questa associazione è efficace
- Tuttavia, gli esperti non raccomandano questa associazione al fine di limitare i rischi di resistenza agli antifungini e i danni epatici
Tacrolimus
In Francia, l’evoluzione della legislazione rende l’uso del tacrolimus difficile da prendere in considerazione.
Prednisolone
- Gli esperti non raccomandano l’uso della prednisolone da sola
- La corticoterapia è consigliata nell’ambito di una gestione multimodale
- È consigliabile non superare 1 mg/kg/giorno come dose di attacco per limitare gli effetti indesiderati
- La corticoterapia locale potrebbe essere interessante nonostante l’assenza di dati scientifici solidi al riguardo
Altri immunomodulatori
Gli esperti non raccomandano l’uso di azatioprina, micofenolato mofetile, oclacitinib, fotobiomodulazione o cellule staminali per mancanza di dati affidabili e ripetuti disponibili ad oggi.
Antibioterapia
- L’antibiotecaria non è necessaria per ottenere la guarigione
- Il metronidazolo, poco utilizzato negli studi, non permette di valutarne l’impatto sull’evoluzione della malattia
- Gli esperti non raccomandano l’uso sistematico di antibiotici
- L’antibiotecaria è raccomandata solo in caso di fistola rettale o di infezione delle sacche anali, sulla base dei risultati di una coltura batterica
Approccio chirurgico
- Gli esperti raccomandano il ricorso alla chirurgia in seconda intenzione
- Questo approccio è indicato per un animale che presenta ancora fastidio o dolore (qualità di vita alterata) dopo un miglioramento ottenuto con il trattamento medico
- L’uso della chirurgia può essere condizionato da ragioni economiche o da una stasi nel miglioramento clinico in un animale la cui qualità di vita rimane insufficiente
Alimentazione
- Nessuna prova scientifica consente di raccomandare l’uso di alimenti a base di proteine nuove o idrolizzate
- Per analogia con la malattia di Crohn nell’uomo e sulla base dell’esperienza clinica, gli esperti consigliano l’introduzione di un’alimentazione ipoallergenica (livello C)
Monitoraggio e adattamento terapeutico
- Si raccomanda di valutare il trattamento medico dopo 6-10 settimane e di modificarlo in base alla risposta osservata
- Dopo la guarigione o in presenza di lesioni persistenti moderate associate a una buona qualità di vita, il trattamento potrà essere semplificato o addirittura interrotto
- In assenza di dati scientifici, gli esperti raccomandano una semplificazione o una sospensione graduale e adattata del trattamento
Discussione e prospettive
Paralleli con le patologie umane
Due affezioni umane, l’idrosadenite suppurativa e la malattia di Crohn fistolizzante, sono state proposte come correlati delle fistole perianali canine. Come le fistole perianali nei cani, queste due affezioni sono dolorose, invalidanti e possono avere un impatto negativo sulla qualità di vita dei pazienti.
L’idrosadenite suppurativa è associata a noduli, ascessi, tratti sinusali e cicatrici, principalmente nelle regioni intertriginose (ascelle, inguine, regione perianale e regione mammaria). È stata inizialmente proposta come potenziale correlato delle fistole perianali canine a causa di caratteristiche istopatologiche simili, tra cui foruncolosi, idradenite e formazione di tratti sinusali rivestiti da epitelio. La patogenesi dell’idrosadenite suppurativa non è stata completamente chiarita, ma si tratta probabilmente di una condizione immuno-mediata con una suscettibilità genetica. Alterazioni del microbiota cutaneo o intestinale possono giocare un ruolo nella patogenesi.
Le manifestazioni perianali della malattia di Crohn sono frequenti, si stima che colpiscano il 25% al 33% dei pazienti con malattia di Crohn. Le fistole perianali sono più frequenti nei pazienti con malattia colica o rettale e possono essere semplici (un tratto fistoloso con una singola apertura esterna) o complesse (molteplici tratti fistolosi, ascessi perianali o stenosi anale/rettale). A differenza della malattia tipica nei cani, si tratta di vere e proprie fistole che comunicano con il lume intestinale. La patogenesi delle fistole perianali nella malattia di Crohn non è completamente compresa ma implicherebbe una transizione epitelio-mesenchimale e una sovraregolazione delle metalloproteinasi di matrice e delle citochine pro-infiammatorie.
Sono state dimostrate somiglianze nella patogenesi dell’idrosadenite suppurativa e della malattia di Crohn, in particolare l’infiltrazione dei tessuti malati da parte dei linfociti T helper di tipo 17. Studi futuri dovrebbero concentrarsi su una migliore caratterizzazione dell’eziologia sottostante di queste tre affezioni e potrebbero aiutare a orientare lo sviluppo di future terapie, come anticorpi che mirano a citochine specifiche, per le fistole perianali nei cani.
Prospettive future e percorsi di ricerca
Diverse aree di ricerca meritano particolare attenzione per migliorare la gestione delle fistole perianali canine:
-
Studio approfondito della patogenesi immunitaria: Una migliore comprensione dei meccanismi immuno-mediati coinvolti potrebbe portare allo sviluppo di terapie mirate, come l’uso di inibitori di JAK (oclacitinib) la cui efficacia è stata suggerita da alcuni studi preliminari.
-
Caratterizzazione del microbioma cutaneo e intestinale: L’esplorazione del ruolo giocato dal microbioma nello sviluppo e nella persistenza delle fistole perianali potrebbe aprire nuove piste terapeutiche, come l’uso di probiotici o il trapianto fecale.
-
Ottimizzazione dei protocolli terapeutici: Sono necessari studi controllati per determinare le dosi ottimali, le durate del trattamento e le strategie di svezzamento delle diverse opzioni terapeutiche.
-
Valutazione più standardizzata della qualità di vita: Lo sviluppo di strumenti specifici per valutare l’impatto delle fistole perianali e dei loro trattamenti sulla qualità di vita dei cani permetterebbe un approccio più centrato sul benessere animale.
-
Sviluppo di terapie innovative: I risultati preliminari incoraggianti ottenuti con le cellule staminali mesenchimali, il plasma ricco di piastrine o l’energia luminosa fluorescente meritano di essere approfonditi con studi controllati su popolazioni più ampie.
-
Studio dei collegamenti con le allergie alimentari: La chiarificazione dei collegamenti potenziali tra fistole perianali e reazioni alimentari avverse permetterebbe di ottimizzare gli approcci nutrizionali.
- Identificazione di biomarcatori predittivi: La ricerca di marcatori biologici che consentano di prevedere la risposta al trattamento o il rischio di recidiva migliorerebbe la personalizzazione terapeutica.
Importanza dell’approccio individualizzato
La gestione delle fistole perianali canine richiede un approccio individualizzato, che tenga conto di diversi fattori:
-
Equilibrio terapeutico: La ricerca di un equilibrio tra efficacia del trattamento, costo, effetti indesiderati e qualità di vita dell’animale è essenziale.
-
Obiettivi realistici: Se la guarigione clinica completa rimane l’obiettivo teorico, il miglioramento clinico con una qualità di vita preservata può costituire un obiettivo accettabile in alcuni casi.
-
Adattabilità terapeutica: La valutazione regolare della risposta al trattamento e l’aggiustamento dei protocolli in funzione di questa risposta sono cruciali per ottimizzare la gestione.
-
Approccio multimodale: La combinazione di diverse modalità terapeutiche (farmaci immunomodulatori, cure locali, gestione del dolore, approccio nutrizionale) offre spesso le migliori probabilità di successo.
-
Considerazione del contesto: I vincoli finanziari, la capacità del proprietario di somministrare i trattamenti e di effettuare le cure necessarie, nonché le eventuali comorbidità devono essere integrate nella strategia terapeutica.
Conclusione
Le fistole perianali canine rappresentano un’affezione dermatologica complessa a patogenesi immuno-mediata la cui prevalenza è particolarmente elevata nel Pastore Tedesco. Questa patologia, potenzialmente invalidante, può avere un impatto significativo sulla qualità di vita degli animali affetti e richiede una gestione rapida e appropriata.
La comprensione di questa malattia si è notevolmente evoluta nel corso dei decenni, con un cambiamento di paradigma che è passato da una visione principalmente anatomica e chirurgica a un approccio immuno-mediato e medico. Le terapie immunomodulatrici, in particolare la ciclosporina A, costituiscono oggi la pietra angolare del trattamento, consentendo di ottenere tassi di guarigione significativi.
L’analisi metodica della letteratura scientifica ha permesso di stabilire raccomandazioni consensuali per guidare i clinici nelle loro scelte terapeutiche. Queste raccomandazioni sottolineano l’efficacia della ciclosporina A a dosi appropriate (minimo 5 mg/kg/giorno), il ruolo limitato ma complementare della corticoterapia e il potenziale interesse di alcune terapie emergenti come l’oclacitinib o le cellule staminali mesenchimali.
La chirurgia, un tempo considerata il trattamento di riferimento, è oggi riservata ai casi refrattari o come complemento dopo stabilizzazione medica. L’approccio alimentare, sebbene manchino ancora prove scientifiche solide, è spesso integrato nella strategia terapeutica globale.
I paralleli stabiliti con patologie umane come l’idrosadenite suppurativa o la malattia di Crohn fistolizzante aprono prospettive interessanti per la ricerca traslazionale e lo sviluppo di nuovi approcci terapeutici mirati.
L’obiettivo finale della gestione rimane il miglioramento della qualità di vita dell’animale, che a volte può essere raggiunto senza la completa guarigione delle lesioni. Un approccio individualizzato, che tenga conto delle specificità di ogni paziente, dei vincoli pratici e delle aspettative dei proprietari, rimane essenziale per ottimizzare le possibilità di successo terapeutico a lungo termine.
Domande frequentemente poste
1. La gravità iniziale delle lesioni influisce sulla prognosi e sulla risposta al trattamento?
Gli studi non hanno dimostrato una correlazione significativa tra la gravità iniziale delle lesioni e la risposta al trattamento, in particolare con la ciclosporina. Tuttavia, una diagnosi precoce e l’implementazione rapida di un trattamento appropriato migliorano generalmente la prognosi. I casi cronici, con fibrosi consolidata, possono essere più refrattari alla terapia.
2. Come gestire le recidive dopo l’interruzione del trattamento?
In caso di recidiva dopo l’interruzione del trattamento, la ripresa del protocollo inizialmente efficace è generalmente consigliata. Una volta ottenuta la remissione, un svezzamento più graduale può essere considerato, o una terapia di mantenimento a dose minima efficace (ad esempio, ciclosporina a dose ridotta o tacrolimus topico) può essere mantenuta a lungo termine. L’identificazione e la gestione dei potenziali fattori scatenanti, come le allergie alimentari, sono anch’esse importanti.
3. I fattori ambientali influenzano l’evoluzione delle fistole perianali?
Sebbene poco studiati in modo specifico, alcuni fattori ambientali sembrano influenzare l’evoluzione della malattia. L’igiene perianale, la consistenza delle feci (influenzata dall’alimentazione), lo stress e l’attività fisica possono tutti avere un impatto sulla cicatrizzazione e sul comfort dell’animale. Un ambiente pulito e cure locali regolari contribuiscono positivamente alla gestione della condizione.
4. Quali sono i rischi di effetti collaterali a lungo termine dei trattamenti immunosoppressori?
I trattamenti immunosoppressivi a lungo termine presentano diversi rischi:
- Per la ciclosporina: disturbi digestivi, iperplasia gengivale, irsutismo, aumento del rischio di infezioni opportunistiche e potenziale sviluppo di neoplasie (raro)
- Per i corticosteroidi: sindrome di Cushing iatrogena, diabete mellito, atrofia cutanea, immunosoppressione, rischio di infezioni secondarie
- Per l’azatioprina: mielosoppressione, epatotossicità, pancreatite
Un monitoraggio regolare che includa esame clinico, analisi del sangue e aggiustamenti della posologia è essenziale per minimizzare questi rischi.
5. Esistono modi per prevedere quali cani Pastore Tedesco svilupperanno questa condizione?
Attualmente non esiste un test predittivo validato che permetta di identificare con certezza i Pastori Tedeschi a rischio di sviluppare fistole perianali. Tuttavia, sono stati identificati alcuni fattori di rischio:
- I cani omozigoti per l’allele DLA-DRB1*00101 potrebbero sviluppare la malattia più precocemente
- Una storia familiare di fistole perianali sembra aumentare il rischio
- Alcuni lignaggi sembrano più colpiti di altri
Ulteriori ricerche sui marcatori genetici e immunologici potrebbero permettere lo sviluppo di test predittivi in futuro, aprendo la strada a strategie preventive negli individui a rischio.