Dalla prima pubblicazione di Wittich nel 1941, che riportava il successo del trattamento di un’allergia in un cane mediante ASIT (Immunoterapia Allergene Specifica), sono stati fatti molti progressi. Sebbene gli studi sull’uomo siano numerosi e documentino ampiamente l’efficacia dell’ASIT in varie patologie allergiche, in particolare la rinite allergica e l’asma, i dati relativi alla DAC rimangono, paradossalmente, frammentari.
Stato delle conoscenze sull’ASIT canina
Mentre nell’uomo alcuni mettono in discussione l’utilità dell’ASIT nella dermatite atopica umana, questa controversia non è apparentemente mai emersa in medicina veterinaria, probabilmente a causa dei primi incoraggianti rapporti riguardanti la DAC. L’assenza di controversie in medicina veterinaria potrebbe anche essere correlata a fattori quali il numero limitato di studi clinici rigorosi condotti nei cani, la complessità della valutazione dell’efficacia dell’ASIT nel contesto della DAC e la variabilità dei protocolli terapeutici utilizzati tra i diversi studi. Questi fattori rendono difficile il confronto diretto dei risultati, limitando così le conclusioni globali sull’efficacia dell’ASIT canina.
Studi, incluso uno studio in cieco controllato con placebo su 51 cani, hanno dimostrato tassi di risposta (generalmente definiti come la percentuale di cani che mostrano un miglioramento di almeno il 50% dei segni clinici) dell’ordine del 60-70%. Tuttavia, è fondamentale notare che, anche nei casi positivi, una percentuale significativa di cani (fino al 65% in uno studio) ha richiesto un trattamento farmacologico complementare, mettendo in discussione la capacità dei proprietari di giudicare obiettivamente l’efficacia dell’ASIT. Le attuali linee guida per il trattamento della DAC qualificano la qualità delle prove pubblicate sull’efficacia dell’ASIT come “limitata”. Questa limitazione delle prove è dovuta a diversi fattori, tra cui le dimensioni ridotte di molti studi, la mancanza di standardizzazione dei protocolli e la difficoltà di ottenere misurazioni oggettive dell’efficacia dell’ASIT nel cane. È importante sottolineare che la valutazione dell’efficacia dell’ASIT si basa spesso su valutazioni soggettive dei proprietari, il che può introdurre un bias nei risultati. Sono necessari metodi di valutazione più obiettivi, come l’uso di biomarcatori o di punteggi clinici validati, per migliorare la qualità delle prove disponibili.
L’interpretazione dei risultati degli studi sull’ASIT canina è spesso complicata dalla variabilità dei protocolli utilizzati. Le differenze in termini di dosaggio, composizione degli estratti allergenici, frequenza delle iniezioni, trattamenti concomitanti e metodi di valutazione dei risultati rendono difficile il confronto diretto dei risultati ottenuti nei diversi studi. L’eterogeneità delle popolazioni di cani incluse negli studi costituisce un altro fattore di complessità. La variabilità delle razze, delle età, della gravità della DAC e delle anamnesi dei cani può influenzare la risposta all’ASIT, rendendo più complessa l’analisi dei risultati. Per migliorare l’interpretazione dei dati, gli studi futuri devono concentrarsi sulla standardizzazione dei protocolli, sull’omogeneità delle popolazioni studiate e sull’uso di misure di efficacia più oggettive.
Confronto con l’ASIT umana: Sebbene l’ASIT sia utilizzata per trattare varie allergie nell’uomo, l’efficacia e i meccanismi d’azione non sono sempre completamente compresi e variano a seconda del tipo di allergia e dell’individuo. Esiste una controversia riguardo all’utilità dell’ASIT nella dermatite atopica umana, con alcuni studi che ne mettono in discussione l’efficacia, mentre altri mostrano risultati positivi. Questa sfumatura riflette la complessità delle risposte immunitarie individuali e l’eterogeneità della dermatite atopica. Il confronto con l’ASIT umana consente di identificare piste di ricerca per l’ASIT canina, ma è importante sfumare questi confronti a causa delle differenze fisiologiche e immunologiche tra le specie.
Meccanismi d’azione: il conosciuto e l’ignoto
Il preciso meccanismo d’azione dell’ASIT canina rimane ancora incompletamente chiarito. Tuttavia, un parallelo con i meccanismi umani è plausibile. Nell’uomo si osserva una riduzione iniziale dell’attività delle cellule effettrici (eosinofili, basofili, mastociti), seguita da un cambiamento immunologico a lungo termine, passando da una risposta delle cellule Th2 (helper 2) a una risposta delle cellule Th1 (helper 1) e allo sviluppo di una tolleranza immunologica. Questo processo complesso e multifattoriale coinvolge diverse fasi e popolazioni cellulari.
- Fase iniziale: L’esposizione agli allergeni a basse dosi provoca una modulazione della risposta infiammatoria immediata. Ciò si traduce in una riduzione del rilascio di istamina e altri mediatori dell’infiammazione da parte dei mastociti e dei basofili, il che diminuisce i sintomi immediati dell’allergia. La degranulazione dei mastociti, processo chiave nella risposta allergica immediata, è inibita o attenuata.
- Fase tardiva: La risposta immunitaria si sposta progressivamente verso un profilo Th1, con un aumento dei linfociti T helper 1 che producono citochine pro-infiammatorie come l’interferone-gamma (IFN-γ) e una diminuzione dei linfociti T helper 2 e delle citochine associate (IL-4, IL-5, IL-13). Questo passaggio Th1/Th2 partecipa alla regolazione della risposta infiammatoria a lungo termine.
- Ruolo delle cellule T regolatorie (Treg): Le cellule Treg, con marcatori come FOXP3, svolgono un ruolo cruciale nella tolleranza immunitaria acquisita dall’ASIT. Queste cellule sopprimono l’attività dei linfociti T effettori, contribuendo all’attenuazione della reazione infiammatoria allergica. L’aumento del numero e dell’attività delle cellule Treg è correlato a una migliore risposta all’ASIT.
- Produzione di IgG: La produzione di immunoglobuline G (IgG), in particolare IgG4, specifiche per l’allergene aumenta dopo un trattamento prolungato. Questi anticorpi IgG bloccanti potrebbero ridurre il legame delle IgE agli allergeni, diminuendo così la loro capacità di scatenare una risposta infiammatoria. Gli studi rimangono tuttavia incerti sull’impatto reale delle IgG sulla riduzione della risposta allergica.
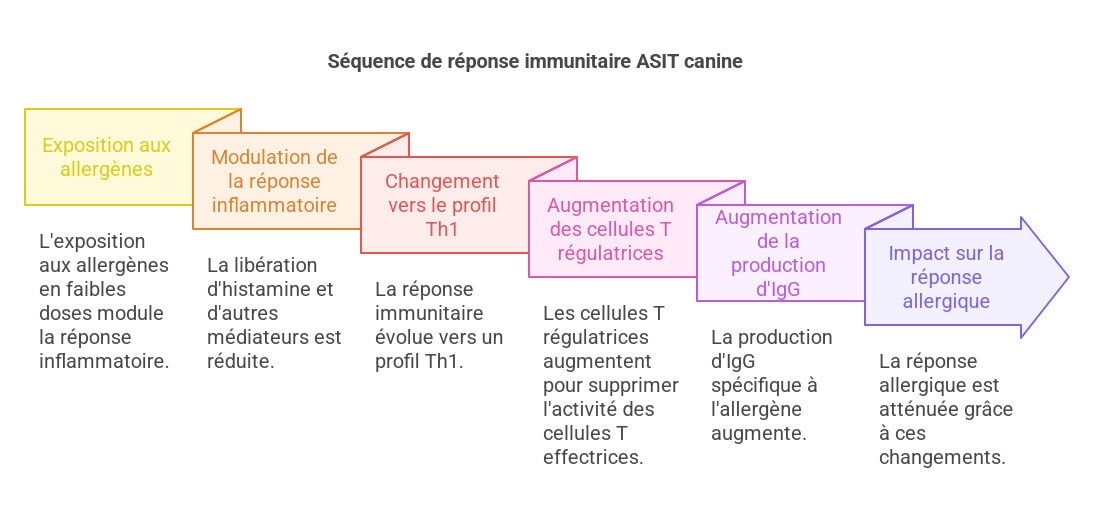
Questi cambiamenti si accompagnano a un aumento di citochine come il fattore di crescita trasformante beta (TGFβ) e l’interleuchina (IL)-10, citochine antinfiammatorie che svolgono un ruolo nel mantenimento della tolleranza immunitaria. Ne consegue un aumento delle immunoglobuline (IgG) specifiche per l’allergene, in particolare IgG4, e, con un trattamento prolungato, una diminuzione delle IgE specifiche per l’allergene. Nel cane, sebbene le conoscenze siano meno estese, un passaggio a una risposta Th1, un aumento dei livelli di IgG, la comparsa di più cellule Treg e aumenti dei livelli di IL-10 sono stati tutti dimostrati, stabilendo così paralleli con l’ASIT umana. Tuttavia, gli studi nel cane sono meno numerosi e meno approfonditi rispetto all’uomo, e l’esplorazione dei meccanismi d’azione dell’ASIT canina richiede ulteriori ricerche per una comprensione più completa. L’uso di modelli animali (ad esempio topi) può consentire di chiarire alcuni meccanismi, ma l’estrapolazione alla specie canina deve essere fatta con cautela.
La somministrazione sublinguale implica un effetto aggiuntivo da parte delle cellule dendritiche oromucosali. Nell’uomo, queste cellule svolgono un ruolo importante nell’induzione della tolleranza orale, un processo immunologico attraverso il quale il sistema immunitario è programmato per non reagire alle sostanze introdotte nella bocca (ad esempio, gli alimenti). Il ruolo preciso di queste cellule nell’ASIT canina deve ancora essere esplorato.
Approcci attuali dell’ASIT canina: efficacia e aree di miglioramento
Gli approcci attuali dell’ASIT per la DAC si basano su due principali vie di somministrazione: sottocutanea (SCIT) e sublinguale (SLIT). La SCIT, praticata da decenni, utilizza estratti allergenici acquosi conservati con fenolo in Nord America ed estratti allergenici precipitati con allume in Europa. L’uso di adiuvanti a base di alluminio, nonostante il vantaggio di iniezioni meno frequenti, solleva crescenti preoccupazioni sui suoi potenziali effetti avversi a lungo termine, legati a un’esposizione cronica all’alluminio. Sono necessari studi approfonditi sulla tossicità a lungo termine dell’alluminio per valutare appieno le implicazioni del suo uso nei vaccini e nei trattamenti allergici. Attualmente si stanno studiando alternative agli adiuvanti a base di alluminio, in particolare adiuvanti più biocompatibili e meno tossici.
La SLIT, più diffusa nell’uomo, è apparsa più recentemente in medicina veterinaria ed è oggetto di controversie nell’uomo per l’affidabilità di molti studi precedenti con protocolli molto variabili. Analisi e posizioni recenti dell’Organizzazione Mondiale dell’Allergia concludono sulla sua efficacia e su un profilo di sicurezza favorevole rispetto alla SCIT. Tuttavia, i dati sulla SLIT canina sono ancora limitati e richiedono studi aggiuntivi per validarne l’efficacia e la sicurezza in questa specie. Gli studi condotti nell’uomo suggeriscono che la SLIT potrebbe essere un approccio più pratico e più sicuro della SCIT. Tuttavia, la variabilità dei protocolli utilizzati negli studi umani rende difficile la determinazione di protocolli ottimali per la SLIT canina, rendendo necessari studi futuri per la validazione del suo utilizzo nel cane. Allo stesso modo, studi comparativi tra SCIT e SLIT nella DAC sono essenziali per valutare la loro efficacia relativa e i benefici e gli svantaggi di ciascun metodo.
Considerazioni importanti sulla qualità degli estratti utilizzati influenzano l’efficacia. Gli estratti allergenici per uso veterinario hanno ricevuto una licenza dal Dipartimento dell’Agricoltura degli Stati Uniti (USDA) decenni fa, basandosi su criteri di sicurezza, purezza, sterilità e coerenza di produzione, e non su studi rigorosi di efficacia a lungo termine. Questa situazione evidenzia la necessità di nuove regolamentazioni e standard più stringenti per garantire la qualità e l’efficacia degli estratti allergenici utilizzati in medicina veterinaria.
La letteratura scientifica riguardante l’ASIT canina soffre di una mancanza di standardizzazione dei protocolli, con una grande variabilità dei regimi di dosaggio, degli estratti allergenici, della loro composizione e della loro potenza tra i produttori, dei programmi di somministrazione, dei trattamenti concomitanti e dei metodi di miscelazione degli estratti. Questa mancanza di standardizzazione limita la comparabilità degli studi e l’interpretazione dei risultati. L’assenza di protocolli standardizzati rende difficile la valutazione dell’efficacia reale dell’ASIT e la determinazione dei parametri ottimali per il trattamento della DAC.
Dettagli sui diversi approcci:
- SCIT (Sottocutanea): L’allergene viene iniettato sotto la pelle. Esistono diversi approcci, con un aumento progressivo delle dosi (induzione) e uno schema di mantenimento a lungo termine. Gli estratti possono essere acquosi (Nord America) o precipitati con allume (Europa) per un rilascio più lento. L’uso dell’allume solleva interrogativi sulla tossicità a lungo termine dell’alluminio, richiedendo studi e una valutazione del rapporto rischio-beneficio.
- SLIT (Sublinguale): L’allergene viene somministrato sotto la lingua, un approccio meno invasivo potenzialmente migliore per l’adesione del proprietario. Sono tuttavia necessari studi più numerosi e una migliore standardizzazione per la sua calibrazione in clinica veterinaria.
- RIT (Immunoterapia accelerata): Somministrazione rapida di dosi crescenti di allergene in un breve periodo, che richiede uno stretto monitoraggio. Esistono rischi maggiori di effetti avversi, ma può essere più pratica per alcuni cani.
Miglioramento della standardizzazione dell’ASIT canina
L’istituzione dei principali epitopi allergenici nel cane, in particolare per gli allergeni comuni, consentirebbe una standardizzazione degli estratti, un dosaggio uniforme, la produzione di allergeni ricombinanti e l’uso dell’immunoterapia peptidica. L’identificazione degli epitopi allergenici maggiori nel cane consente di creare estratti più specifici e purificati. Questi estratti standardizzati consentono una migliore riproducibilità dei risultati tra i diversi studi, migliorando così l’affidabilità dei dati. Inoltre, la conoscenza degli epitopi consente lo sviluppo di allergeni ricombinanti, sintetizzati in laboratorio, il che consente di ottenere preparazioni di allergeni più pure e omogenee.
Il dosaggio dell’allergene è fondamentale. Nell’uomo, la dose e l’intervallo di iniezione influenzano l’efficacia. Questi parametri non sono stati sufficientemente studiati nel cane. Studi dose-risposta sono cruciali per determinare la dose ottimale di allergene che massimizza l’efficacia minimizzando gli effetti avversi. L’identificazione di biomarcatori predittivi della risposta all’ASIT potrebbe anche consentire di personalizzare il trattamento in base alla risposta individuale del cane.
Allo stesso modo, l’immunoterapia accelerata (RIT) presenta vantaggi in termini di numero di iniezioni a domicilio, ma anche rischi di sicurezza accresciuti e un costo più elevato a causa dell’ospedalizzazione necessaria. L’immunoterapia accelerata (RIT) è un approccio che consente di somministrare le dosi di allergene più rapidamente. Ciò può ridurre la durata del trattamento e migliorare l’aderenza del proprietario, ma aumenta il rischio di effetti avversi. Per ottimizzare l’uso della RIT, è necessario documentare meglio la sicurezza e l’efficacia di questo metodo, ed eventualmente ideare protocolli meno intensivi al fine di ridurre i rischi preservando l’efficacia. Sono necessari studi che confrontino la RIT con l’immunoterapia convenzionale.
Ottimizzazione dei protocolli di ASIT canina
L’omogeneizzazione dei protocolli di ASIT canina rappresenta una sfida importante. Il numero ottimale di estratti in una miscela deve essere ancora definito, così come il modo di gestire gli estratti contenenti proteasi, come le muffe. La standardizzazione dei protocolli richiede un approccio multifattoriale. È necessario definire i parametri ottimali di trattamento, in particolare:
- Numero e tipo di allergeni: Determinare il numero di allergeni da includere nella miscela. Studi suggeriscono che un singolo allergene dominante può essere sufficiente, anche in caso di polisensibilizzazione, sebbene questo approccio sia meno comune in Nord America che in Europa.
- Gestione delle proteasi: Le muffe contengono proteasi che possono degradare altri allergeni. Ciò può compromettere l’efficacia della miscela di allergeni. La gestione di questo problema richiede uno studio aggiuntivo.
- Metodi di selezione degli allergeni: Utilizzare i test intradermici, i test sierologici o una combinazione di entrambi. Le limitazioni di ciascun metodo devono essere prese in considerazione. Sono necessarie ulteriori ricerche per determinare il metodo ottimale di selezione degli allergeni per l’ASIT canina.
- Formulazione della miscela di allergeni: Sono necessari ulteriori studi per determinare l’approccio migliore, il che consentirà un miglioramento della riproducibilità degli studi.
Documenti ufficiali raccomandano di non mescolare estratti di muffe e pollini nello stesso flacone a causa della degradazione degli allergeni pollinici da parte delle proteasi fungine durante la conservazione. Dati simili, ma meno probanti, esistono per il cane. Queste raccomandazioni sottolineano la necessità di comprendere meglio le interazioni tra i diversi allergeni nella miscela. È importante tenere conto delle potenziali degradazioni enzimatiche a livello dei diversi componenti della miscela e determinare così la formulazione ottimale al fine di garantire un’efficacia a lungo termine.
Biomarcatori di successo terapeutico e nuovi approcci
L’uso di biomarcatori per la valutazione obiettiva del successo dell’ASIT canina è essenziale per migliorare gli studi clinici, ovviare alla mancanza di dati riproducibili e superare l’importante effetto placebo. Sebbene siano stati osservati nel cane aumenti delle concentrazioni sieriche totali di IgG1, risposte specifiche in IgG all’immunoterapia agli acari della polvere e modificazioni di diversi livelli di cellule Treg, queste scoperte non sono state sufficientemente approfondite da fungere da mezzo di valutazione obiettiva e rapida del successo dell’ASIT. L’identificazione di biomarcatori affidabili consentirebbe una migliore valutazione dell’efficacia del trattamento e una migliore previsione della risposta individuale all’ASIT.
I potenziali biomarcatori da esplorare includono:
- Concentrazioni sieriche di IgG (soprattutto IgG4): L’aumento delle IgG specifiche per l’allergene potrebbe corrispondere a un miglioramento clinico. La misurazione delle IgG4 è particolarmente promettente, in quanto questa sottoclasse di IgG è particolarmente legata all’induzione della tolleranza.
- Cellule T regolatorie (Treg): Il numero e l’attività delle cellule Treg sono indicatori chiave della tolleranza immunitaria. La misurazione delle Treg circolanti o nei tessuti potrebbe essere utile per monitorare la risposta all’ASIT.
- Citochine antinfiammatorie (IL-10, TGF-β): L’aumento di queste citochine potrebbe indicare una diminuzione dell’infiammazione allergica.
- Attività delle cellule effettrice (eosinofili, basofili, mastociti): La diminuzione dell’attività potrebbe essere correlata a una migliore risposta clinica.
- Misurazioni oggettive del prurito: Per esempio, l’uso di accelerometri per quantificare l’attività di grattage.
L’uso di biomarcatori combinati potrebbe fornire un’immagine più completa della risposta all’ASIT, migliorando così l’interpretazione dei risultati degli studi clinici.
Nuovi approcci terapeutici
Lo sviluppo di preparazioni allergeniche modificate (allergicoidi, allergeni ricombinanti o peptidi) e il miglioramento dell’efficacia degli allergeni tramite adiuvanti (induttori di IL-10, incapsulamento in particelle tipo virus (VLPs) o, nel caso di SLIT, polimeri mucoadesivi) rappresentano assi di progresso promettenti. Queste preparazioni modificate presentano diversi vantaggi:
- Allergooidi: Allergeni modificati chimicamente per ridurre la loro capacità di scatenare una reazione allergica immediata, pur mantenendo la loro capacità immunogena. Ciò ridurrebbe i rischi di effetti indesiderati.
- Allergeni ricombinanti: Allergeni prodotti in laboratorio, che offrono una purezza e un’omogeneità superiori agli estratti naturali.
- Peptidi allergenici: Piccoli frammenti di allergeni contenenti epitopi specifici per i linfociti T, che minimizzano i rischi di anafilassi.
L’aggiunta di immunomodulanti (oligodeossinucleotidi CpG, anticorpi monoclonali specifici) potrebbe indirizzare la risposta immunitaria verso una tolleranza specifica moderando la “tempesta di citochine” nell’infiammazione attiva. Questi immunomodulanti consentono di manipolare la risposta immunitaria, favorendo le risposte antinfiammatorie e la tolleranza immunitaria. I CpG ODN stimolano l’immunità innata attivando le cellule dendritiche e le cellule NK, e gli anticorpi monoclonali possono mirare a citochine pro-infiammatorie specifiche.
Studi condotti su vie alternative di somministrazione (immunoterapia epicutanea o intralinfatica) si stanno rivelando promettenti. L’immunoterapia epicutanea applicata per via topica sulla pelle potrebbe indurre una tolleranza locale e sistemica agli allergeni. L’immunoterapia intralinfatica, consistente nell’iniettare l’allergene direttamente nei linfonodi, potrebbe ottimizzare il contatto con le cellule immunitarie coinvolte nello sviluppo della tolleranza. Sebbene esistano studi sull’immunoterapia intralinfatica nel cane, sono necessarie ulteriori ricerche per definire i protocolli ottimali e valutarne a lungo termine l’efficacia e la sicurezza. Inoltre, l’immunoterapia intralinfatica potrebbe essere meno gravosa per il proprietario rispetto all’immunoterapia sottocutanea classica, migliorando così l’aderenza terapeutica.
Inoltre, i progressi compiuti nell’immunoterapia per le allergie alimentari umane, in particolare l’uso della diagnostica molecolare e dei metodi di somministrazione alternativi, potrebbero ispirare approcci innovativi per la DAC. L’ottimizzazione della diagnostica delle allergie alimentari nel cane è un’importante area di ricerca. Metodi diagnostici molecolari più precisi potrebbero identificare gli allergeni alimentari specifici responsabili delle reazioni. Nuovi metodi di somministrazione, come i trattamenti orali, potrebbero migliorare la tolleranza dei cani alle proteine allergeniche. I progressi compiuti nell’uomo potrebbero essere fonte di ispirazione per adattare questi approcci nel contesto della DAC.
ASIT a fronte dei nuovi trattamenti
Infine, è importante ricordare che, di fronte all’efficacia di nuovi trattamenti come la ciclosporina, l’oclacitinib o gli anticorpi monoclonali anti-IL-31, il ruolo dell’ASIT nel trattamento multimodale delle allergie canine richiede una riflessione costante. Tuttavia, l’ASIT rimane l’unica terapia in grado di modificare o invertire almeno una parte della patogenesi e di offrire la prospettiva di una guarigione definitiva. È quindi essenziale che l’ASIT sia considerata non come un trattamento di ultima istanza, ma come un’opzione terapeutica attuabile in prima linea. L’ASIT può essere un’opzione terapeutica di elezione in prima istanza, in particolare nei cani che non rispondono bene ai trattamenti farmacologici convenzionali, o in quelli che presentano effetti indesiderati a tali farmaci. La combinazione dell’ASIT con altri trattamenti può migliorare l’efficacia complessiva del trattamento della DAC. È importante tenere conto del profilo di sicurezza e dell’efficacia relativa dei diversi trattamenti disponibili.
Confronto con trattamenti alternativi: La ciclosporina, l’oclacitinib e gli anticorpi monoclonali anti-IL-31 sono trattamenti efficaci per alleviare i sintomi della DAC, ma non modificano la patogenesi della malattia e la loro somministrazione a lungo termine è necessaria. L’ASIT, d’altra parte, mira alla causa profonda dell’allergia, modificando la risposta immunitaria del cane. Sebbene l’ASIT possa richiedere tempo per produrre un effetto, offre una prospettiva di guarigione completa, in contrasto con i trattamenti sintomatici. L’uso combinato di ASIT e trattamenti sintomatici è un approccio possibile.
Conclusione e prospettive
In conclusione, sebbene l’ASIT sia un’opzione terapeutica promettente per la dermatite atopica canina, la sua efficacia deve ancora essere formalmente dimostrata da studi clinici rigorosi e più standardizzati. I meccanismi d’azione rimangono enigmatici e sono necessarie ulteriori vie di indagine. Studi più numerosi e più rigorosi sono essenziali per colmare le attuali lacune nelle conoscenze. In particolare, è necessario capire meglio i meccanismi d’azione, determinare i parametri ottimali di trattamento e identificare biomarcatori affidabili per valutare l’efficacia e prevedere la risposta.
Gli studi futuri devono concentrarsi su:
- Identificazione precisa degli allergeni canini: Sviluppo di test diagnostici più precisi e standardizzati al fine di identificare gli allergeni coinvolti.
- Ottimizzazione dei protocolli di somministrazione: Standardizzazione dei protocolli e confronto dei diversi metodi di somministrazione (SCIT, SLIT, RIT, ILIT). Sono necessari studi comparativi rigorosi.
- Identificazione di biomarcatori predittivi del successo terapeutico: Determinare i marcatori che consentono di prevedere la risposta al trattamento prima della sua somministrazione. Ciò consentirà di personalizzare il trattamento.
- Esplorazione delle preparazioni allergeniche modificate: Testare gli allergeni ricombinanti, i peptidi e gli allergoidi. Queste formulazioni più pure potrebbero migliorare la sicurezza e l’efficacia.
- Strategie immunomodulatorie: Testare l’uso di immunomodulatori per influenzare la risposta immunitaria e ottimizzare la tolleranza.
- Studi a lungo termine: Valutare gli effetti a lungo termine dei diversi protocolli, al fine di comprendere meglio la durata dell’efficacia del trattamento.
L’ASIT potrebbe così diventare un trattamento di prima linea nella gestione della DAC, invece di rimanere confinata a un’opzione di secondo piano. Il miglioramento dei protocolli, la standardizzazione e lo sviluppo di nuovi strumenti diagnostici e terapeutici consentiranno di fare dell’ASIT uno strumento di scelta nel trattamento della dermatite atopica canina.
Domande Frequenti (FAQ)
D1: Quali sono i limiti dei test intradermici e sierologici per la diagnosi della DAC?
I test intradermici (IDT) e i test sierologici per la determinazione delle IgE specifiche per l’allergene (ASIS) presentano delle limitazioni. Gli IDT non misurano la sensibilità di tutti i percorsi allergici e sono descritte reazioni falsamente positive nei cani non allergici. Le reazioni falsamente positive sono più numerose per concentrazioni più elevate, e i risultati positivi possono essere legati a una sensibilità non specifica delle IgE (reazioni crociate con altri allergeni). Gli ASIS misurano solo le IgE circolanti specifiche per l’allergene e non tengono conto di altre vie allergiche, e sono state osservate anche reazioni falsamente positive. Inoltre, entrambi i test mancano di standardizzazione e sono possibili risultati falsi positivi e falsi negativi. La sensibilità può variare da un laboratorio all’altro.
Si stima che tra il 10 e il 30% dei cani affetti da DAC clinicamente confermata possano mostrare un IDT negativo, a causa di diversi fattori come la tecnica, la concentrazione di allergeni, le interferenze farmacologiche, i fattori intrinseci dell’ospite o una scelta imprecisa degli allergeni. I limiti dei test intradermici includono anche la necessità di una preparazione specifica del cane (tosatura, ecc.), il rischio di reazioni locali e la soggettività dell’interpretazione dei risultati. I test sierologici (ASIS) evitano questi inconvenienti, ma presentano limiti in termini di sensibilità e specificità; reazioni positive possono essere osservate in cani non allergici.
Alla fine, questi test allergologici sono utili solo per la determinazione degli allergeni da includere nella desensibilizzazione e in nessun caso per la diagnosi della dermatite atopica canina.
D2: Come scegliere gli allergeni per un protocollo di ASIT?
La scelta degli allergeni per un protocollo di ASIT deve basarsi sull’anamnesi clinica dell’animale, in associazione con le reazioni positive ai test intradermici o sierologici. Non bisogna però fidarsi solo dei test, poiché reazioni positive possono essere osservate in cani sani, e le reazioni non riflettono necessariamente un’ipersensibilità clinica. Un’attenta interpretazione della storia clinica e la correlazione con i risultati dei test consentono di identificare gli allergeni pertinenti per l’istituzione del protocollo terapeutico. In alcuni casi, potrebbero essere considerati test di provocazione.
D3: Quali sono i vantaggi e gli svantaggi dell’immunoterapia accelerata (RIT)?
L’immunoterapia accelerata (RIT) riduce la durata dell’induzione rispetto all’immunoterapia convenzionale. Nel cane, la RIT è ben tollerata, gli effetti collaterali maggiori sono rari, ed è soprattutto associata al prurito. Tuttavia, richiede un monitoraggio clinico ospedaliero, e questo tipo di approccio comporta maggiori rischi per la sicurezza, oltre a un costo più elevato. La RIT può essere considerata nei cani in cui il rischio di anafilassi è basso, consentendo di guadagnare tempo se la tolleranza è buona. L’ottimizzazione dei protocolli richiederà una valutazione più approfondita per identificare i parametri di sicurezza ottimali ed evitare reazioni avverse. È necessario il confronto tra RIT classica.
D4: Quali sono le nuove prospettive di ricerca sull’ASIT canina?
Diversi assi di ricerca meritano di essere esplorati: l’uso di preparazioni allergeniche modificate (allergoidi, allergeni ricombinanti, peptidi), lo sviluppo di nuovi adiuvanti per migliorare l’efficacia e la sicurezza del trattamento, l’identificazione di biomarcatori di successo terapeutico e la standardizzazione dei protocolli. Anche l’esplorazione di tecniche di somministrazione innovative, come l’immunoterapia intralinfatica, epicutanea o l’somministrazione orale, è promettente. La ricerca sull’ASIT canina è un campo in costante sviluppo, e nuove piste di ricerca vengono sempre esplorate. Uno sforzo di standardizzazione per migliorare l’affidabilità degli studi è fondamentale.
D5: Esistono interazioni farmacologiche da considerare prima di eseguire test cutanei?
La somministrazione di farmaci può influenzare i risultati degli IDT. Alcuni farmaci, come gli antistaminici, i glucocorticoidi, la ciclosporina e gli antidepressivi triciclici, possono interferire con gli IDT. Potrebbe essere necessario un periodo di sospensione di alcuni farmaci prima di eseguire un IDT. Le potenziali interazioni farmacologiche devono essere prese in considerazione prima dell’inizio del trattamento. L’effetto dei farmaci deve essere considerato prima dell’esecuzione dei test. Una discussione con il veterinario è essenziale per determinare la potenziale sospensione di alcuni farmaci prima dell’esecuzione dei test. È necessario considerare una potenziale interazione con il farmaco utilizzato nel trattamento della malattia.
Riferimenti
Hensel P, Santoro D, Favrot C, Hill P, Griffin C. Canine atopic dermatitis: detailed guidelines for diagnosis and allergen identification. BMC Veterinary Research 2015; 11:196. DOI: 10.1186/s12917-015-0515-5.
Mueller RS. Update on Allergen Immunotherapy. Vet Clin Small Anim 2019; 49: 1–7. DOI: 10.1016/j.cvsm.2018.08.001.
DeBoer DJ. The future of immunotherapy for canine atopic dermatitis: a review. Vet Dermatol 2017; 28: 25–66. DOI: 10.1111/vde.12416.
Pinto MSN, Gil SJRC, Ramió-Lluch L, et al. Challenging the norm: Epicutaneous immunotherapy for canine atopic dermatitis. Allergy 2023; 78: 255–257. DOI: 10.1111/all.15946.
Ricerche correlate
trattamento dermatite atopica cane, dermatite atopica, dermatite, cani, atopica nel cane, nel cane, dermatite atopica nel, malattia genetica, dermatite atopica canina, animale, trattamento, malattia, pelle, allergia, qualcosa, barriera cutanea, prurito, lesioni, gatto, test, acari, in un cane, desensibilizzazione, pollini, prurito, acidi grassi essenziali, durata, vaccino, vita, schema, allergeni, muffe, rafforzare la barriera cutanea, dac, dermatite, effetti collaterali, acidi grassi, atopica, proprietario, malattie, sintomi, gestione, sostanze, umani, sistema immunitario, pulci, golden retriever, cause, scopo, regola, età, jack russel terrier, punture, razze, salute, patologia, carico, allergologia, effetto, infiammazione, barriera, microrganismi, forma, shar peï, arrossamenti, casi, origine, funzione, punture di pulci, riacutizzazioni, predisposizione, fase, compagno