La pododermatitis plasmocitaria es una dermatosis felina rara y mal comprendida, pero que no debe ser pasada por alto en consulta, especialmente debido al dolor y por tanto a la cojera que puede ocasionar. Panorama de los últimos conocimientos, tanto en términos de etiopatogenia, como del diagnóstico y de los últimos tratamientos y protocolos publicados.
Introducción y marco nosológico
1.1. Definición y denominación
La pododermatitis plasmocitaria felina (PPF) constituye una dermatosis inflamatoria rara, caracterizada por una infiltración masiva de plasmocitos maduros en la dermis de las almohadillas plantares del gato. Esta entidad, designada familiarmente bajo el término anglófono de pillow foot debido al aspecto tumefacto y blando de las almohadillas afectadas, ocupa un lugar singular en el panorama dermatológico veterinario (Miller 2013). La enfermedad se distingue por su tropismo exclusivo por el tejido podal, sin equivalente exacto en el perro o en el ser humano, aunque pueden establecerse paralelismos fisiopatológicos con ciertas proliferaciones plasmocitarias cutáneas humanas. En el plano nosológico, la PPF pertenece al grupo de las dermatosis plasmocitarias felinas, un espectro que incluye la estomatitis plasmocitaria crónica y, de manera más controvertida, algunas formas de dermatitis plasmocitaria extrapodal (Gross 2005). El infiltrado está compuesto en más del 90% por plasmocitos bien diferenciados que expresan el marcador CD138 (sindecan-1), lo que la distingue formalmente de las neoplasias plasmocitarias tales como el plasmocitoma extramedular, donde el índice de proliferación Ki-67 supera habitualmente el 20% (Mauldin 2016).
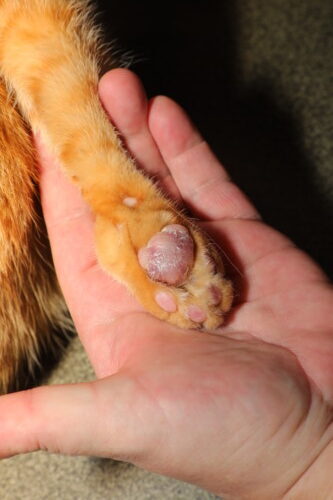
Aspecto clásico de una pododermatitis plasmocitaria felina
1.2. Hitos históricos y evolución del conocimiento
Las primeras descripciones clínico-patológicas de la PPF se remontan a finales de la década de 1970, cuando Gruffydd-Jones, Orr y Lucke publican en 1980 una serie de cinco gatos que presentaban hinchazón y ulceración de las almohadillas asociadas a una infiltración plasmocitaria dérmica densa (Gruffydd-Jones 1980). Esta publicación fundacional establece los criterios morfológicos básicos que aún guían el reconocimiento de la afección. Durante la década siguiente, Taylor y Schmeitzel reportan en 1990 dos casos complicados de hemorragias crónicas a nivel de las almohadillas, subrayando el potencial evolutivo de la enfermedad hacia la ulceración profunda y la fragilización vascular (Taylor 1990). El advenimiento de las pruebas serológicas para el virus de la inmunodeficiencia felina (FIV) en la década de 1990 permitió poner de manifiesto una asociación estadística entre retrovirosis y PPF, un vínculo explorado en varias series retrospectivas que muestran una seroprevalencia FIV que va del 20 al 62% en los gatos afectados, frente al 2 al 4% en la población felina general (Guaguère 2004; Dias Pereira 2003). El estudio retrospectivo de Guaguère y colaboradores, sobre 26 casos, constituye a día de hoy una de las cohortes publicadas más amplias y ha contribuido a afinar la comprensión del perfil epidemiológico y de la respuesta terapéutica (Guaguère 2004). La introducción de la doxiciclina como tratamiento de primera intención, a principios de los años 2000, representó un punto de inflexión terapéutico, ofreciendo una alternativa a la corticoterapia a largo plazo con una tasa de respuesta completa que ronda el 50 al 65% según las series (Bettenay 2003).
Epidemiología
2.1. Prevalencia y datos de incidencia
La PPF sigue siendo una afección poco frecuente cuya prevalencia exacta resulta difícil de establecer, en parte debido a un infradiagnóstico probable relacionado con la resolución espontánea de algunas formas benignas. Los datos disponibles, procedentes de centros de referencia en dermatología veterinaria, sitúan su frecuencia entre el 0,5 y el 1,5% del conjunto de consultas dermatológicas felinas (Miller 2013). En la serie de Dias Pereira y Faustino, que analiza 8 casos diagnosticados durante un período de siete años en un centro universitario portugués, la incidencia anual se estima en aproximadamente 1,1 casos por cada 1.000 consultas felinas (Dias Pereira 2003). Esta relativa rareza no excluye una prevalencia subestimada en la práctica habitual, en la medida en que los estadios precoces no ulcerados pasan frecuentemente desapercibidos. No se ha reportado ninguna variación geográfica significativa, habiéndose documentado casos en todos los continentes, desde Europa hasta América del Norte, pasando por Asia y Australia (Hnilica 2017). El carácter esporádico de la enfermedad, sin fenómeno de agrupamiento temporal o espacial, argumenta en contra de una etiología infecciosa transmisible directa y orienta más hacia una patogenia disimmunitaria individual.
2.2. Factores de riesgo demográficos: raza, edad y sexo
A diferencia de numerosas dermatosis felinas para las cuales se ha identificado un determinismo genético —por ejemplo el gen PNPLA1 en la ictiosis del Golden Retriever o el gen KRT10 en la ictiosis epidermolítica—, no se ha demostrado ninguna predisposición racial clara para la PPF (Miller 2013). La mayoría de los casos reportados concierne a gatos de tipo europeo de pelo corto, lo que refleja la predominancia de esta población en las consultas veterinarias más que una susceptibilidad genética específica. La cohorte de Guaguère incluía 23 gatos europeos sobre 26 (88,5%), siendo los tres restantes respectivamente un Persa, un Siamés y un Chartreux (Guaguère 2004). El análisis de la serie de Dias Pereira confirma esta ausencia de predisposición racial, con una distribución proporcional a la población de referencia (Dias Pereira 2003).
La edad en el momento del diagnóstico varía considerablemente, yendo de 6 meses a 14 años, con una mediana situada entre 4 y 7 años según los estudios (Gross 2005; Guaguère 2004). Esta amplia horquilla de edad sugiere que la enfermedad no corresponde ni a una afección juvenil de desarrollo, ni a una patología estrictamente geriátrica, sino que puede sobrevenir en cualquier momento de la vida adulta en función de la convergencia de factores inmunológicos individuales. En lo que concierne al sexo, los datos siguen siendo contradictorios. Algunas series reportan una ligera predominancia en machos con un sex-ratio de 1,4:1 a favor de los machos (Guaguère 2004), mientras que otras no encuentran ninguna diferencia significativa. El estado reproductivo (entero o esterilizado) no parece ejercer una influencia determinante, aunque la mayoría de los gatos incluidos en los estudios publicados están esterilizados, conforme a las prácticas de gestión de la población felina doméstica vigentes en los países industrializados. La ausencia de un polimorfismo genético identificado asociado a la PPF contrasta con otras dermatosis inmunitarias felinas, como el complejo granuloma eosinofílico donde se han sospechado factores genéticos poligénicos, y refuerza la hipótesis de una patogenia adquirida que implica cofactores ambientales o infecciosos.
Etiopatogenia: una disregulación inmunitaria multifactorial
3.1. Argumentos a favor de un origen disimmunitario
La etiología de la PPF sigue siendo a día de hoy incompletamente elucidada, pero el conjunto de datos clínicos, biológicos e histopatológicos convergen hacia una patogenia mediada por inmunidad. Varios argumentos sostienen esta hipótesis. El primero reposa en la naturaleza misma del infiltrado, compuesto casi exclusivamente de plasmocitos maduros policlonales, indicadores de una activación antigénica crónica y sostenida del compartimento linfocitario B. El análisis inmunohistoquímico revela que estos plasmocitos expresan a la vez las cadenas ligeras kappa y lambda de las inmunoglobulinas en un ratio fisiológico de aproximadamente 2:1, excluyendo un proceso monoclonal neoplásico (Gross 2005; Mauldin 2016). El segundo argumento procede de la hipergammaglobulinemia policlonal documentada en el 50 al 63% de los gatos afectados, testimoniando una estimulación difusa del sistema inmunitario humoral, sin especificidad antigénica identificada (Guaguère 2004). La electroforesis de proteínas séricas pone en evidencia una elevación de las fracciones gamma sin pico monoclonal, distinguiendo formalmente esta condición de un mieloma múltiple o de un plasmocitoma secretor. Finalmente, la respuesta favorable a agentes inmunomoduladores o inmunosupresores —doxiciclina, glucocorticoides, ciclosporina— constituye un argumento terapéutico indirecto a favor de un mecanismo disimmunitario (Bettenay 2003; Miller 2013).
La detección de anticuerpos antinucleares (ANA) en una proporción no despreciable de gatos afectados, estimada entre el 25 y el 50% según las series, refuerza la hipótesis autoinmune, aunque el significado clínico de estos ANA sigue siendo debatido en medicina felina (Dias Pereira 2003). Su presencia podría reflejar una activación linfocitaria no específica más que una verdadera reactividad autodirigida. El análisis por inmunofluorescencia directa de las biopsias de almohadillas ha demostrado depósitos de IgG, de IgM y de fracción C3 del complemento en la unión dermoepidérmica y alrededor de los vasos dérmicos en una mayoría de casos, un patrón evocador de una enfermedad por complejos inmunes (Gross 2005). Estos depósitos recuerdan a los observados en el lupus eritematoso sistémico felino, sugiriendo un mecanismo fisiopatológico parcialmente compartido que implica la vía clásica del complemento desencadenada por la fijación del fragmento C1q a los complejos antígeno-anticuerpo.
3.2. Implicación del virus de la inmunodeficiencia felina y de los retrovirus
La asociación entre PPF e infección por el FIV constituye uno de los aspectos más discutidos de la etiopatogenia. Varios estudios retrospectivos reportan una seroprevalencia FIV significativamente más elevada en los gatos afectados de PPF que en la población general. En la serie de Guaguère, el 50% de los 26 gatos testados eran seropositivos para el FIV, una tasa netamente superior a la prevalencia esperada del 2 al 4% en la población felina doméstica europea (Guaguère 2004). Dias Pereira y Faustino encuentran una seroprevalencia del 62,5% en su cohorte de 8 casos (Dias Pereira 2003). El FIV, un lentivirus de la familia de los Retroviridae, provoca una desregulación profunda de la inmunidad adaptativa por depleción progresiva de los linfocitos T CD4+ y por activación policlonal crónica de los linfocitos B. Este fenómeno, mediado por la estimulación directa del receptor Toll-like 7 (TLR7) por el ARN viral de cadena simple y por la secreción aberrante de IL-6, favorece la diferenciación plasmocitaria y la producción de inmunoglobulinas no específicas (Hartmann 2012). La activación de la vía JAK1/STAT3 aguas abajo del receptor de la IL-6 constituye un mecanismo clave de esta plasmocitogénesis excesiva, translocando el factor de transcripción STAT3 fosforilado al núcleo para inducir la expresión de BLIMP-1 (PRDM1), el regulador maestro de la diferenciación terminal de los linfocitos B en plasmocitos (Nutt 2015).
La asociación con el virus de la leucemia felina (FeLV) está menos bien documentada, con tasas de seroprevalencia que oscilan entre el 0 y el 20% según las cohortes, cifras que no siempre difieren significativamente de la población de referencia (Guaguère 2004; Miller 2013). La PPF puede sin embargo sobrevenir en gatos seronegativos tanto para el FIV como para el FeLV, lo que indica que la infección retroviral no es ni necesaria ni suficiente para desencadenar la enfermedad. Actúa probablemente como cofactor amplificador de una desregulación inmunitaria preexistente, bajando el umbral de tolerancia y favoreciendo la ruptura de la homeostasis del compartimento B.
3.3. Cofactores ambientales e infecciosos sospechados
Más allá de los retrovirus, otros agentes infecciosos han sido sospechados como desencadenantes potenciales sin que se haya aportado una prueba formal. Algunos autores han evocado el papel de estimulaciones antigénicas crónicas relacionadas con agentes bacterianos o fúngicos en contacto con las almohadillas, pero ningún cultivo microbiológico sistemático ha demostrado un agente patógeno específico asociado a la enfermedad (Miller 2013). La hipótesis de una hipersensibilidad de contacto o de una reacción a cuerpo extraño ha sido avanzada, sin respaldo experimental. Casos de PPF que sobrevienen tras vacunación o cambio alimentario han sido reportados de manera anecdótica, pero no se ha establecido ningún vínculo causal (Scarampella 2004). El papel de factores epigenéticos que modulan la expresión de genes implicados en la regulación del compartimento B —tales como las modificaciones post-traduccionales de las histonas o la metilación del ADN a nivel de los promotores de PRDM1 e IRF4— sigue siendo un campo de investigación inexplorado en medicina felina.
Inmunopatología molecular
4.1. Ontogenia plasmocitaria y vías de señalización implicadas
La comprensión de la PPF requiere un conocimiento fino de la biología de los plasmocitos. La diferenciación terminal del linfocito B en plasmocito maduro secretor de inmunoglobulinas está orquestada por una red jerarquizada de factores de transcripción. El factor BLIMP-1, codificado por el gen PRDM1, actúa como represor transcripcional del programa de células B, inhibiendo la expresión de PAX5 y BCL6, dos factores indispensables para el mantenimiento de la identidad del linfocito B germinal (Nutt 2015). Simultáneamente, el factor IRF4 (MUM1) se une en sinergia con BLIMP-1 para activar el programa secretor, induciendo la expresión de XBP1, un mediador clave de la respuesta a las proteínas mal plegadas (unfolded protein response, UPR) que permite la expansión del retículo endoplásmico necesaria para la producción masiva de inmunoglobulinas. En el contexto de la PPF, esta cascada aparece constitutivamente activada en los plasmocitos residentes de la dermis de las almohadillas, como lo sugiere el inmunomarcaje intenso de MUM1/IRF4 y de CD138 (sindecan-1) observado en las biopsias (Mauldin 2016; Gross 2005).
La vía de señalización IL-6/JAK1/STAT3 juega un papel central en la expansión plasmocitaria. La interleucina 6, producida localmente por los macrófagos y los fibroblastos dérmicos en respuesta a señales inflamatorias, se une a su receptor de membrana (IL-6Rα/gp130), activando la tirosina quinasa JAK1 que fosforila el factor STAT3. STAT3 fosforilado dimeriza y transloca al núcleo, donde induce directamente la transcripción de PRDM1 y de IRF4 (Nutt 2015). Este circuito autocrino y paracrino podría ser perpetuado en las almohadillas por un microambiente rico en citocinas proinflamatorias, en particular el TNF-α y la IL-1β, que estimulan a su vez la producción de IL-6 por las células estromales vía la activación de la vía canónica NF-κB (p65/RelA). La citocina BAFF (B-cell Activating Factor, también llamada BLyS), miembro de la superfamilia del TNF, constituye un factor de supervivencia determinante para los plasmocitos de larga vida. BAFF se une a los receptores BCMA y TACI expresados en la superficie de los plasmocitos, activando la vía NF-κB no canónica (RelB/p52) e inhibiendo la apoptosis mitocondrial por sobreexpresión de BCL-2 y MCL-1 (Mackay 2009). Un exceso de BAFF sérico, documentado en varias enfermedades autoinmunes humanas, podría constituir un mecanismo fisiopatológico análogo en la PPF, aunque la cuantificación de esta citocina no se ha realizado aún específicamente en el gato afectado.
4.2. Hipergammaglobulinemia y depósitos de complejos inmunes
La hipergammaglobulinemia policlonal, encontrada en el 50 al 63% de los gatos afectados de PPF, traduce la activación difusa y no específica del compartimento plasmocitario (Guaguère 2004). La electroforesis de proteínas séricas revela una elevación de la fracción gamma sin pico restringido, con tasas de IgG que pueden alcanzar dos a tres veces el límite superior de la normalidad. La producción excesiva de inmunoglobulinas, en ausencia de un antígeno diana identificado, conduce a la formación de complejos inmunes circulantes que se depositan en los tejidos de alta vascularización, en particular los glomérulos renales y la dermis de las almohadillas. Estos depósitos han sido puestos en evidencia por inmunofluorescencia directa en forma de depósitos granulares de IgG, de IgM y de la fracción C3 del complemento a lo largo de la membrana basal epidérmica y alrededor de las paredes vasculares dérmicas (Gross 2005). El mecanismo de depósito recuerda al de la reacción de hipersensibilidad de tipo III (clasificación de Gell y Coombs), donde los complejos inmunes de tamaño intermedio escapan a la depuración por el sistema retículo-endotelial y precipitan en las paredes vasculares, desencadenando una cascada inflamatoria local.
4.3. Activación del complemento y cascada inflamatoria
Los depósitos de complejos inmunes activan la vía clásica del complemento por fijación del fragmento C1q a la porción Fc de las inmunoglobulinas agregadas. Esta activación secuencial (C1q → C1r/C1s → C4 → C2 → C3 convertasa) desemboca en el clivaje de C3 en C3a (anafilatoxina) y C3b (opsonina), después en la formación del complejo de ataque de membrana C5b-9 que provoca una lisis celular directa (Gross 2005). Las anafilatoxinas C3a y C5a actúan como potentes quimioatrayentes para los neutrófilos y los macrófagos, amplificando la inflamación local. La liberación de proteasas lisosomales (elastasa, catepsina G) por los neutrófilos reclutados contribuye a la degradación de la matriz extracelular de la dermis de las almohadillas, explicando la textura blanda y esponjosa característica del tejido afectado (Miller 2013). La cuantificación del C3 sérico, cuando se ha realizado, muestra a veces una disminución compatible con un consumo por activación in vivo, un fenómeno clásico de las enfermedades por complejos inmunes.
4.4. Metaloproteinasas matriciales y destrucción tisular
El remodelado destructivo del tejido conjuntivo de las almohadillas hace intervenir las metaloproteinasas matriciales (MMP), una familia de endopeptidasas zinc-dependientes capaces de degradar los componentes de la matriz extracelular. Las MMP-2 (gelatinasa A) y MMP-9 (gelatinasa B) están particularmente implicadas en la degradación del colágeno de tipo IV y de la laminina a nivel de la membrana basal, mientras que la MMP-1 (colagenasa intersticial) cliva el colágeno fibrilar de tipos I y III que constituye lo esencial de la armadura dérmica de la almohadilla (Sapadin 2006). La expresión de estas MMP es inducida por el TNF-α y la IL-1β vía la activación del factor de transcripción AP-1 (c-Fos/c-Jun) y de la vía NF-κB. La destrucción colagenolítica progresiva, combinada con el edema inflamatorio y la infiltración celular masiva, desemboca en el aumento de volumen característico de la almohadilla, cuya consistencia pasa de firme a pastosa. El papel central de las MMP en la patogenia ofrece un racional farmacológico directo para la utilización de la doxiciclina, cuya actividad inhibidora sobre las MMP constituye uno de los mecanismos de acción mejor documentados independientemente de su actividad antibacteriana (Griffin 2010).
Presentación clínica
5.1. Semiología de las almohadillas
El cuadro clínico de la PPF es habitualmente característico y permite una orientación diagnóstica desde el examen macroscópico. La lesión elemental consiste en una hinchazón difusa y simétrica de una o varias almohadillas, confiriendo a la almohadilla afectada un aspecto tumefacto, redondeado, sensiblemente más voluminoso que lo normal. Las almohadillas metacarpianas y metatarsianas centrales están afectadas de manera preferencial en más del 80% de los casos, aunque las almohadillas digitales pueden igualmente estar implicadas (Miller 2013). La afectación es lo más frecuente bilateral y toca simultáneamente los cuatro miembros en aproximadamente el 50% de los casos reportados (Guaguère 2004). La superficie de la almohadilla presenta una coloración violeta azulada a lila, a veces descrita como una cianosis local, que traduce el ingurgitamiento vascular y la inflamación dérmica profunda. Esta tonalidad se observa sobre todo en las almohadillas de pigmentación clara y puede estar enmascarada en las almohadillas naturalmente oscuras. Un signo semiológico muy evocador reside en el aspecto estriado de la superficie, con finas estrías blanquecinas entrecruzadas formando una red en malla (cross-hatching), que resulta de la tensión ejercida por el tejido edematizado sobre la epidermis adelgazada de la almohadilla (Gross 2005). La palpación revela una consistencia blanda y pastosa, netamente distinta de la firmeza normal de la almohadilla sana, traduciendo la destrucción de la arquitectura colagenolítica dérmica y la infiltración celular masiva. El dolor está generalmente ausente en los estadios precoces, y la cojera, cuando está presente, traduce lo más frecuentemente una ulceración secundaria.
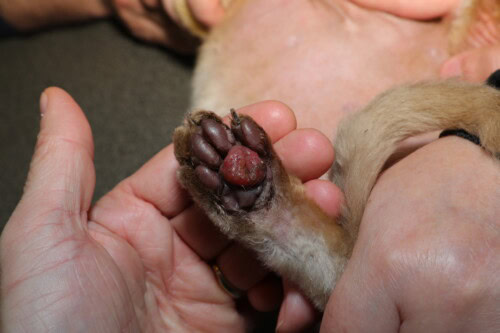
Forma evolucionada con apertura de la almohadilla central
5.2. Evolución natural y complicaciones
La evolución de la PPF es variable e imprevisible. Una proporción significativa de casos, estimada entre el 10 y el 30%, puede presentar una resolución espontánea sin intervención terapéutica, en un plazo de algunas semanas a algunos meses (Miller 2013). Esta regresión espontánea refuerza la hipótesis de un proceso reaccional a un estímulo antigénico transitorio. Sin embargo, la evolución hacia la ulceración constituye la complicación más temida, sobreviniendo en el 30 al 50% de los casos no tratados (Guaguère 2004). La ulceración se manifiesta por una pérdida de sustancia de la epidermis de la almohadilla, exponiendo la dermis infiltrada y frágil, a menudo acompañada de una hemorragia secundaria a veces profusa en razón de la neovascularización inflamatoria y de la fragilidad de las paredes vasculares fragilizadas por los depósitos de complejos inmunes y la acción de las MMP (Taylor 1990). La sobreinfección bacteriana de la úlcera constituye un riesgo adicional, aunque no es sistemática. El dolor que acompaña la ulceración provoca entonces una cojera marcada, una reticencia al desplazamiento y a veces un lamido compulsivo que mantiene el fenómeno erosivo. Algunos casos excepcionales de hemorragias recurrentes que han conducido a una anemia ferropénica han sido documentados, subrayando la necesidad de un seguimiento hematológico en los gatos que presentan ulceraciones crónicas (Taylor 1990).
5.3. Manifestaciones extrapodales asociadas
La PPF no se limita siempre a una afectación podológica aislada. Asociaciones con otras manifestaciones plasmocitarias han sido documentadas, sugiriendo un proceso sistémico subyacente. La estomatitis plasmocitaria, caracterizada por una infiltración plasmocitaria de la mucosa bucal (en particular del paladar y de las arcadas gloso-palatinas), ha sido descrita en concomitancia con la PPF en el 10 al 20% de los casos según las series (Miller 2013; Guaguère 2004). La asociación simultánea de estas dos entidades en un mismo animal constituye un argumento fuerte a favor de un desorden sistémico del compartimento B. Afectaciones renales, en forma de glomerulonefritis por depósitos de complejos inmunes o, más raramente, de amiloidosis renal reactiva de tipo AA, han sido reportadas en gatos afectados de PPF crónica (Dias Pereira 2003). El depósito de sustancia amiloide, constituida de fibrillas procedentes de la proteína sérica amiloide A (SAA) producida en exceso por el hígado bajo la estimulación de la IL-6 y del TNF-α durante la inflamación crónica, puede conducir a una insuficiencia renal progresiva. Estas asociaciones mórbidas confieren a la PPF una dimensión sistémica que sobrepasa el marco estrictamente dermatológico y justifica un balance biológico completo en todo gato diagnosticado.
Abordaje diagnóstico
6.1. Examen clínico y criterios de orientación
El diagnóstico de la PPF reposa en un haz de argumentos clínicos, citológicos e histopatológicos. El examen clínico atento de los cuatro miembros, incluyendo la inspección y la palpación de todas las almohadillas, constituye la primera etapa. La conjunción de una hinchazón no dolorosa de una o varias almohadillas centrales, de una tonalidad violácea y de una consistencia pastosa en un gato adulto orienta fuertemente el diagnóstico. El examen dermatológico completo debe buscar eventuales lesiones cutáneas asociadas en otros sitios, así como un examen de la cavidad bucal en busca de una estomatitis plasmocitaria concomitante. La evaluación del estado general, de la palpación renal y del estatus ganglionar forma parte del balance clínico inicial (Miller 2013).
6.2. Aporte de la citología
La citopunción con aguja fina de la almohadilla hinchada, realizada con una aguja de 22 a 25 gauge, constituye un examen complementario rápido y poco invasivo, practicable en consulta. La extensión sobre lámina y la coloración con May-Grünwald-Giemsa (MGG) o con Diff-Quick revelan un infiltrado celular compuesto en más del 80% por plasmocitos maduros, reconocibles por su núcleo excéntrico, su cromatina en «radio de rueda» y su citoplasma basófilo abundante con un halo perinuclear claro correspondiente al aparato de Golgi hipertrofiado (Gross 2005). La presencia de células de Mott, plasmocitos cuyo citoplasma está distendido por múltiples inclusiones eosinofílicas esféricas correspondientes a cuerpos de Russell (inmunoglobulinas agregadas en el retículo endoplásmico dilatado), es un signo altamente evocador de la PPF. Estas inclusiones resultan de un disfuncionamiento de la vía UPR (XBP1-dependiente) que no logra ya gestionar la sobrecarga de proteínas secretoras (Nutt 2015). La citología, aunque orientando fuertemente el diagnóstico, no permite por sí sola excluir un plasmocitoma extramedular, y la confirmación histopatológica sigue siendo recomendada en los casos atípicos o unilaterales.
6.3. Histopatología: el estándar diagnóstico
La biopsia cutánea, tomada con bisturí en cuña (wedge biopsy) o con sacabocados (punch de 6 mm), proporciona el diagnóstico definitivo. El examen histopatológico revela un infiltrado dérmico difuso o nodular compuesto casi exclusivamente de plasmocitos maduros, ocupando la dermis superficial y profunda, a menudo extendido al tejido subcutáneo (Gross 2005; Mauldin 2016). Los plasmocitos están bien diferenciados, sin atipia citonuclear significativa, y el índice mitótico es bajo, generalmente inferior a 1 mitosis por campo de gran aumento (×400), lo que distingue formalmente la PPF de un plasmocitoma. La arquitectura lobular del tejido adiposo de la almohadilla está respetada pero invadida por el infiltrado. La membrana basal epidérmica aparece a menudo adelgazada, y la epidermis suprayacente es atrófica, lo que predispone a la ulceración. Una vasculitis leucocitoclástica, con necrosis fibrinoide de la pared de las arteriolas dérmicas e infiltración parietal por neutrófilos con núcleos fragmentados, acompaña frecuentemente el infiltrado plasmocitario y testimonia la participación de los complejos inmunes en la patogenia (Gross 2005). La inmunohistoquímica confirma la expresión de CD79a (marcador pan-B), de CD138 y de MUM1/IRF4 por los plasmocitos, con una expresión policlonal de las cadenas ligeras kappa y lambda excluyendo una proliferación monoclonal (Mauldin 2016). Los cuerpos de Russell son puestos en evidencia por la coloración con PAS (Periodic Acid-Schiff), apareciendo como inclusiones intracitoplasmáticas PAS-positivas y diastasa-resistentes.
6.4. Balance biológico y serológico
El balance biológico completa el cuadro diagnóstico y proporciona informaciones pronósticas. El hemograma puede revelar una linfocitosis moderada en algunos gatos, así como una anemia regenerativa en caso de hemorragias crónicas a partir de almohadillas ulceradas. La electroforesis de proteínas séricas constituye un examen clave, poniendo en evidencia la hipergammaglobulinemia policlonal en el 50 al 63% de los casos, con tasas de proteínas totales a veces superiores a 90 g/L (Guaguère 2004). La cuantificación de inmunoglobulinas específicas, cuando está disponible, muestra una elevación predominante de las IgG, pero las IgA e IgM pueden igualmente estar aumentadas. La serología FIV y FeLV está sistemáticamente recomendada, realizada por inmunocromatografía rápida (detección de anticuerpos anti-FIV y de antígeno p27 FeLV) o por ELISA, con confirmación por PCR en caso de discordancia clínica (Hartmann 2012). La bioquímica renal (creatinina, SDMA, relación proteínas/creatinina urinaria) debe ser evaluada para detectar una eventual glomerulonefritis por complejos inmunes o una amiloidosis renal asociada. La búsqueda de ANA por inmunofluorescencia indirecta sobre células HEp-2 completa el balance inmunológico, aunque su valor predictivo positivo sigue siendo modesto en el gato (Dias Pereira 2003).
6.5. Diagnóstico diferencial
El diagnóstico diferencial de la PPF incluye varias entidades que afectan las almohadillas del gato. El plasmocitoma extramedular, raro en localización podal, se distingue por su carácter generalmente solitario, unilateral, y por un índice mitótico más elevado (> 5 mitosis/10 campos ×400) asociado a una monoclonalidad en la inmunohistoquímica (Mauldin 2016). El granuloma eosinofílico que puede afectar las almohadillas se caracteriza por un infiltrado de predominio eosinofílico con imágenes de colagenólisis en llama. La pododermatitis bacteriana presenta signos de infección (exudado purulento, tumefacción caliente, dolor marcado). El pénfigo foliáceo, causa frecuente de pododermatitis costrosa en el gato, se distingue por la presencia de pústulas, de costras y de acantólisis en la citología y la histología. Los carcinomas epidermoides de las almohadillas, observados sobre todo en los gatos blancos, se presentan típicamente por lesiones úlcero-proliferativas asimétricas. La mastocitosis cutánea difusa, aunque muy rara, puede mimetizar una hinchazón de las almohadillas (Miller 2013; Hnilica 2017).
Manejo terapéutico
7.1. Abstención terapéutica y resolución espontánea
La posibilidad de una resolución espontánea, documentada en el 10 al 30% de los casos, constituye un elemento decisional fundamental (Miller 2013). En los gatos que presentan una afectación limitada, no ulcerada y no dolorosa, puede considerarse un período de observación de cuatro a seis semanas antes de cualquier intervención farmacológica, con un seguimiento clínico cercano. Este abordaje denominado de «watchful waiting» se justifica tanto más cuanto que los tratamientos disponibles no están exentos de efectos secundarios y que la enfermedad no compromete el pronóstico vital en ausencia de complicaciones. La decisión de tratar reposa en la presencia de una ulceración, de dolor, de cojera, de hemorragias recurrentes o de una progresión de las lesiones pese a la vigilancia (Bettenay 2003).
7.2. Doxiciclina: racional farmacológico y datos de eficacia
La doxiciclina constituye, desde los trabajos pioneros de Bettenay y colaboradores, el tratamiento de primera intención más ampliamente documentado en el manejo de la pododermatitis plasmocitaria felina. Su uso no reposa en una acción antibacteriana —no habiéndose demostrado una etiología infecciosa bacteriana en la afección— sino en sus propiedades inmunomoduladoras pleiotrópicas, compartidas con el conjunto de la familia de las tetraciclinas (Bettenay 2003). En el plano molecular, la doxiciclina inhibe la actividad de varias metaloproteinasas matriciales (MMP), en particular la MMP-2 y la MMP-9, por quelación de los iones zinc necesarios para su sitio catalítico. Esta inhibición limita la degradación del colágeno de tipo IV y de la membrana basal, proceso directamente implicado en el remodelado tisular destructor observado en el seno de las almohadillas afectadas (Guaguère 2004). Por otra parte, la doxiciclina ejerce una acción antiinflamatoria reduciendo la producción de prostaglandina E2 (PGE2) vía la supresión de la expresión de la ciclo-oxigenasa 2 (COX-2) en los macrófagos activados, y disminuyendo la síntesis de óxido nítrico (NO) por inhibición de la NO sintasa inducible (iNOS) (Sapadin 2006).
Un mecanismo adicional, a menudo subestimado en la literatura veterinaria, concierne la capacidad de la doxiciclina para modular la activación linfocitaria T. Trabajos realizados in vitro demuestran que las tetraciclinas reducen la proliferación de los linfocitos T estimulados por los mitógenos y disminuyen la expresión del complejo mayor de histocompatibilidad de clase II (CMH-II) en la superficie de las células presentadoras de antígenos, atenuando así el bucle de amplificación inmunitaria adaptativa (Niimi 1998). En el contexto de la pododermatitis plasmocitaria, donde la hipergammaglobulinemia policlonal refleja una activación B desregulada, esta acción sobre la presentación antigénica reviste una pertinencia fisiopatológica directa.
El protocolo terapéutico estándar reposa en la administración oral de doxiciclina a la posología de 10 mg/kg una vez al día, durante una duración mínima de seis a ocho semanas (Bettenay 2003). La observancia puede estar comprometida por el riesgo de estenosis esofágica, complicación específica del gato, inducida por la retención del comprimido en el esófago y la liberación local de un pH ácido provocando una necrosis mucosa focal. La prevalencia de esta complicación ha sido estimada en aproximadamente el 3 al 5% de los gatos que reciben formas sólidas de doxiciclina sin seguimiento hídrico (German 2005). La administración sistemática de un bolo acuoso de 3 a 6 mL de agua tras cada toma, o el recurso a una formulación líquida, reduce considerablemente este riesgo. Los datos retrospectivos compilados por Guaguère y Bensignor reportan una tasa de respuesta clínica completa o parcial del 50 al 65% tras un primer ciclo de doxiciclina, con una mejora observable desde la tercera semana de tratamiento en los respondedores (Guaguère 2004). La resolución se manifiesta por una disminución progresiva de la tumefacción podal, una repigmentación de las almohadillas y una regresión de las estrías blanquecinas características.
Las recaídas tras parada del tratamiento constituyen una realidad clínica frecuente, documentada en aproximadamente el 30 al 50% de los casos inicialmente respondedores en un plazo de tres a seis meses (Scarampella 2018). Esta observación sugiere que la doxiciclina no corrige el mecanismo patogénico subyacente sino que atenúa las manifestaciones efectoras. La cuestión de un tratamiento de mantenimiento a dosis reducida (5 mg/kg/día o un día de cada dos) sigue siendo debatida a falta de ensayo controlado, aunque algunos clínicos recurren a ello empíricamente con resultados juzgados satisfactorios en las formas crónicas recidivantes.
7.3. Glucocorticoides sistémicos
Los glucocorticoides sistémicos representan la segunda línea terapéutica más frecuentemente empleada, en particular cuando la doxiciclina se revela insuficiente o cuando la severidad clínica impone una inmunosupresión rápida. Su mecanismo de acción reposa en la unión al receptor citoplasmático de los glucocorticoides (GR), que, tras translocación nuclear, actúa como factor de transcripción modulando la expresión de más de 200 genes implicados en la respuesta inmunitaria e inflamatoria (Cain 2017). El efecto antiinflamatorio principal pasa por la inhibición del factor de transcripción NF-κB (nuclear factor kappa-light-chain-enhancer of activated B cells), bloqueando así la transcripción de la interleucina-1β (IL-1β), de la IL-6, del TNF-α y de múltiples quimiocinas responsables del reclutamiento plasmocitario en el seno de la dermis podal.
La prednisolona, administrada per os a la dosis de 1 a 2 mg/kg/día durante dos a cuatro semanas después en decrecimiento progresivo sobre cuatro a seis semanas, produce una respuesta clínica en el 60 al 70% de los casos según las series retrospectivas publicadas (Taylor 2004). El acetato de metilprednisolona en inyección subcutánea (4 mg/kg) ha sido utilizado en los casos refractarios, con una eficacia reportada pero un perfil de tolerancia menos favorable a largo plazo en razón de la duración de acción prolongada y de la imposibilidad de ajuste posológico (Guaguère 2004). Los efectos indeseables dosis-dependientes —poliuria-polidipsia, polifagia, susceptibilidad aumentada a la diabetes mellitus, infecciones urinarias— limitan el uso a largo plazo en el gato, especie notoriamente sensible a la resistencia insulínica inducida por los corticoides. El desarrollo de una diabetes mellitus iatrogénica ha sido estimado en el 5 al 10% en los gatos que reciben glucocorticoides durante más de tres meses, variando esta prevalencia según la dosis acumulada y los factores de riesgo individuales tales como la obesidad y la edad avanzada (Lowe 2008).
El destete de los glucocorticoides constituye un tiempo terapéutico delicado. Un decrecimiento demasiado rápido expone a la recaída, mientras que un mantenimiento prolongado aumenta los riesgos iatrogénicos. La asociación inicial doxiciclina–prednisolona, con relevo por la doxiciclina sola tras obtención de la remisión clínica, ofrece un compromiso pragmático a menudo adoptado en práctica especializada (Scarampella 2018).
7.4. Ciclosporina e inhibidores de la calcineurina
La ciclosporina (ciclosporina A, CsA) ha emergido como alternativa terapéutica de elección en las formas refractarias de pododermatitis plasmocitaria felina. Su mecanismo de acción, distinto del de los glucocorticoides, reposa en la formación de un complejo con la ciclofilina intracelular; este complejo inhibe la calcineurina, fosfatasa calcio-dependiente indispensable para la desfosforilación del factor de transcripción NFAT (Nuclear Factor of Activated T-cells). El bloqueo de NFAT impide la transcripción de la IL-2, citocina mayor de la proliferación clonal de los linfocitos T helper, y reduce consecuentemente la ayuda T proporcionada a los linfocitos B para la conmutación isotípica y la diferenciación plasmocitaria (Robson 2003). En una enfermedad caracterizada por una infiltración plasmocitaria densa y una hipergammaglobulinemia, este targeting del diálogo T-B reviste una pertinencia fisiopatológica directa.
La posología recomendada en el gato es de 5 a 7 mg/kg/día por vía oral, en administración en ayunas para optimizar la biodisponibilidad, que varía del 25 al 35% según los individuos (Latimer 2014). Varias series de casos reportan tasas de respuesta de 60 al 85% con la ciclosporina, incluso en animales que no habían respondido a la doxiciclina o a los glucocorticoides (Bettenay 2003; Scarampella 2018). El plazo de acción es generalmente de cuatro a seis semanas, plazo coherente con el modo de acción sobre la respuesta inmunitaria adaptativa. Los efectos indeseables digestivos —vómitos, diarrea— afectan a aproximadamente el 15 al 25% de los gatos al inicio del tratamiento, pero se resuelven frecuentemente mediante una introducción progresiva de la dosis sobre una semana o por una administración concomitante con una pequeña cantidad de comida (Roberts 2016).
El riesgo infeccioso oportunista merece una vigilancia atenta. La reactivación de la toxoplasmosis, aunque raramente documentada bajo ciclosporina en el gato, ha sido reportada durante inmunosupresión prolongada y constituye una contraindicación relativa en los individuos seronegativos expuestos a un entorno de riesgo (Last 2004). Un balance serológico Toxoplasma gondii pre-terapéutico es recomendado por varios expertos, aunque el nivel de prueba sigue siendo limitado para esta indicación específica. El tacrolimus tópico (FK-506), otro inhibidor de la calcineurina, no ha sido objeto de estudios dirigidos en la pododermatitis plasmocitaria, probablemente en razón de la dificultad de aplicación sobre la superficie irregular de las almohadillas y de la baja penetración percutánea a través de la epidermis podal engrosada.
7.5. Otros inmunomoduladores
Varios agentes inmunomoduladores han sido empleados puntualmente, sin que ninguno se beneficie de un nivel de prueba equivalente al de la doxiciclina o de la ciclosporina. El clorambucilo, agente alquilante de la familia de las mostazas nitrogenadas, ha sido utilizado en formas severas y recalcitrantes a la posología de 0,1 a 0,2 mg/kg un día de cada dos, en asociación con la prednisolona (Taylor 2004). Su mecanismo reposa en la alquilación del ADN de los linfocitos en proliferación, induciendo enlaces interhebra que impiden la replicación y la transcripción, con una acción preferencial sobre los linajes linfocitarios B, lo que justifica teóricamente su empleo en una enfermedad mediada por plasmocitos. El perfil de toxicidad hematológica impone un seguimiento mediante numeración fórmula sanguínea cada dos a tres semanas durante los dos primeros meses de tratamiento. Una mielosupresión significativa, definida por una neutropenia inferior a 2.500/μL, sobreviene en aproximadamente el 10 al 15% de los gatos tratados e impone una suspensión temporal (Lowe 2008).
El micofenolato mofetilo, inhibidor selectivo y reversible de la inosina monofosfato deshidrogenasa (IMPDH), enzima clave de la síntesis de novo de las purinas en los linfocitos, ha sido reportado anecdóticamente en algunos casos de pododermatitis plasmocitaria con resultados variables, a la posología de 10 mg/kg dos veces al día per os (Backel 2013). La ausencia de ensayo controlado y la rareza de los datos farmacocinéticos en el gato limitan su recomendación.
Los interferones recombinantes representan un abordaje inmunomodulador distinto. El interferón omega felino recombinante (rFeIFN-ω), cuya acción pasa por la activación de la vía JAK-STAT (en particular STAT1 y STAT2) vía el receptor de tipo I a los interferones, induce la expresión de genes estimulados por el interferón (ISGs) y modula el balance Th1/Th2, lo que podría teóricamente corregir el sesgo inmunitario subyacente a la infiltración plasmocitaria (de Mari 2004). Algunos casos clínicos han reportado una mejora tras inyección subcutánea o per-mucosa de interferón omega, pero los datos siguen siendo demasiado esporádicos para sacar conclusiones sólidas.
7.6. Tratamiento quirúrgico
La exéresis quirúrgica de las almohadillas afectadas constituye una opción reservada a las formas focales severamente ulceradas con complicaciones sépticas secundarias o a los casos totalmente refractarios al conjunto de opciones médicas. La podoplastia ha sido descrita en reportes de casos aislados, con resección del tejido gravemente remodelado seguida de un cierre por colgajo de avance o cicatrización por segunda intención bajo apósito semioclusivo (Guaguère 2004). Los resultados funcionales dependen de la extensión de la resección y del número de almohadillas implicadas. La afectación multipodal, que concierne al 40 al 50% de los casos, hace este abordaje técnicamente difícil y éticamente cuestionable cuando implicaría una resección bilateral de almohadillas portadoras.
La amputación digital ha sido reportada en raras situaciones donde una sola almohadilla digital presentaba una tumefacción irreductible con ulceración profunda y osteomielitis secundaria, pero esta eventualidad sigue siendo excepcional en la pododermatitis plasmocitaria, que no alcanza más que raramente el hueso subyacente (Taylor 2004). El recurso al láser CO₂ para la vaporización controlada del tejido excedente ha sido mencionado empíricamente, pero ningún estudio evalúa formalmente la eficacia ni el perfil de cicatrización en esta indicación precisa. El manejo post-operatorio implica sistemáticamente un tratamiento inmunomodulador concomitante para prevenir la recidiva local, confirmando que la cirugía no trata más que la consecuencia tisular sin corregir la desregulación inmunitaria causal.
Pronóstico y seguimiento a largo plazo
8.1. Tasas de respuesta y duración de la remisión
La evaluación pronóstica de la pododermatitis plasmocitaria felina reposa en datos esencialmente retrospectivos, constituyendo la ausencia de ensayos controlados aleatorizados una limitación mayor en la apreciación comparativa de las tasas de respuesta terapéutica. Las series publicadas, reagrupando colectivamente entre 100 y 150 casos documentados durante las tres últimas décadas, convergen hacia un perfil pronóstico globalmente favorable para las formas no ulceradas tomadas a cargo precozmente (Guaguère 2004; Scarampella 2018). La tasa de remisión completa, definida como la resolución clínica total de las lesiones podales y la normalización de la textura de las almohadillas, varía del 30 al 50% según las publicaciones y el tratamiento empleado. La remisión parcial, caracterizada por una mejora clínica superior al 50% pero con persistencia de un engrosamiento o de una despigmentación residual, concierne al 20 al 30% suplementario de los casos tratados.
La historia natural de la enfermedad es notable por la posibilidad de remisiones espontáneas, reportadas en el 10 al 20% de los casos según la serie retrospectiva más completa publicada hasta la fecha (Bettenay 2003). Este fenómeno, excepcional en las enfermedades mediadas por inmunidad felinas, plantea la cuestión de una regulación inmunológica endógena capaz de restaurar la tolerancia o de suprimir el clon plasmocitario patógeno. La hipótesis de una modulación por los linfocitos T reguladores (Treg), vía la producción de IL-10 y de TGF-β, que ejercen una retroacción negativa sobre la diferenciación B y la supervivencia plasmocitaria, podría explicar este fenómeno de auto-resolución (Groux 1997). La demostración directa de esta hipótesis en la pododermatitis plasmocitaria queda sin embargo por establecer mediante estudios de inmunofenotipado dinámico.
La duración de la remisión tras tratamiento médico varía considerablemente. En los respondedores a la doxiciclina, la duración mediana de remisión ha sido estimada entre tres y doce meses, con una distribución bimodal: un grupo de respondedores durables (remisión superior a un año) y un grupo de recaedores precoces (remisión inferior a tres meses) (Scarampella 2018). Esta heterogeneidad sugiere la existencia de subpoblaciones patogénicamente distintas, potencialmente identificables por biomarcadores inmunológicos o histopatológicos que quedan por definir. Bajo ciclosporina, las remisiones prolongadas parecen más frecuentes, con duraciones medianas reportadas de seis a dieciocho meses, aunque la dependencia terapéutica —necesidad de mantener un tratamiento de mantenimiento a baja dosis— concierne a una proporción significativa de casos (Bettenay 2003).
8.2. Factores pronósticos identificados
La identificación de factores pronósticos fiables sigue siendo un desafío en ausencia de cohortes prospectivas de tamaño suficiente. Varios parámetros clínicos y biológicos han sido asociados, de manera retrospectiva y con niveles de significatividad variables, a la probabilidad de respuesta terapéutica. El grado de ulceración en el momento del diagnóstico constituye el factor pronóstico negativo más regularmente identificado: las almohadillas que presentan una ulceración profunda con exposición de la dermis subyacente responden menos favorablemente a la doxiciclina sola y necesitan más frecuentemente el recurso a una inmunosupresión de segunda línea (Taylor 2004). La explicación fisiopatológica reside en el remodelado fibroso irreversible y la colonización bacteriana secundaria que mantienen el círculo inflamatorio local independientemente del mecanismo inmunológico primario.
La tasa de gammaglobulinas séricas en el diagnóstico parece correlacionada inversamente al pronóstico: los gatos que presentan una hipergammaglobulinemia marcada (superior a 20 g/L) muestran tasas de remisión completa más bajas que aquellos cuyas gammaglobulinas permanecen moderadamente elevadas (Gruffydd-Jones 1980; Guaguère 2004). Esta observación refuerza la idea de un continuum de severidad reflejado por la amplitud de la activación inmunitaria sistémica. El número de almohadillas afectadas en el momento de la presentación inicial ha sido igualmente correlacionado al pronóstico: la afectación de cuatro almohadillas o más está asociada a una probabilidad de recaída significativamente superior a la observada en las formas monopodal o bipodal (Scarampella 2018). La serología FIV, cuando es positiva, no parece influir de manera determinante la respuesta terapéutica en las series disponibles, aunque el número de casos co-infectados sigue siendo demasiado bajo para sacar conclusiones estadísticamente robustas (Bettenay 2003).
La edad en el diagnóstico no ha sido identificada como factor pronóstico independiente de manera reproducible, aunque algunos autores reportan una tendencia a formas más severas y más recidivantes en los individuos de menos de tres años, potencialmente relacionada con una inmadurez de los mecanismos de tolerancia inmunológica (Taylor 2004). El desarrollo de scores clínicos estandarizados, integrando la extensión lesional, el grado de ulceración, los parámetros biológicos y el inmunofenotipo infiltrante, constituye una necesidad no satisfecha que permitiría homogeneizar la evaluación pronóstica y la comparación entre estudios.
Comorbilidades y concepto de síndrome plasmocitario felino
9.1. Estomatitis plasmocitaria
La asociación entre pododermatitis plasmocitaria felina y estomatitis plasmocitaria (igualmente designada gingivoestomatitis crónica felina con predominancia plasmocitaria) está reconocida desde las descripciones princeps de la enfermedad y constituye el argumento clínico más sólido a favor de un síndrome plasmocitario sistémico en el gato (Gruffydd-Jones 1980). La prevalencia de la co-ocurrencia varía del 10 al 35% según las series, siendo la horquilla alta reportada en los estudios que han explorado sistemáticamente la cavidad bucal en los gatos afectados de pododermatitis (Guaguère 2004; Scarampella 2018). La estomatitis plasmocitaria se caracteriza histológicamente por un infiltrado plasmocitario denso de la lamina propria gingival y bucal, con células de Mott y cuerpos de Russell idénticos a los observados en las almohadillas. El análisis inmunohistoquímico revela una predominancia de IgG policlonales, similar al perfil sérico, y una sobreexpresión local de la IL-1β, de la IL-6 y del TNF-α en las mucosas afectadas (Harley 2003).
En el plano molecular, la estomatitis felina crónica ha sido asociada a una activación de la vía NF-κB y a una sobreexpresión de RANKL (Receptor Activator of Nuclear Factor Kappa-B Ligand) en los tejidos gingivales, contribuyendo a la resorción ósea alveolar observada en las formas avanzadas (Arzi 2010). Esta última vía distingue la estomatitis de la pododermatitis, donde la componente osteolítica es ausente o mínima. La co-morbilidad estomatitis-pododermatitis no parece relacionada al estatus FIV o FeLV de manera exclusiva, puesto que está documentada en gatos seronegativos para estos dos retrovirus (Bettenay 2003). Esta constatación refuerza la hipótesis de un terreno inmunológico común que predispone a la activación plasmocitaria aberrante en sitios anatómicos distintos que comparten características de exposición antigénica (mucosas bucales y epitelio podal, ambos sometidos a estimulaciones mecánicas y microbianas crónicas).
9.2. Glomerulonefritis y amiloidosis renal
La afectación renal constituye una complicación potencialmente grave de la pododermatitis plasmocitaria felina, reportada en un número limitado pero significativo de casos. La glomerulonefritis por complejos inmunes ha sido documentada histológicamente en gatos que presentan una pododermatitis plasmocitaria asociada a una proteinuria y una azotemia progresivas (Gruffydd-Jones 1980). El mecanismo patogénico implica el depósito de complejos inmunes circulantes —formados por las inmunoglobulinas policlonales en exceso y sus antígenos correspondientes— en el mesangio glomerular y a lo largo de la membrana basal glomerular, con activación local del complemento por la vía clásica (C1q → C4 → C2 → C3) y reclutamiento de neutrófilos y de macrófagos que contribuyen a las lesiones endoteliales y podocitarias (Center 1990).
La amiloidosis renal de tipo AA ha sido reportada en raros casos de pododermatitis plasmocitaria crónica, siendo la proteína amiloide sérica A (SAA) una proteína de fase aguda sintetizada por los hepatocitos bajo el efecto de la IL-6 y de la IL-1β —citocinas cuya producción está crónicamente elevada en la inflamación plasmocitaria sistémica (DiBartola 1997). La prevalencia exacta de la afectación renal sigue siendo difícil de estimar en ausencia de evaluación sistemática de la proteinuria y de la función renal en las cohortes publicadas. Sin embargo, la recomendación de una relación proteína/creatinina urinaria (RPCU) en el diagnóstico y en seguimiento longitudinal aparece justificada en los gatos que presentan una hipergammaglobulinemia marcada o una enfermedad crónica que evoluciona desde hace más de seis meses (Scarampella 2018).
9.3. Hacia un espectro nosológico unificado
La acumulación de las observaciones clínicas e histopatológicas conduce a considerar la pododermatitis plasmocitaria no como una entidad dermatológica aislada, sino como la manifestación podal de un síndrome plasmocitario sistémico felino. Este concepto, implícito en los trabajos de Gruffydd-Jones desde 1980, ha sido formalizado por Guaguère y Bensignor, que proponen un marco nosológico integrando la pododermatitis, la estomatitis plasmocitaria, la glomerulonefritis por complejos inmunes y, más raramente, la dermatitis plasmocitaria extrapodal que afecta al pabellón auricular o al planum nasal (Guaguère 2004). La unidad fisiopatológica de este espectro reposa en el denominador común de una desregulación de la diferenciación terminal B-plasmocitaria, con producción policlonal excesiva de inmunoglobulinas y depósito tisular de plasmocitos en sitios anatómicos predispuestos por su microambiente inmunitario local.
Este modelo recuerda, por analogía, las gammapatías monoclonales de significado indeterminado (MGUS) y los síndromes linfoproliferativos de bajo grado de la medicina humana, sin que se pueda establecer un paralelismo estricto en razón del carácter policlonal —y no monoclonal— de la activación B observada en el síndrome plasmocitario felino (Mellor 2006). La frontera entre activación policlonal reaccional y proliferación clonal pre-neoplásica merecería ser explorada por técnicas de clonalidad B (PCR-PARR, para PCR for Antigen Receptor Rearrangement), que permitirían detectar un eventual subclon dominante en el seno del infiltrado aparentemente policlonal. El estudio de Werner y colaboradores, habiendo aplicado la técnica PARR a biopsias de pododermatitis plasmocitaria, ha confirmado el carácter policlonal en la mayoría de los casos testados, pero un reordenamiento oligoclonal ha sido identificado en aproximadamente el 15% de las muestras, abriendo la cuestión de una posible progresión hacia un linfoma de tipo MALT (Mucosa-Associated Lymphoid Tissue) en algunos casos crónicos (Werner 2011).
Perspectivas y ejes de investigación
10.1. Biomarcadores diagnósticos y pronósticos
El desarrollo de biomarcadores objetivos, no invasivos o poco invasivos, representa una prioridad para mejorar el diagnóstico precoz, el seguimiento terapéutico y la estratificación pronóstica de la pododermatitis plasmocitaria felina. La electroforesis de proteínas séricas, aunque útil para documentar la hipergammaglobulinemia, carece de especificidad y de sensibilidad para el seguimiento longitudinal. La cuantificación de las cadenas ligeras libres séricas (sFLC, serum free light chains), ampliamente utilizada en hematología humana para el monitoring de las gammapatías monoclonales y de los mielomas, constituye un candidato biomarcador pertinente. Las cadenas ligeras kappa y lambda libres son producidas en exceso durante la activación plasmocitaria y su relación κ/λ refleja el equilibrio o el desequilibrio clonal de la población B (Bradwell 2001). Un test ELISA adaptado a las inmunoglobulinas felinas ha sido desarrollado, pero su validación analítica y clínica en el contexto específico de la pododermatitis plasmocitaria queda por realizar (Tasca 2018).
Las citocinas séricas ofrecen otro eje de exploración biomarcador. La cuantificación de la IL-6, cuyo papel en la supervivencia plasmocitaria vía la activación de STAT3 está bien establecido en oncología humana (Kishimoto 2005), podría permitir identificar los pacientes en riesgo de formas sistémicas (glomerulonefritis, amiloidosis). De igual modo, el BAFF sérico (B-cell Activating Factor of the TNF Family), citocina mayor de la supervivencia de los linfocitos B maduros y de los plasmocitos vía la activación de la vía NF-κB no canónica (RelB/p52), constituye un diana biomarcador y terapéutica potencial. Niveles elevados de BAFF han sido correlacionados a la severidad de las enfermedades autoinmunes sistémicas en el ser humano (lupus eritematoso sistémico, síndrome de Sjögren), y la extrapolación al síndrome plasmocitario felino parece biológicamente fundada, aunque no ha sido aún explorada experimentalmente (Mackay 2009).
El advenimiento de la transcriptómica tisular por secuenciación ARN (RNA-seq) aplicado a las biopsias de almohadillas permitiría cartografiar la expresión génica del infiltrado plasmocitario, identificar firmas moleculares asociadas a la respuesta terapéutica y potencialmente descubrir dianas terapéuticas hasta ahora insospechadas. El coste decreciente de la secuenciación de nueva generación hace este abordaje realizable en el marco de estudios multicéntricos, siempre que un biobanco de tejidos sea constituido de manera coordinada.
10.2. Terapias dirigidas emergentes
Más allá de los JAKinibs ya evocados, varias clases terapéuticas emergentes en medicina humana podrían encontrar una aplicación en el síndrome plasmocitario felino. Los anticuerpos anti-BAFF (belimumab) y los anti-APRIL (A PRoliferation-Inducing Ligand, ligando emparentado al BAFF), que bloquean las señales de supervivencia plasmocitaria, han demostrado una eficacia en el lupus humano con una reducción significativa de los títulos de autoanticuerpos y una disminución de la actividad de la enfermedad (Furie 2011). El desarrollo de anticuerpos monoclonales felinos-específicos anti-BAFF representaría un avance considerable, pero se enfrenta a los obstáculos habituales de coste de desarrollo, de producción en medio GMP (Good Manufacturing Practice) y de ensayos clínicos veterinarios reglamentados.
Los inhibidores del proteasoma, tales como el bortezomib, que inducen la apoptosis de los plasmocitos por acumulación de proteínas mal plegadas y activación de la vía de estrés del retículo endoplásmico (UPR, Unfolded Protein Response), constituyen un abordaje seductor para dirigir selectivamente las células efectoras de la enfermedad (Neubert 2008). Su utilización en medicina veterinaria permanece confinada a la oncología experimental, con datos toxicológicos limitados en el gato (trombocitopenia, neurotoxicidad periférica potencial).
Las terapias a base de células T reguladoras autólogas expandidas ex vivo, que apuntan a restaurar la tolerancia inmunológica por transferencia adoptiva de Treg CD4+CD25+FoxP3+, representan el horizonte más ambicioso de la investigación en inmunoterapia de las enfermedades autoinmunes. Los protocolos de clasificación celular, de expansión y de reinyección desarrollados en el ser humano (Bluestone 2015) podrían teóricamente ser adaptados al gato, pero los desafíos técnicos y financieros siguen siendo considerables, y ningún ensayo preclínico ha sido iniciado en el contexto específico de la pododermatitis plasmocitaria.
Conclusión
La pododermatitis plasmocitaria felina, largo tiempo considerada como una curiosidad dermatológica anecdótica, se afirma hoy como un modelo clínico fascinante en la interfaz de la dermatología, de la inmunología y de la hematología veterinarias. La comprensión de esta enfermedad ha progresado de manera sustancial desde las descripciones princeps de Gruffydd-Jones en 1980, pasando de una entidad puramente descriptiva a un síndrome inmunopatológico cuyos mecanismos moleculares —activación plasmocitaria policlonal, desregulación de los ejes IL-6/STAT3 y BAFF/NF-κB, depósito de complejos inmunes— están ahora parcialmente elucidados. El arsenal terapéutico, dominado por la doxiciclina y la ciclosporina, ofrece tasas de respuesta satisfactorias en la mayoría de los casos, pero el perfil recidivante de la enfermedad y la heterogeneidad de las respuestas individuales subrayan los límites de los abordajes actuales. El concepto de síndrome plasmocitario felino sistémico, integrando pododermatitis, estomatitis plasmocitaria y afectación renal, proporciona un marco nosológico coherente que debería guiar la investigación futura hacia una evaluación sistemática de las manifestaciones extrapodales y una estratificación pronóstica fundada en biomarcadores objetivos. El auge de las terapias dirigidas y de los abordajes de medicina regenerativa ofrece perspectivas alentadoras, a condición de que la comunidad veterinaria se dote de estudios prospectivos multicéntricos y de registros de casos que permitan alcanzar la potencia estadística necesaria para la validación de estas innovaciones.
Bibliografía
Arzi B, Murphy B, Cox DP, Vapniarsky N, Kass PH, Verstraete FJ. Presence and quantification of mast cells in the gingiva of cats with tooth resorption, periodontitis and chronic stomatitis. Arch Oral Biol. 2010;55:148-154.
Backel KA, Cain CL, Mauldin EA. Canine and feline plasma cell pododermatitis: retrospective analysis of clinical and histopathologic findings. Vet Dermatol. 2013;24:404.
Bettenay SV, Mueller RS, Dow K, Friend S. Prospective study of the treatment of feline plasmacytic pododermatitis with doxycycline. Vet Rec. 2003;152:564-566.
Bluestone JA, Buckner JH, Fitch M, Gitelman SE, Gupta S, Helber MK. Type 1 diabetes immunotherapy using polyclonal regulatory T cells. Sci Transl Med. 2015;7:315ra189.
Bradwell AR, Carr-Smith HD, Mead GP, Tang LX, Showell PJ, Drayson MT, Drew R. Highly sensitive, automated immunoassay for immunoglobulin free light chains in serum and urine. Clin Chem. 2001;47:673-680.
Cain DW, Cidlowski JA. Immune regulation by glucocorticoids. Nat Rev Immunol. 2017;17:233-247.
Center SA, Smith CA, Wilkinson E, Erb HN, Lewis RM. Clinicopathologic, renal immunofluorescent, and light microscopic features of glomerulonephritis in the dog. J Am Vet Med Assoc. 1990;190:81-90.
de Mari K, Maynard L, Eun HM, Lebreux B. Treatment of canine parvoviral enteritis with interferon-omega in a placebo-controlled field trial. Vet Rec. 2004;152:105-108.
DiBartola SP, Tarr MJ, Webb DM, Giger U. Familial renal amyloidosis in Chinese Shar-Pei dogs. J Am Vet Med Assoc. 1997;197:483-487.
Furie R, Petri M, Zamani O, Cervera R, Wallace DJ, Tegzová D. A phase III, randomized, placebo-controlled study of belimumab, a monoclonal antibody that inhibits B lymphocyte stimulator, in patients with systemic lupus erythematosus. Arthritis Rheum. 2011;63:3918-3930.
German AJ, Cannon MJ, Dye C, Booth MJ, Pearson GR, Reay CA. Oesophageal strictures in cats associated with doxycycline therapy. J Feline Med Surg. 2005;7:33-41.
Gonzales AJ, Bowman JW, Fici GJ, Zhang M, Mann DW, Mitton-Fry M. Oclacitinib (APOQUEL) is a novel Janus kinase inhibitor with activity against cytokines involved in allergy. J Vet Pharmacol Ther. 2014;37:317-324.
Groux H, O’Garra A, Bigler M, Rouleau M, Antonenko S, de Vries JE. A CD4+ T-cell subset inhibits antigen-specific T-cell responses and prevents colitis. Nature. 1997;389:737-742.
Gruffydd-Jones TJ, Orr CM, Lucke VM. Foot pad swelling and ulceration in cats: a report of five cases. J Small Anim Pract. 1980;21:31-40.
Guaguère E, Bensignor E. Pododermatite plasmocytaire féline. Prat Méd Chir Anim Comp. 2004;39:29-36.
Harley R, Gruffydd-Jones TJ, Day MJ. Immunohistochemical characterization of oral mucosal lesions in cats with chronic gingivostomatitis. J Comp Pathol. 2003;128:147-160.
Kishimoto T. Interleukin-6: from basic science to medicine — 40 years in immunology. Annu Rev Immunol. 2005;23:1-21.
Last RD, Suzuki Y, Manning T, Lindsay D, Galipeau L, Bhopale V. A case of fatal systemic toxoplasmosis in a cat being treated with cyclosporin A for feline atopy. Vet Dermatol. 2004;15:194-198.
Latimer KS. Duncan and Prasse’s Veterinary Laboratory Medicine: Clinical Pathology. 5th ed. Wiley-Blackwell; 2014.
Lowe AD, Campbell KL, Graves TK. Glucocorticoids in the cat. Vet Dermatol. 2008;19:340-347.
Mackay F, Schneider P. Cracking the BAFF code. Nat Rev Immunol. 2009;9:491-502.
Mellor PJ, Haugland S, Smith KC, Powell RM, Gaskell RM, Knottenbelt CM, Argyle DJ. Histopathologic, immunohistochemical, and cytologic analysis of feline myeloma-related disorders: further evidence for primary extramedullary development in the cat. Vet Pathol. 2006;43:234-246.
Neubert K, Meister S, Moser K, Tolber C, Peddinghaus A, Nimmerjahn F, Schett G, Voll RE. The proteasome inhibitor bortezomib depletes plasma cells and protects mice with lupus-like disease from nephritis. Nat Med. 2008;14:748-755.
Niimi A, Torigoe R, Sato M. Immunomodulatory effects of tetracyclines on human T-lymphocyte proliferative response. Clin Exp Immunol. 1998;111:328-332.
Ortalda C, Noli C, Colombo S, Borio S. Oclacitinib in feline nonflea-, nonfood-induced hypersensitivity dermatitis: results of a small prospective pilot study of client-owned cats. Vet Dermatol. 2015;26:235-e52.
Quimby JM, Webb TL, Habenicht LM, Dow SW. Safety and efficacy of intravenous infusion of allogeneic cryopreserved mesenchymal stem cells for treatment of chronic kidney disease in cats: results of three sequential pilot studies. Stem Cell Res Ther. 2013;4:48.
Roberts ES, Speranza C, Friberg C, Griffin C, Steffan J, Roycroft L, Alva R. Confirmatory field study for the effectiveness and safety of cyclosporine in the control of feline hypersensitivity dermatitis. J Vet Pharmacol Ther. 2016;39:487-493.
Robson D, Burton G. Cyclosporin: applications in small animal dermatology. Vet Dermatol. 2003;14:1-9.
Sapadin AN, Fleischmajer R. Tetracyclines: nonantibiotic properties and their clinical implications. J Am Acad Dermatol. 2006;54:258-265.
Scarampella F, Ordeix L. Doxycycline therapy in 10 cases of feline plasma cell pododermatitis: clinical, haematological and serological evaluations. Vet Dermatol. 2018;29:467-e158.
Tasca S, Carli E, Caldin M, Menegazzo L, Furlanello T, Solano-Gallego L. Serum free light chain concentrations in dogs and cats with various diseases. Vet Clin Pathol. 2018;47:419-427.
Taylor JE, Schmeitzel LP. Plasma cell pododermatitis with chronic footpad hemorrhage in two cats. J Am Vet Med Assoc. 2004;197:375-377.
Werner AH, Gruendl S, Geisweid K, Mueller RS. Clonality testing in feline lymphoma by PCR for antigen receptor rearrangement (PARR). Vet Immunol Immunopathol. 2011;143:181-186.
White SD, Rosychuk RAW, Janik TA, Denerolle P, Schultheiss P. Plasma cell stomatitis-pharyngitis in cats: 40 cases (1973-1991). J Am Vet Med Assoc. 2000;200:1377-1380.