Las calcinosis cutáneas representan un desafío diagnóstico y terapéutico mayor en dermatología veterinaria canina. Estas afecciones, caracterizadas por la acumulación anormal de sales cálcicas en las estructuras dérmicas e hipodérmicas, requieren un enfoque clínico riguroso basado en una comprensión precisa de sus mecanismos fisiopatológicos distintos.
Septiembre 2025
La identificación precoz de los diferentes tipos de calcinosis y la instauración de un tratamiento adaptado condicionan directamente el pronóstico funcional y estético. Durante las últimas jornadas anuales del GEDAC, nuestro colega Vincent Bruet, presidente del GEDAC, presentó los avances recientes en la clasificación etiológica, las modalidades diagnósticas contemporáneas y las perspectivas terapéuticas emergentes, particularmente aquellas inspiradas en los protocolos desarrollados en medicina humana.
Definición y Nomenclatura de la Calcinosis Cutánea
La calcinosis cutánea se define precisamente por depósitos anormales de sales de calcio en la dermis y la hipodermis. Estas acumulaciones minerales se manifiestan clínicamente en forma de nódulos o placas induradas, presentando típicamente una coloración blanquecina característica, y son susceptibles de alterar significativamente la superficie cutánea. La clasificación moderna distingue tres entidades clínicas principales según su extensión anatómica y su presentación morfológica.
La calcinosis cutánea constituye el término genérico que engloba el conjunto de los depósitos cálcicos que afectan las estructuras cutáneas, independientemente de su localización o extensión. Esta denominación general permite identificar el proceso patológico fundamental sin prejuzgar sus características específicas.
La calcinosis circumscripta representa una forma clínica localizada, caracterizada por depósitos cálcicos circunscritos, frecuentemente observados en las regiones peri-articulares o en proximidad de las extremidades. Esta localización preferencial sugiere la intervención de factores mecánicos locales en la génesis de estas lesiones.
La calcinosis universalis constituye la forma más extensiva y severa, caracterizada por una afectación difusa que afecta no solamente las estructuras cutáneas sino también los tejidos subcutáneos, musculares y tendinosos. Esta forma sistémica se asocia generalmente a un pronóstico más reservado y requiere una toma a cargo multidisciplinar compleja.
Fundamentos Fisiopatológicos y Clasificación Moderna de las Calcinosis
La taxonomía actual de las calcinosis cutáneas se articula alrededor de cinco entidades fisiopatológicas distintas, cada una respondiendo a mecanismos biológicos específicos. Esta estratificación constituye la base de todo enfoque terapéutico racional, pues determina la orientación diagnóstica y condiciona las elecciones terapéuticas.
La calcinosis distrófica
Ocupa una posición central en dermatología veterinaria. Su desarrollo surge exclusivamente sobre tejidos previamente alterados por procesos inflamatorios, necróticos o degenerativos, en un contexto metabólico fisiológico caracterizado por una normocalcemia y una normofosfatemia. Los daños tisulares iniciales desencadenan una cascada molecular compleja implicando la liberación de proteínas celulares con afinidad fosfática, notablemente las proteínas mitocondriales, que favorecen la formación de focos de nucleación cristalina, luego la precipitación progresiva de compuestos cálcicos alrededor de las estructuras fibrilares de la dermis, notablemente las fibras de colágeno y elastina.
En medicina humana, esta forma representa la manifestación más frecuente y concierne hasta el 70% de los niños afectados de dermatomiositis. Las conectivitis constituyen las etiologías principales, incluyendo la esclerodermia, la dermatomiositis, el lupus eritematoso y las conectivitis mixtas. Los procesos infecciosos, neoplásicos y ciertas dermatosis hereditarias como el síndrome de Ehlers-Danlos completan el espectro etiológico de esta forma.
La Calcinosis Metastásica
Procede de un mecanismo radicalmente diferente, implicando la precipitación cálcica en tejidos estructuralmente intactos. Esta forma resulta directamente de anomalías metabólicas sistémicas provocando una hipercalcemia, una hiperfosfatemia, o ambas simultáneamente. El hiperparatiroidismo, ya sea primario o secundario, constituye el principal factor desencadenante por intermedio de tres vías metabólicas convergentes: la activación de la resorción osteoclástica, el aumento de la reabsorción tubular renal del calcio, y la estimulación indirecta de la síntesis de calcitriol que intensifica la absorción intestinal cálcica.
El concepto de producto fosfocálcico reviste aquí una importancia capital. Cuando este producto (calcio sérico × fósforo sérico) franquea el umbral crítico de 70 mg²/dL², fenómenos de cristalización espontánea se inician en diversas estructuras orgánicas. Aunque los órganos viscerales (estómago, pulmones, riñones, miocardio) constituyen los blancos privilegiados, la piel puede también estar afectada, aunque más raramente.
Formas Particulares y Emergentes
La calcinosis idiopática representa una entidad enigmática caracterizada por la ausencia de toda anomalía metabólica detectable y de lesión tisular preexistente. Esta forma suscita interrogantes fundamentales concernientes a la existencia de mecanismos fisiopatológicos aún desconocidos o de predisposiciones genéticas latentes. En medicina humana, esta categoría incluye la calcinosis tumoral, los nódulos calcificados subepidérmicos y la calcinosis escrotal.
La calcinosis iatrogénica resulta directamente de intervenciones o tratamientos médicos específicos. La administración local o sistémica de productos que contienen calcio o fosfato, como el gluconato de calcio, puede provocar depósitos cálcicos localizados. La suplementación excesiva en vitamina D constituye igualmente un factor de riesgo reconocido, particularmente en animales que reciben complementos nutricionales no controlados.
La calciofilaxis constituye indudablemente la forma más temible. Esta entidad se distingue por la calcificación selectiva de la media de las arteriolas dérmicas e hipodérmicas, generando un proceso isquémico progresivo. Las consecuencias clínicas resultan dramáticas: necrosis cutáneas extensivas, desbridamientos tisulares, sobreinfecciones sépticas recurrentes y mortalidad elevada. Esta forma permanece estrechamente asociada a los estadios terminales de insuficiencia renal crónica y se observa particularmente en pacientes dializados en medicina humana.
Mecanismos Fisiopatológicos Detallados de la Calcinosis Distrófica
En la calcinosis distrófica, las tasas séricas de calcio y fosfato permanecen dentro de los límites fisiológicos normales. El proceso patológico se inicia por daños tisulares que entrañan la liberación masiva de proteínas intracelulares, notablemente las proteínas mitocondriales dotadas de una afinidad particular por el fosfato. Estas proteínas actúan como centros de nucleación, favoreciendo la precipitación local de las sales cálcicas.
La hipoxia tisular local, consecuencia directa de las lesiones iniciales, crea un ambiente favorable a la calcificación. La inflamación crónica mantiene este proceso por la liberación sostenida de citoquinas pro-inflamatorias, particularmente el TNF-α, la IL-6 y la IL-1β. Estos mediadores inflamatorios amplifican la respuesta tisular local y perpetúan las condiciones propicias a la mineralización patológica.
La formación de cristales intracelulares constituye un evento deletéreo mayor, conduciendo ineludiblemente a la necrosis celular. Esta muerte celular libera nuevos focos de nucleación y mantiene un círculo vicioso auto-mantenido de calcificación progresiva. El proceso se extiende gradualmente a las estructuras adyacentes, particularmente las fibras de colágeno y elastina de la dermis, creando las lesiones características observadas clínicamente.
Epidemiología y Particularidades Etiológicas en Medicina Veterinaria Canina
Distribución Etiológica y Datos Cuantitativos
El análisis epidemiológico revela una repartición etiológica particularmente característica en medicina veterinaria canina. Un estudio retrospectivo de envergadura permitió establecer con precisión la distribución de las causas subyacentes, revelando patrones distintos de aquellos observados en medicina humana.
El hipercorticismo domina masivamente el paisaje etiológico, representando aproximadamente el 80% del conjunto de casos observados. Esta predominancia se explica por la frecuencia de las corticoterapias sistémicas en medicina veterinaria y por la incidencia no desdeñable de los síndromes de Cushing espontáneos en la especie canina. Dentro de esta categoría mayoritaria, el hipercorticismo iatrogénico, consecuencia directa de tratamientos corticoides prolongados, constituye cerca del 70% de los casos, mientras que los hipercorticismos endógenos (hipofisarios y suprarrenales) representan el 30% restante.
Esta predominancia del hipercorticismo iatrogénico se explica por el uso frecuente de los corticosteroides en medicina veterinaria para el tratamiento de diversas afecciones inflamatorias, alérgicas y autoinmunes. La facilidad de acceso a estas moléculas y su eficacia terapéutica inmediata favorecen a veces su prescripción prolongada, creando las condiciones propicias al desarrollo de calcinosis cutáneas.
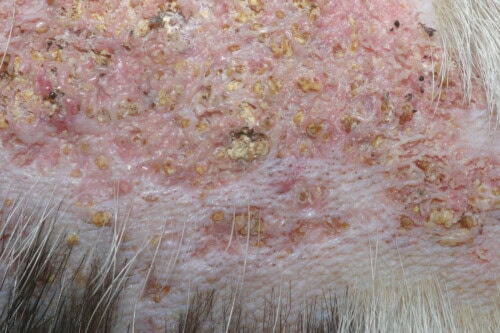
Calcinosis cutánea : Vista de cerca
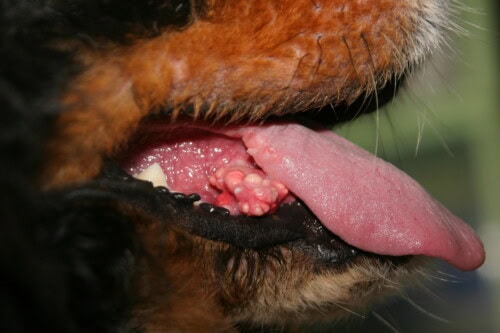
Calcinosis cutánea : Lesiones sublinguales
Causas Minoritarias y Situaciones Particulares
La insuficiencia renal crónica ocupa la segunda posición etiológica con aproximadamente el 10% de los casos documentados. Esta proporción relativamente modesta se explica por la predilección de los depósitos cálcicos metastásicos por los tejidos blandos viscerales más que por las estructuras cutáneas en esta patología. Sin embargo, las formas cutáneas, cuando ocurren, se asocian generalmente a estadios avanzados de la enfermedad renal y constituyen un indicador pronóstico desfavorable.
La última décima parte agrupa un conjunto heterogéneo de etiologías raras pero clínicamente significativas. La calcinosis distrófica post-traumática puede sobrevenir consecutivamente a traumatismos repetidos o a lesiones mecánicas crónicas, particularmente en las zonas sometidas a fricciones recurrentes o a presiones mecánicas sostenidas.
Las formas post-inflamatorias se observan a veces en el contexto de infecciones sistémicas severas, particularmente las micosis profundas como la blastomicosis o la histoplasmosis, y ciertas leptospirosis. Estas infecciones crean un estado inflamatorio sistémico propicio al desarrollo de lesiones de calcificación distrófica.
La calcinosis idiopática, aunque rara, merece una atención particular pues suscita preguntas fundamentales sobre nuestra comprensión de los mecanismos fisiopatológicos. La ausencia de causa subyacente identificada sugiere la existencia de factores predisponentes genéticos o ambientales aún desconocidos.
Las calcinosis iatrogénicas no corticoides, ligadas a las perfusiones de solutos cálcicos o a las suplementaciones vitamínicas excesivas, completan este cuadro etiológico. Estas formas evitables subrayan la importancia de una vigilancia atenta durante la administración de tratamientos potencialmente calcificantes.
Consideraciones Raciales y Predisposiciones
Aunque ninguna exclusividad racial esté establecida de manera formal, ciertas observaciones clínicas sugieren una predisposición de las razas de gran tamaño. Esta tendencia podría explicarse por una susceptibilidad acrecentada a las patologías endocrinas, notablemente el hiperadrenocorticismo, o por diferencias en las prácticas terapéuticas según el tamaño de los animales.
El Bulldog inglés es objeto de una atención particular en la literatura veterinaria, ciertos datos sugiriendo una predisposición específica en esta raza. Esta susceptibilidad podría estar ligada a las particularidades anatómicas de la raza, notablemente los pliegues cutáneos numerosos creando microtraumatismos repetidos, o a factores genéticos específicos aún no elucidados.
Las razas braquicéfalas en su conjunto podrían presentar una predisposición relativa, posiblemente en relación con su propensión a los trastornos respiratorios crónicos que requieren tratamientos anti-inflamatorios prolongados. Esta hipótesis requiere sin embargo estudios epidemiológicos más profundos para ser confirmada.
Semiología Clínica y Enfoque Diagnóstico Contemporáneo
Polimorfismo de las Manifestaciones Clínicas
La presentación clínica de las calcinosis cutáneas caninas se caracteriza por un polimorfismo notable, reflejando la diversidad de los mecanismos fisiopatológicos subyacentes y la heterogeneidad de las respuestas tisulares individuales. Esta variabilidad semiológica constituye a veces un desafío diagnóstico considerable, requiriendo un enfoque clínico metódico y experimentado.
La localización anatómica privilegia clásicamente la región dorsal, constituyendo el sitio de afectación más frecuentemente observado. Sin embargo, la afectación puede extenderse a las zonas ventrales glabras, particularmente el abdomen y la región inguinal, a los pliegues cutáneos donde los fenómenos de maceración favorecen la inflamación local, a la región cervical y a las axilas. Esta distribución topográfica no aleatoria sugiere la intervención de factores mecánicos locales, notablemente las fricciones y presiones repetidas, o de particularidades vasculares regionales en el desarrollo y progresión de las lesiones.
Las zonas de predilección corresponden a menudo a las regiones sometidas a tensiones mecánicas particulares o que presentan características anatómicas específicas. Los pliegues cutáneos, por ejemplo, crean un microambiente húmedo y cálido propicio a la inflamación crónica, mientras que las zonas de contacto con el suelo o las superficies de descanso sufren traumatismos repetidos de baja intensidad.
Características Morfológicas de las Lesiones
El aspecto lesional presenta dos fenotipos principales distintos, cada uno correspondiendo probablemente a estadios evolutivos diferentes o a mecanismos fisiopatológicos específicos. El primer fenotipo se manifiesta por placas firmes a francamente duras, ostentando una coloración amarillenta característica y circunscritas por un rodete eritematoso marcado que atestigua la intensa reacción inflamatoria perilesional. Esta presentación corresponde generalmente a los estadios agudos o subagudos del proceso patológico.
El segundo fenotipo corresponde a placas alopécicas extendidas, notablemente induradas, presentando una tinta rosada intensa evocadora de una inflamación crónica subyacente. Estas lesiones atestiguan generalmente una evolución más prolongada y una cronicización del proceso inflamatorio local.
La palpación revela una consistencia característica, oscilando entre la firmeza marcada y la dureza francamente pétrea según el grado de mineralización. Esta induración constituye un elemento semiológico patognomónico, permitiendo diferenciar las calcinosis de otras dermatosis inflamatorias crónicas.
La superficie lesional puede presentar diversas alteraciones: hiperqueratosis localizada, formación de costras superficiales, exudación de composición variable, y en los casos más evolucionados, ulceración franca con exposición de la dermis subyacente. La presencia de un exudado purulento atestigua generalmente una sobreinfección bacteriana secundaria.
Signos Patognomónicos y Evolución Lesional
La evolución lesional sigue generalmente un patrón previsible, aunque la cronología puede variar considerablemente de un individuo a otro. Las fases iniciales se acompañan frecuentemente de costras superficiales y de un exudado de composición variable, yendo de un simple rezume seroso a una descarga purulenta en caso de sobreinfección.
Un signo patognomónico particularmente evocador reside en la extrusión espontánea de material calcáreo blanquecino a través de la epidermis. Este fenómeno corresponde a la eliminación transcutánea de los cristales cálcicos y constituye un elemento diagnóstico de primera importancia. La observación de este material cristalino, fácilmente reconocible por su textura y coloración características, permite a menudo establecer el diagnóstico con una cuasi-certeza.
La ulceración representa una complicación corriente, particularmente en las formas severas o descuidadas. Estas úlceras presentan características específicas: bordes sobreelevados e indurados, fondo anfractuoso tapizado de tejido de granulación, tendencia a la cronicización y resistencia a los tratamientos cicatrizantes convencionales.
Durante la fase de resolución, observada principalmente después de la corrección de la causa subyacente, las lesiones sufren una transformación progresiva de su aspecto. El componente inflamatorio se atenúa gradualmente, traduciéndose por una disminución del eritema perilesional y de la sensibilidad local. La coloración evoluciona hacia tonalidades grisáceas más opacas, atestiguando la normalización progresiva de los procesos tisulares locales. Sin embargo, la induración puede persistir durante meses, incluso definitivamente en ciertos casos.
Complicaciones Infecciosas y Evolución
Las sobreinfecciones bacterianas secundarias constituyen una complicación cuasi-constante, favorecidas por la alteración de la barrera epidérmica y por el ambiente inflamatorio local que compromete los mecanismos de defensa naturales. Estas sobreinfecciones pueden enmascarar las lesiones subyacentes y complicar significativamente la evaluación diagnóstica.
La flora bacteriana implicada comprende clásicamente los estafilococos y estreptococos, pero gérmenes oportunistas más resistentes pueden colonizar las lesiones crónicas. La identificación precisa de estos agentes patógenos por cultivo bacteriano y antibiograma resulta a menudo necesaria para adaptar la antibioterapia local o sistémica.
La presencia de material cálcico en los tejidos crea un ambiente particularmente propicio al desarrollo de biofilms bacterianos, estructuras tridimensionales complejas que protegen los microorganismos de la acción de los antimicrobianos y de los mecanismos de defensa del huésped. Esta particularidad explica la resistencia frecuente a los tratamientos antibióticos convencionales y la tendencia a la recidiva de las sobreinfecciones.
Estrategia Diagnóstica Diferencial
El establecimiento del diagnóstico de calcinosis reposa principalmente sobre el reconocimiento de los patrones clínicos característicos y sobre el análisis del contexto anamnésico. La piodermitis profunda crónica o recidivante constituye la principal trampa diagnóstica, tanto más cuanto que las dos afecciones pueden coexistir y potenciarse mutuamente.
Varios elementos permiten orientar el diagnóstico diferencial: la consistencia particularmente dura de las lesiones de calcinosis contrasta con la consistencia más blanda de las piodermitis, la extrusión de material calcáreo constituye un signo patognomónico de calcinosis, y el contexto anamnésico (corticoterapia, síndrome de Cushing) orienta fuertemente hacia una calcinosis.
Otras afecciones pueden ocasionalmente prestarse a confusión: los granulomas a cuerpo extraño, los tumores cutáneos calcificados, los quistes sebáceos infectados, o las paniculitis crónicas. La toma en cuenta del conjunto de elementos clínicos y anamnésicos permite generalmente levantar estas ambigüedades diagnósticas.
La citología cutánea resulta particularmente preciosa para caracterizar las sobreinfecciones bacterianas concomitantes y orientar las elecciones antimicrobianas locales. Aunque no permitiendo la confirmación formal del diagnóstico de calcinosis, este examen contribuye a la evaluación global del estado lesional y guía las decisiones terapéuticas complementarias. La observación de cristales cálcicos durante el examen citológico puede reforzar la sospecha diagnóstica.
En ciertos casos complejos o atípicos, la histopatología cutánea puede resultar necesaria para confirmar el diagnóstico y caracterizar precisamente el tipo de calcinosis. Este examen permite objetivar la presencia de depósitos cálcicos en las estructuras dérmicas y evaluar la intensidad de la reacción inflamatoria asociada.
Estrategias Terapéuticas Actuales y Limitaciones
Principio Fundamental : Corrección de la Causa Primaria
La toma a cargo terapéutica de las calcinosis cutáneas reposa sobre un principio cardinal: la identificación y corrección de la causa subyacente constituyen la etapa fundamental, condicionando el conjunto del pronóstico. Este enfoque etiológico prima sobre toda consideración sintomática y determina las posibilidades de regresión lesional a medio y largo plazo.
En el contexto mayoritario del hipercorticismo iatrogénico, este enfoque implica la detención progresiva y cuidadosamente controlada de la corticoterapia. Esta decrecencia debe ser adaptada a la duración del tratamiento anterior, a las dosis utilizadas y a la patología inicialmente tratada. Un destete demasiado brutal expone al riesgo de insuficiencia suprarrenal iatrogénica, particularmente temible después de tratamientos prolongados a dosis elevadas.
El protocolo de decrecencia debe tener en cuenta la vida media biológica de los corticosteroides utilizados y la duración de supresión del eje hipotálamo-hipófiso-suprarrenal. Generalmente, una reducción del 25 al 50% de la dosis cada dos semanas constituye un compromiso aceptable entre eficacia y seguridad. En ciertos casos, una sustitución por anti-inflamatorios alternativos (inmunosupresores, bioterapias) puede facilitar el destete corticoide.
La regresión de las lesiones cutáneas se observa efectivamente después de la corrección de la causa primaria, pero su amplitud permanece impredecible, oscilando entre una resolución completa y una mejoría solamente parcial. Los factores que influyen en esta variabilidad incluyen la duración de evolución de las lesiones antes del tratamiento, la intensidad de la exposición a los corticosteroides, y la capacidad de regeneración tisular individual.
Cuidados Locales y Gestión de las Complicaciones
La antisepsia local constituye un pilar terapéutico ineludible en la toma a cargo de las calcinosis cutáneas. La aplicación rigurosa de antisépticos tópicos, particularmente la clorhexidina a concentración adaptada (0,5 al 2% según la tolerancia local), resulta fundamental para controlar las sobreinfecciones bacterianas secundarias y mantener un ambiente local propicio a la cicatrización.
Este enfoque preventivo permite limitar las complicaciones infecciosas que pueden enmascarar la evolución natural de las lesiones y comprometer la evaluación de la eficacia terapéutica. La clorhexidina presenta la ventaja de una excelente tolerancia local y de un espectro antimicrobiano amplio, incluyendo las bacterias gram-positivas y gram-negativas habitualmente implicadas en las sobreinfecciones cutáneas.
Otros antisépticos pueden ser utilizados en alternativa o en rotación: la povidona yodada, particularmente eficaz pero potencialmente irritante, los derivados clorados a baja concentración, o los antisépticos a base de plata para las lesiones ulceradas resistentes. La alternancia de antisépticos puede prevenir el desarrollo de resistencias bacterianas.
La antibioterapia sistémica permanece raramente indicada en la toma a cargo de rutina, salvo en caso de septicemia comprobada, de sobreinfección extensiva con signos sistémicos, o de fracaso de los tratamientos antisépticos locales. Cuando resulta necesaria, la elección del antibiótico debe ser guiada por un cultivo bacteriano y un antibiograma, teniendo en cuenta la frecuencia de resistencias en este contexto.
El uso de agentes queratomoduladores y emolientes puede facilitar el ablandamiento de las zonas hiperqueratósicas y costrosas, mejorando así el confort del animal y favoreciendo la eliminación de los detritos superficiales. Estos tópicos, incluyendo la urea, el ácido salicílico a baja concentración, o las ceramidas, contribuyen igualmente a la restauración progresiva de la flexibilidad cutánea en las zonas periféricas a las lesiones.
Los apósitos oclusivos pueden ser benéficos para mantener la hidratación local y proteger las lesiones ulceradas de los traumatismos mecánicos. Sin embargo, su uso requiere una vigilancia atenta para prevenir la maceración excesiva que favorecería las sobreinfecciones.
Enfoques Quirúrgicos Selectivos
La exéresis quirúrgica conserva su pertinencia para lesiones únicas, muy localizadas y fuentes de molestia mayor para el animal. Esta opción terapéutica debe ser cuidadosamente evaluada en función de varios criterios: el tamaño y localización de las lesiones, el estado general del animal, la factibilidad técnica de la exéresis, y las perspectivas de cicatrización.
Las ventajas del enfoque quirúrgico incluyen la resolución inmediata de las lesiones problemáticas, la posibilidad de análisis histopatológico de confirmación, y la mejoría rápida del confort del animal. Sin embargo, los inconvenientes comprenden los riesgos anestésicos, particularmente en animales que presentan un hipercorticismo con sus complicaciones cardiovasculares y metabólicas, y el riesgo de trastornos de cicatrización ligados al hipercorticismo.
El láser CO2 puede constituir una alternativa interesante para ciertas situaciones particulares. Esta técnica presenta la ventaja de una mejor hemostasia, de una precisión de corte superior, y potencialmente de una cicatrización mejorada. Sin embargo, su accesibilidad permanece limitada y su uso requiere una experiencia técnica específica.
Las técnicas de cirugía reconstructiva pueden resultar necesarias para las lesiones extendidas, particularmente en las zonas donde el cierre primario resulta imposible. Los colgajos cutáneos locales o los injertos pueden ser considerados, aunque el hipercorticismo comprometa a menudo la toma de los injertos.
El Dimetilsulfóxido : Eficacia Controvertida y Límites
El DMSO, solvente orgánico con propiedades anti-inflamatorias reconocidas, notablemente por captación de radicales libres e inhibición de ciertas vías inflamatorias, se beneficia de un uso histórico en el tratamiento de las calcinosis. Su capacidad de penetración tisular notable, ligada a su estructura molecular particular, lo convierte teóricamente en un candidato interesante para esta indicación tópica.
Las propiedades fisicoquímicas del DMSO explican su interés potencial: peso molecular bajo facilitando la difusión transcutánea, capacidad de solubilización de numerosas sustancias, propiedades anti-inflamatorias por inhibición de la polimerización de radicales libres, y efecto analgésico local por bloqueo de las fibras nerviosas de pequeño calibre.
Sin embargo, su eficacia real queda por demostrar por estudios controlados rigurosos. La dificultad de evaluación proviene del hecho de que las calcinosis pueden regresar espontáneamente una vez corregida la causa primaria, volviendo compleja la atribución de las mejorías observadas al tratamiento por DMSO. El mecanismo de acción exacto en este contexto permanece enigmático: disolución directa de los cristales cálcicos, efecto anti-inflamatorio no específico, mejoramiento de la microcirculación local, o simple efecto placebo.
La ausencia de protocolo estandarizado constituye una limitación mayor que compromete la evaluación objetiva de esta terapéutica. La literatura reporta esquemas terapéuticos extremadamente variables, desde tres a cuatro aplicaciones cotidianas durante dos semanas máximo hasta una aplicación bisemanal sobre varias semanas según ciertos reportes de casos. Las recomendaciones de Muller & Kirk preconizan dos aplicaciones cotidianas sin precisión de duración, mientras que otras fuentes sugieren una aplicación cada dos días sobre varias semanas.
Esta heterogeneidad protocolaria refleja la ausencia de datos probatorios sólidos y la naturaleza empírica de esta utilización. El establecimiento de un protocolo estandarizado requeriría estudios clínicos controlados randomizados comparando diferentes esquemas terapéuticos a un placebo.
Los efectos secundarios potenciales imponen una vigilancia particular y limitan el uso de esta molécula. Para el aplicador, el porte de guantes de caucho espesos resulta indispensable para evitar la absorción percutánea que puede provocar efectos sistémicos indeseables. La inhalación de vapores debe igualmente ser evitada, requiriendo una ventilación adecuada de los locales de aplicación.
En el animal tratado, reacciones locales diversas han sido reportadas: sensación de quemadura inmediata después de la aplicación, eritema y edema transitorios, sequedad cutánea y descamación, y en ciertos casos, agravación paradójica de la inflamación local. Los efectos oculares en caso de uso prolongado o a dosis fuerte incluyen modificaciones del cristalino y trastornos de la acomodación. Un malestar general no específico puede igualmente sobrevenir, particularmente durante aplicaciones sobre superficies extendidas.
Los datos concernientes a una eventual nefrotoxicidad o hepatotoxicidad permanecen contradictorios e insuficientemente sustentados. Ciertos reportes sugieren alteraciones de los parámetros hepáticos durante usos prolongados, mientras que otros estudios no encuentran ninguna toxicidad sistémica significativa. Esta incertidumbre impone una vigilancia clínica y biológica en animales tratados de manera prolongada.
En caso de uso sobre grandes superficies cutáneas, un enfoque prudente consistente en tratar pequeñas zonas de manera secuencial es fuertemente recomendado para minimizar los riesgos de absorción sistémica y de efectos indeseables. Esta estrategia permite igualmente evaluar la tolerancia local antes de extender el tratamiento.
Diversidad de los Enfoques Farmacológicos Humanos
La medicina humana ha desarrollado un arsenal terapéutico sustancial para la toma a cargo de las calcinosis, apuntando a diferentes mecanismos fisiopatológicos. Estos enfoques múltiples ofrecen perspectivas interesantes para una transposición en medicina veterinaria, aunque ninguna evaluación sistemática haya sido aún emprendida en la especie canina. La ausencia de tratamiento estándar universalmente eficaz en medicina humana subraya la complejidad de esta patología y la necesidad de enfoques individualizados.
Las estrategias terapéuticas humanas apuntan a varios mecanismos: inhibición de la formación de cristales cálcicos, mejoramiento de su solubilización en los tejidos, disminución de la inflamación local y sistémica, o modulación de las vías metabólicas del calcio y del fosfato. Este enfoque multimodal permite adaptar el tratamiento a los mecanismos fisiopatológicos predominantes en cada caso particular.
El diltiazem, antagonista cálcico
Inhibe la entrada del calcio intracelular por bloqueo de los canales cálcicos voltaje-dependientes de tipo L. Esta acción podría teóricamente limitar los procesos de calcificación tisular reduciendo la disponibilidad del calcio intracelular para la formación de cristales. La posología humana de 2 a 4 mg/kg/día presenta una toxicidad limitada, principalmente cardiovascular (hipotensión, bradicardia), pero la inocuidad en uso prolongado en el perro permanece no documentada.
El uso del diltiazem en medicina veterinaria cardiológica, notablemente para el tratamiento de la cardiomiopatía hipertrófica felina, sugiere una tolerancia aceptable. Sin embargo, la adaptación posológica y la vigilancia de efectos secundarios requerirían estudios específicos para la indicación calcinosis.
Bifosfonatos : Moduladores de la Actividad Macrofágica
Los bifosfonatos (alendronato, pamidronato, etidronato) ejercen su acción por inhibición de la actividad macrofágica y de la resorción cálcica ósea. Estas moléculas, análogos estructurales del pirofosfato, se fijan preferencialmente sobre la hidroxiapatita e interfieren con los procesos de mineralización y desmineralización.
Su eficacia ha sido documentada en varias conectivitis humanas, particularmente la esclerodermia y la dermatomiositis, donde reducen significativamente el tamaño y número de depósitos cálcicos. El mecanismo de acción implica probablemente una inhibición de la actividad de los macrófagos tisulares que participan activamente en los procesos de calcificación distrófica.
Los efectos secundarios potenciales incluyen la hipocalcemia, a veces severa y requiriendo una suplementación, la fiebre post-administración (particularmente con las formas intravenosas), y la osteonecrosis mandibular, complicación rara pero grave observada principalmente con los bifosfonatos de tercera generación.
En medicina veterinaria canina, su uso permanece actualmente limitado pero ciertas moléculas como el pamidronato son utilizadas para la gestión de dolores óseos metastásicos o de osteólisis tumorales. Esta experiencia clínica limitada sugiere una tolerancia aceptable, pero requeriría una adaptación para la indicación calcinosis cutánea.
Agentes Quelantes y Moduladores de Solubilidad
El tiosulfato de sodio presenta la propiedad de aumentar la solubilidad cálcica por formación de complejos solubles con los iones calcio. Esta molécula puede ser utilizada por vía tópica, intralesional o intravenosa según las indicaciones y la tolerancia. Su mecanismo de acción implica una quelación directa del calcio tisular y un mejoramiento de su movilización hacia la circulación sistémica.
Su toxicidad sistémica notable comprende náuseas y vómitos, una hipocalcemia potencialmente severa, y diversos trastornos electrolíticos incluyendo una hipomagnesemia y una hipopotasemia. Estos efectos indeseables imponen una vigilancia biológica estrecha durante usos sistémicos.
Aunque ningún uso actual esté reportado en el perro, investigaciones podrían ser consideradas para un uso local bajo forma de gel o de solución tópica. Este enfoque minimizaría los riesgos de efectos sistémicos conservando el efecto local buscado.
El hidróxido de aluminio actúa como ligante del fosfato a nivel intestinal y reduce la absorción digestiva de este último. Esta acción indirecta sobre el metabolismo fosfocálcico podría presentar un interés en las formas metastásicas de calcinosis. Las dosis humanas de 1,8 a 2,4 g/día sugieren un uso potencial en el animal, pero esta aplicación permanece no validada en el contexto de la calcinosis.
El uso de esta molécula en medicina veterinaria para la gestión de la hiperfosfatemia en insuficientes renales crónicos sugiere una tolerancia aceptable. Sin embargo, la adaptación posológica y la evaluación de la eficacia específica requerirían estudios dedicados.
Antibióticos con Propiedades Anti-calcificantes
La minociclina presenta propiedades múltiples particularmente interesantes: inhibición de las metaloproteasas matriciales (MMP) que participan en los procesos de remodelación tisular, quelación cálcica directa por sus agrupamientos funcionales, y reducción de la inflamación por inhibición de la activación microglial y de la producción de citoquinas pro-inflamatorias.
La posología humana de 50 a 100 mg/día abre perspectivas de uso en el perro, tanto más cuanto que esta molécula existe ya en ciertas indicaciones dermatológicas veterinarias, notablemente para el tratamiento de piodermitis a gérmenes resistentes. Esta experiencia clínica preexistente facilitaría la adaptación posológica y la vigilancia de efectos secundarios.
Las metaloproteasas matriciales juegan un papel crucial en los procesos de calcificación distrófica degradando la matriz extracelular y liberando factores que favorecen la mineralización. Su inhibición por la minociclina podría entonces presentar un interés terapéutico directo.
La ceftriaxona ofrece un efecto secundario potencialmente benéfico por inhibición de las metaloproteasas matriciales, quelación del calcio por sus agrupamientos β-lactama, y acción anti-inflamatoria no específica. Sin embargo, las reglas de prescripción responsable de antibióticos, particularmente estrictas para las cefalosporinas de tercera generación, prohíben formalmente considerar su uso en medicina veterinaria para esta indicación no infecciosa.
Esta restricción reglamentaria subraya la importancia de desarrollar alternativas no antibióticas para evitar la contribución a la antibiorresistencia explorando vías terapéuticas innovadoras.
Moduladores del Metabolismo Fosfocálcico
El probenecid aumenta la excreción renal del fosfato por inhibición de su reabsorción tubular. Su efecto benéfico ha sido documentado en la dermatomiositis juvenil, donde reduce significativamente los depósitos cálcicos cutáneos. Esta molécula no es actualmente utilizada en medicina veterinaria, pero su mecanismo de acción podría presentar un interés para las formas metastásicas de calcinosis.
La adaptación de este enfoque en medicina veterinaria requeriría estudios farmacocinéticos previos para determinar las posologías apropiadas y evaluar la tolerancia en la especie canina. Los efectos secundarios humanos incluyen principalmente trastornos digestivos y reacciones de hipersensibilidad.
La colchicina
Presenta propiedades anti-inflamatorias específicas por inhibición de la polimerización de microtúbulos y modulación de la activación de neutrófilos. Su uso en medicina veterinaria permanece poco desarrollado, pero algunas aplicaciones existen, notablemente para el tratamiento de la fiebre familiar del Shar-Pei.
Un reporte de caso particularmente alentador documentó una neta mejoría de lesiones de calcinosis en un perro tratado con colchicina a la dosis utilizada para la fiebre familiar del Shar-Pei (sea aproximadamente 0,01 a 0,03 mg/kg/día). Aunque este dato permanezca muy preliminar y no constituya más que una observación aislada, ilustra el interés potencial de agentes anti-inflamatorios dirigidos y subraya la necesidad de conducir estudios clínicos para evaluar rigurosamente estas nuevas opciones.
El mecanismo de acción de la colchicina en este contexto podría implicar una inhibición de la activación de los inflamasomas, complejos multiproteicos responsables de la maduración de la IL-1β y de la IL-18, citoquinas clave en los procesos de calcificación distrófica.
Esta observación preliminar con la colchicina abre perspectivas particularmente interesantes pues demuestra la factibilidad de un enfoque farmacológico específico en medicina veterinaria. La tolerancia aparentemente satisfactoria y la mejoría clínica observada justifican la puesta en marcha de estudios clínicos más rigurosos.
La ventaja de la colchicina reside en su perfil de seguridad bien establecido en el perro, gracias a su uso en la fiebre familiar del Shar-Pei, y en su mecanismo de acción específico sobre las vías inflamatorias implicadas en la calcificación distrófica.
Recomendaciones Prácticas y Algoritmo Decisional
Enfoque Diagnóstico Estructurado
El reconocimiento precoz de las calcinosis reposa sobre un tríptico diagnóstico: identificación de los patrones clínicos característicos, análisis del contexto anamnésico y exclusión de los diagnósticos diferenciales principales. Este enfoque sistemático permite evitar los retrasos diagnósticos que comprometen la eficacia terapéutica y optimizar la toma a cargo precoz.
El interrogatorio anamnésico debe ser particularmente minucioso, buscando sistemáticamente los antecedentes de corticoterapia (molécula, posología, duración, vía de administración), los signos de hipercorticismo espontáneo (poliuro-polidipsia, polifagia, alopecias bilaterales simétricas, amiotrofia, distensión abdominal), y las patologías susceptibles de provocar trastornos del metabolismo fosfocálcico (insuficiencia renal crónica, tumores malignos, hiperparatiroidismo).
El examen clínico debe ser sistemático y completo, no limitándose a las lesiones cutáneas sino buscando igualmente los signos sistémicos asociados. La palpación atenta del conjunto del tegumento permite identificar lesiones debutantes o asintomáticas que orientan hacia una afectación más difusa.
La evaluación de la causa subyacente debe ser exhaustiva y orientada por los datos epidemiológicos. La búsqueda de un hipercorticismo, ya sea iatrogénico o espontáneo, constituye la prioridad absoluta teniendo en cuenta su frecuencia dominante. Esta evaluación incluye la medida del cortisol basal, las pruebas de frenación a la dexametasona, y eventualmente la dosificación de la ACTH endógena para diferenciar las formas hipofisarias y suprarrenales.
La exploración de la insuficiencia renal crónica se impone en segunda intención, particularmente en animales ancianos o que presentan antecedentes de nefropatía. Esta evaluación comprende la medida de la creatinina y de la urea séricas, el análisis de orina completo, y la evaluación del metabolismo fosfocálcico (calcemia, fosfatemia, parathormona si disponible).
Estrategia Terapéutica Jerarquizada
La corrección de la causa primaria permanece como la etapa fundamental ineludible, condicionando el conjunto del pronóstico a medio y largo plazo. Este enfoque etiológico debe ser privilegiado sobre toda consideración sintomática, pues determina directamente las posibilidades de regresión lesional espontánea.
En el caso mayoritario del hipercorticismo iatrogénico, la detención progresiva de la corticoterapia debe ser planificada de manera individualizada según la duración del tratamiento anterior, las dosis utilizadas, y la patología inicialmente tratada. Un protocolo de decrecencia progresiva sobre 4 a 8 semanas minimiza los riesgos de insuficiencia suprarrenal iatrogénica permitiendo una recuperación del eje hipotálamo-hipófiso-suprarrenal.
Para los hipercorticismos espontáneos, el tratamiento específico (trilostano, mitotano) o quirúrgico (suprarrenalectomía, hipofisectomía) debe ser emprendido según las recomendaciones establecidas para estas patologías. La gestión de las calcinosis se vuelve entonces secundaria y sigue generalmente el mejoramiento del hipercorticismo.
Los cuidados locales antisépticos constituyen un complemento indispensable para prevenir las complicaciones infecciosas y mantener la integridad de los tejidos circundantes. Este enfoque preventivo permite preservar las condiciones óptimas para la cicatrización espontánea y evitar los factores agravantes.
El protocolo antiséptico recomendado comprende una limpieza biquotidiana de las lesiones con una solución de clorhexidina al 0,5-2% según la tolerancia local, seguida de un secado cuidadoso y de la aplicación eventual de un agente emoliente. Esta rutina debe ser mantenida hasta resolución completa de las lesiones.
El uso de tratamientos específicos como el DMSO debe ser reservado a los casos severos o resistentes, respetando escrupulosamente las precauciones de empleo e informando a los propietarios de las incertidumbres concernientes a la eficacia real. Un enfoque secuencial, tratando pequeñas zonas sucesivamente, minimiza los riesgos de efectos sistémicos permitiendo una evaluación de la tolerancia local.
Criterios de Vigilancia e Indicadores Pronósticos
La evaluación de la evolución lesional requiere criterios objetivos estandarizados para permitir una apreciación reproducible de la eficacia terapéutica. La fotografía médica seriada constituye una herramienta preciosa para documentar las modificaciones morfológicas y apreciar cuantitativamente la evolución de la superficie lesional.
Los parámetros a vigilar incluyen el tamaño de las lesiones (medida bidimensional), su aspecto (coloración, relieve, induración), la presencia de complicaciones (ulceración, extrusión de material cálcico, sobreinfección), y el estado general del animal (prurito, dolor, molestia funcional).
Un score lesional compuesto integrando estos diferentes parámetros facilitaría la evaluación estandarizada y la comparación inter-individual. Este score podría incluir una cotación de 0 a 3 para cada parámetro (tamaño, induración, inflamación, ulceración) con un score global máximo orientando hacia la severidad.
La vigilancia de complicaciones potenciales, particularmente infecciosas, impone exámenes clínicos regulares a intervalos adaptados a la severidad inicial. Un ritmo semanal para las formas severas, quincenal para las formas moderadas, y mensual para las formas menores constituye un compromiso razonable entre vigilancia óptima y limitaciones prácticas.
La citología cutánea repetida permite detectar precozmente las sobreinfecciones bacterianas y ajustar los protocolos antisépticos. Esta vigilancia microbiológica resulta particularmente importante para las lesiones ulceradas o exudativas que presentan un riesgo infeccioso aumentado.
Gestión de los Fracasos Terapéuticos
La ausencia de mejoría después de 6 a 8 semanas de tratamiento etiológico bien conducido debe hacer reconsiderar el diagnóstico o buscar factores agravantes desconocidos. Esta situación impone una reevaluación completa incluyendo la verificación de la corrección efectiva de la causa primaria y la búsqueda de comorbilidades.
Las causas de fracaso terapéutico incluyen la persistencia de un hipercorticismo residual (decrecencia insuficiente, hipercorticismo espontáneo desconocido), la presencia de complicaciones infecciosas no controladas, o la existencia de factores intrínsecos de resistencia (cronicidad excesiva, trastornos de la cicatrización).
En estas situaciones de impasse terapéutico, el uso de tratamientos adyuvantes inspirados en la medicina humana puede ser considerado en ausencia de alternativa. Este enfoque compasional requiere una información esclarecida de los propietarios sobre el carácter experimental de estos tratamientos y la necesidad de una vigilancia reforzada.
Prevención y Educación
La prevención primaria de las calcinosis iatrogénicas reposa sobre el uso razonado de los corticosteroides: prescripción a la dosis mínima eficaz, limitación de la duración de tratamiento, búsqueda de alternativas terapéuticas cada vez que sea posible, y vigilancia clínica regular de pacientes bajo corticoterapia prolongada.
La educación de los propietarios juega un papel crucial en la detección precoz de las lesiones y la observancia terapéutica. Los consejos incluyen la vigilancia cotidiana del estado cutáneo, el reconocimiento de signos de alarma que requieren una consulta urgente, y la importancia del cumplimiento del protocolo terapéutico prescrito.
La formación continua de los practicantes sobre los últimos avances diagnósticos y terapéuticos permitiría mejorar la calidad de la toma a cargo y reducir los retrasos diagnósticos. Esta formación debería incluir el reconocimiento de las formas atípicas y el conocimiento de las nuevas opciones terapéuticas.
Conclusión y Perspectivas de Futuro
La calcinosis cutánea canina representa un modelo ejemplar de patología dermatológica que requiere un enfoque multidisciplinar integrando dermatología, endocrinología y medicina interna. La comprensión profunda de los mecanismos fisiopatológicos subyacentes y la identificación precisa de las causas etiológicas constituyen los fundamentos de una toma a cargo óptima que condiciona directamente el pronóstico funcional y estético.
La predominancia aplastante del hipercorticismo en la etiología de las calcinosis caninas, contrastando con la diversidad de causas observadas en medicina humana, subraya las particularidades epidemiológicas de esta afección en la especie canina. Esta especificidad etiológica simplifica relativamente el enfoque diagnóstico pero no debe hacer descuidar las formas minoritarias que requieren estrategias terapéuticas adaptadas.
Las limitaciones actuales del arsenal terapéutico veterinario contrastan de manera llamativa con la riqueza de opciones desarrolladas en medicina humana. Esta disparidad subraya la urgencia de desarrollar programas de investigación traslacional para evaluar la eficacia e inocuidad de los enfoques farmacológicos prometedores en la especie canina. La experiencia humana ofrece un reservorio considerable de innovaciones terapéuticas que merecerían una adaptación y validación en medicina veterinaria.
La ausencia de estudios clínicos controlados permanece como la principal limitación al progreso terapéutico en este dominio. Esta laguna metodológica perpetúa el uso de tratamientos empíricos y limita la capacidad de establecer recomendaciones basadas en las pruebas. La puesta en marcha de ensayos clínicos randomizados multicéntricos constituye un imperativo para hacer progresar los conocimientos y mejorar la calidad de los cuidados.
La investigación fundamental sobre los mecanismos moleculares de la calcificación cutánea canina podría revelar particularidades específicas a la especie e identificar nuevas dianas terapéuticas. Este enfoque mecanístico es indispensable para desarrollar tratamientos racionales y eficaces.