Die letzten Jahrestagungen des GEDAC, die in Ajaccio stattfanden, boten unserem Kollegen Vincent Bruet die Gelegenheit, eine Bestandsaufnahme der perianalen Fisteln, ihrer Pathogenese, ihrer klinischen Manifestationen und ihrer aktuellen therapeutischen Ansätze zu machen.
Perianale Fisteln bei Hunden stellen eine potenziell behindernde Hauterkrankung dar, die unbehandelt zu irreversiblen Veränderungen von Rektum und Anus führen und manchmal eine Euthanasie erforderlich machen kann. Diese Pathologie, auch bekannt als anale Furunkulose, betrifft hauptsächlich Deutsche Schäferhunde, kann aber auch andere Rassen betreffen und äußert sich durch Fistelgänge oder Ulzerationen um den Anus herum.
Lange Zeit wurde angenommen, dass die Pathogenese von perianalen Fisteln mit anatomischen Faktoren zusammenhängt. Heute wird jedoch angenommen, dass sie hauptsächlich immunvermittelt ist. Auch das therapeutische Management hat sich von einem hauptsächlich chirurgischen Ansatz zu einer überwiegend medizinischen Strategie entwickelt. Dieser Artikel bietet eine Synthese des aktuellen Wissensstands über diese Erkrankung und stellt therapeutische Empfehlungen vor, die auf einer methodischen Analyse der wissenschaftlichen Literatur basieren.
Pathogenese und klinische Aspekte von perianalen Fisteln bei Hunden
Eine komplexe und multifaktorielle Ätiologie
Die genaue Pathogenese von perianalen Fisteln ist trotz zahlreicher Studien noch nicht vollständig geklärt. Historisch gesehen wurden verschiedene Hypothesen zur Erklärung des Auftretens dieser Erkrankung aufgestellt. Die hohe Inzidenz bei Deutschen Schäferhunden ließ zunächst einen genetischen Zusammenhang vermuten, doch wurde bisher kein spezifischer genetischer Marker identifiziert. Auch ein tief getragener Schwanz wurde als prädisponierender Faktor angesehen, eine Theorie, die heute widerlegt ist, da auch andere Rassen betroffen sind und eine Schwanzamputation als Behandlung nicht wirksam ist.
Jüngste Forschungen deuten auf eine immunvermittelte Pathogenese hin. Es wurden Veränderungen der lokalen Entzündungsreaktion nachgewiesen, insbesondere eine Infiltration durch CD31+-T-Lymphozyten und eine erhöhte Expression von Zytokinen, die mit T-Helferzellen vom Typ 1 in der Läsionshaut assoziiert sind. Diese Mechanismen beinhalten wahrscheinlich:
- Eine lokale, T-Lymphozyten-vermittelte Entzündung
- Eine abnorme Aktivierung von Makrophagen mit Überexpression von Matrix-Metalloproteinasen MMP-9 und MMP-13
- Eine dysfunktionale Immunantwort auf Mikroben in der perianalen Region
- Mögliche Heilungsstörungen im perianalen Bereich
- Eine potenzielle Nahrungsmittelüberempfindlichkeitsreaktion, obwohl diese Hypothese noch bestätigt werden muss
Eine genetische Studie hat einen Zusammenhang zwischen dem MHC-Klasse-II-Allel DLA-DRB1*00101 und einem erhöhten Risiko für die Entwicklung perianaler Fisteln bei Deutschen Schäferhunden gezeigt. Die Klasse-II-Moleküle des Haupthistokompatibilitätskomplexes sind an der Antigenpräsentation und der Aktivierung von T-Lymphozyten beteiligt, was die Hypothese einer immunvermittelten Pathogenese stützt. Eine weitere Studie ergab eine potenzielle Assoziation mit den Genregionen ADAMTS16 und CTNND2, wobei letztere auch mit Morbus Crohn und Colitis ulcerosa beim Menschen in Verbindung gebracht wird.
Klinisches Bild und Signalement
Rassedisposition und Auftrittsalter
Perianale Fisteln betreffen hauptsächlich Deutsche Schäferhunde, die laut einigen Studien mehr als 80 % der betroffenen Population ausmachen. Es können jedoch auch verschiedene andere Rassen betroffen sein, darunter:
- Beagles
- Border Collies
- Australian Shepherds
- Irische Setter
- Chesapeake Bay Retriever
- Leonberger
- Staffordshire Bull Terrier
- Shih Tzu
- Welsh Corgis Pembroke
- Boxer
- Labrador Retriever
- Mischlingshunde
Das Auftrittsalter liegt im Allgemeinen zwischen dem jungen Erwachsenen- und dem mittleren Alter, mit einer Spanne von 2 bis 9 Jahren bei den meisten Patienten. Eine Geschlechts- oder Kastrationsprädisposition wurde nicht klar festgestellt, obwohl eine Studie ein erhöhtes Risiko bei unkastrierten Rüden im Vergleich zu kastrierten Rüden andeutete.
Läsionsaspekte und klinische Manifestationen
Die charakteristischen Läsionen von perianalen Fisteln umfassen:
- Sinus oder Fistelgänge um den Anus
- Perianale Ulzerationen
- Erosionen
- Pusteln in weniger schweren Fällen
- Seltenere rektale Fisteln
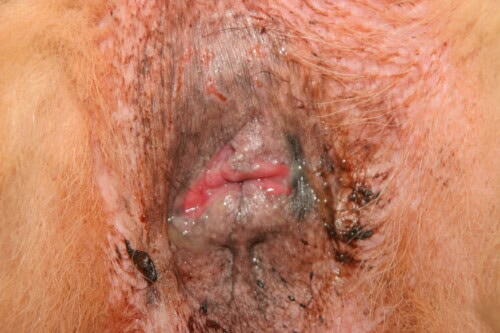
Mäßige perianale Fistelläsionen
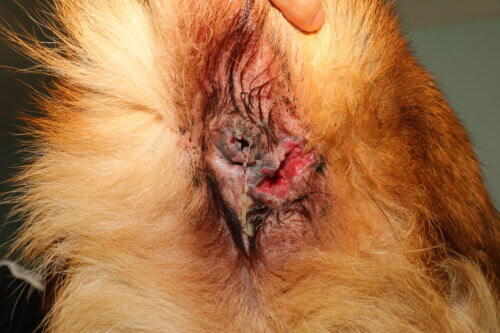
Schwere Läsionen, die hauptsächlich den unteren rechten Quadranten betreffen
Es ist wichtig zu beachten, dass die kutanen Sinusgänge, entgegen dem Begriff “perianale Fistel”, in der Regel nicht mit dem Rektallumen kommunizieren, im Gegensatz zu den bei Morbus Crohn beim Menschen beobachteten Fisteln. Diese Läsionen können einzeln oder multipel sein, und ihr Schweregrad variiert von leicht bis schwer, oft mit erheblichen Schmerzen.
Die von den Besitzern berichteten klinischen Anzeichen umfassen:
- Tenesmus (Anstrengung beim Kotabsatz)
- Hämatochezie (Blut im Stuhl)
- Dyschezie (Schmerzen beim Kotabsatz)
- Absetzen kleiner, häufiger Kotmengen
- Übermäßiges perianales Lecken
- Eitriger Ausfluss
- Verstopfung
- Koprophagie
- Anorexie
- Durchfall
- Fäkale Inkontinenz
- Gewichtsverlust
- Lethargie
Diese klinischen Manifestationen können stark beeinträchtigend sein und die Lebensqualität des Tieres erheblich beeinträchtigen. Eine Verbindung zwischen perianalen Fisteln und Kolitis wurde nachgewiesen, und einige betroffene Hunde zeigen auch weichen oder schleimigen Kot, Durchfall und eine erhöhte Häufigkeit des Kotabsatzes.
Diagnostischer Ansatz
Klinische Untersuchung und Differentialdiagnose
Die Diagnose perianaler Fisteln basiert hauptsächlich auf dem klinischen Bild und der körperlichen Untersuchung, insbesondere bei Deutschen Schäferhunden. Eine gründliche Untersuchung der perianalen Region und eine rektale Untersuchung sind unerlässlich, um das Ausmaß der Läsionen zu beurteilen und mögliche Begleitanomalien zu identifizieren. Aufgrund der Schmerzen und Beschwerden, die diese Erkrankung verursacht, kann eine Sedierung erforderlich sein, um eine vollständige rektale Untersuchung durchzuführen.
Das Sondieren der Fistelgänge mit einem Wattestäbchen oder einem ähnlichen Instrument ermöglicht die Bestimmung ihrer Tiefe. Die klinische Verlaufskontrolle kann durch Messung der Tiefen dieser Gänge erfolgen. Je nach Schwere und Dauer der Erkrankung kann die rektale Untersuchung das Fehlen innerer Anomalien oder eine schwere Fibrose ergeben, die durch eine Verdickung der perianalen Region mit der Möglichkeit von Analstenosen erkennbar ist.
Bei allen Patienten müssen eine gründliche Palpation und die Expression der Analsäcke durchgeführt werden, um ein Abszess der Analdrüse auszuschließen und festzustellen, ob die perianalen Fisteln mit den Analsäcken kommunizieren. Darüber hinaus können die Fistelgänge mit einem Katheter und steriler physiologischer Kochsalzlösung gespült werden, um festzustellen, ob sie miteinander kommunizieren oder ob eine Beteiligung der Analsäcke vorliegt.
Die Differentialdiagnose variiert erheblich je nach den vorliegenden klinischen Anzeichen:
- Bei ausschließlich perianalem Pruritus: allergische Dermatitis (atopische Dermatitis und unerwünschte Futtermittelreaktion), Analsäcke-Abszess
- Bei Tenesmus und Hämatochezie ohne sichtbare Fistelgänge: gastrointestinale Erkrankungen (entzündliche Darmerkrankung, Darmparasiten, Rektalstenosen)
- Ulkusbildende perianale Neoplasie (perianales Adenom oder Adenokarzinom)
- Kutane lymphozytäre Kolangitis (CLEC)
Es ist wichtig zu beachten, dass Deutsche Schäferhunde auch für CLEC prädisponiert sind, was zu analen oder perianalen Läsionen führen kann. Perianale Fisteln unterscheiden sich in der Regel von CLEC durch gut abgegrenzte Sinusgänge oder kraterförmige Ulzera, während CLEC mit Erosionen, Ulzera, Erythem und konfluenteren Krusten verbunden ist.
Wenn die klinische Differenzierung zwischen perianalen Fisteln und CLEC schwierig ist, können Hautbiopsien zur Histopathologie hilfreich sein. Ebenso sollten, wenn der Hund zu einer weniger häufig betroffenen Rasse gehört, andere Ursachen, die auf den klinischen Anzeichen basieren, zuerst ausgeschlossen werden.
Histopathologische Beurteilung
Obwohl die Histopathologie bei der Diagnose von perianalen Fisteln bei Hunden selten durchgeführt wird, kann sie in Fällen mit ungewöhnlicher klinischer Präsentation oder bei einer Rasse, die seltener betroffen ist, in Betracht gezogen werden. Die histopathologischen Merkmale umfassen:
- Eine periaddnexale Entzündung mit oder ohne Furunkulose
- Eine ausgeprägte Hidradenitis
- Eine periaddnexale Fibrose
- Eine Ulzeration
- Die Bildung von Sinusgängen, die im Dermis mit Epithel ausgekleidet sind
Entzündliche Infiltrate, bestehend aus Neutrophilen, Lymphozyten, Plasmazellen und Makrophagen, können in den Sinusgängen beobachtet werden. Tiefere Läsionen können auch mit pyogranulomatöser Cellulitis und lymphatischen Follikeln in Verbindung gebracht werden.
Kolonbiopsien von Hunden mit perianalen Fisteln können histopathologische Anzeichen einer Kolitis zeigen; eine Studie fand bei 9 von 18 Hunden mit perianalen Fisteln histopathologische Veränderungen, die mit einer Kolitisdiagnose vereinbar waren.
Therapeutische Ansätze bei Perianalfisteln
Chirurgisches Management: Eine begrenzte Rolle
Entwicklung der chirurgischen Praktiken
Die Behandlung von perianalen Fisteln hat sich im Laufe der Zeit erheblich entwickelt. Von den 1940er bis zu den 1970er Jahren wurden diese Läsionen als ausschließlich chirurgische Pathologie angesehen. Die Eingriffe umfassten in der Regel die Resektion aller betroffenen Gewebe, mit oder ohne Entfernung der Analsäcke. Dieses Verfahren konnte eine fokale Resektion oder eine vollständige (360 Grad) zirkumferentielle Resektion mit Anoplastik umfassen.
Verschiedene chirurgische Techniken wurden beschrieben:
- En-bloc-Exzision, gefolgt von einer chirurgischen Rekonstruktion
- Laser-Exzision (insbesondere ND:YAG-Laser)
- Kryotherapie zur Zerstörung des erkrankten Gewebes
- Amputation der Schwanzwurzel (wenn Fisteln als mit einem tief getragenen Schwanz assoziiert angesehen wurden)
Typischerweise erhielten die Patienten nach der Operation einen Stuhlweichmacher, um den Druck beim Stuhlgang zu verringern und die Heilung des Bereichs zu ermöglichen.
Grenzen und Komplikationen des chirurgischen Ansatzes
Die ausschließliche Anwendung der Chirurgie als Therapie weist mehrere große Probleme auf:
- Hohe Rezidivraten (in einer Studie bei über 50 % der Hunde berichtet)
- Fehlende vollständige Auflösung in vielen Fällen
- Signifikante chirurgische Komplikationen:
- Wunddehiszenz
- Flatulenz
- Fäkale Inkontinenz
- Durchfall
- Tenesmus
- Verstopfung
- Rektalstenosen
Die Studienergebnisse variieren, aber die Chirurgie wurde bei 6 % bis 21 % der Hunde als unwirksam beschrieben, wobei einige infolgedessen aufgegeben oder eingeschläfert wurden.
Ergänzender chirurgischer Ansatz
In jüngster Zeit haben mehrere Studien die Anwendung von Operationen beschrieben, nachdem die Wirksamkeit immunsuppressiver Therapien ein Plateau erreicht hatte. Dieser kombinierte Ansatz, bei dem die medikamentöse Behandlung der Operation vorausgeht, scheint bessere Ergebnisse zu erzielen als die alleinige Operation.
Bei dieser Strategie wird die chirurgische Behandlung eingesetzt:
- Wenn die medikamentöse Besserung ein Plateau erreicht hat
- Zur Behandlung persistierender Läsionen nach einer durch medizinische Behandlung erzielten Besserung
- Bei Tieren mit weiterhin Beschwerden oder Schmerzen (beeinträchtigte Lebensqualität)
- Aus Kostengründen, wenn eine langfristige medikamentöse Behandlung zu teuer ist
Die in diesem Zusammenhang durchgeführten chirurgischen Eingriffe umfassen:
- Exzision persistierender Fisteln
- Sakkulektomie
- Kryptenektomie
- Naht eventueller rektaler Fisteln
Immunmodulatorische Therapien: Eckpfeiler der Behandlung
Calcineurin-Inhibitoren
Ciclosporin A
Ciclosporin A gilt als eine der Referenzbehandlungen für Perianalfisteln bei Hunden. Sein Wirkmechanismus beinhaltet die Bindung an das intrazelluläre Protein Cyclophilin-1, wodurch Calcineurin gehemmt wird. Diese Hemmung verhindert die Dephosphorylierung des nuklearen Faktors aktivierter T-Lymphozyten und die anschließende Produktion proinflammatorischer Zytokine, insbesondere IL-2. Die verminderte IL-2-Produktion führt zu einer Reduktion des Wachstums und der Aktivierung von T-Lymphozyten.
Mehrere Studien, darunter randomisierte, kontrollierte klinische Studien, haben die Wirksamkeit von Ciclosporin A gezeigt. In einer randomisierten klinischen Studie, die Ciclosporin A mit einem Placebo bei Deutschen Schäferhunden mit Perianalfisteln verglich, wurde eine vollständige Auflösung der Läsionen bei 17 von 20 Hunden (85 %), die Ciclosporin A erhielten, nach 16 Behandlungswochen berichtet. Die mittlere Gesamtfläche und Tiefe der Läsionen nahmen nach 4 Wochen Therapie um 78 % bzw. 62 % ab.
Die für die Behandlung von Perianalfisteln untersuchten Dosen von Ciclosporin A variieren erheblich, von 1,5 mg/kg alle 24 Stunden bis zu 10 mg/kg alle 12 Stunden. Im Allgemeinen sind höhere Dosen mit besseren Ergebnissen verbunden, wobei die Wirksamkeit dosisabhängig ist. Modifizierte oder mikroemulgierte Formulierungen von Ciclosporin A haben eine höhere Bioverfügbarkeit bei Hunden und sollten bevorzugt eingesetzt werden. Die Bioverfügbarkeit von Ciclosporin A wird auch durch die Anwesenheit von Nahrung reduziert; es wird daher am besten auf nüchternen Magen (2 Stunden vor oder nach einer Mahlzeit) verabreicht.
Die Kosten für Ciclosporin A, insbesondere in hohen Dosen oder bei großen Hunden, können prohibitive sein. Die gleichzeitige Verabreichung von Ciclosporin A und Ketoconazol kann den Metabolismus von Ciclosporin A durch hepatische Cytochrom-P450-Mikroenzyme hemmen und dessen Bioverfügbarkeit durch Hemmung des intestinalen P-Glykoproteins (wodurch der Transport von Ciclosporin A in das Darmlumen verringert wird) verbessern. Die gleichzeitige Verabreichung beider Medikamente kann die Bioverfügbarkeit von Ciclosporin A um 75% oder mehr verbessern, je nach Ketoconazol-Dosis, und eine Reduzierung der Ciclosporin A-Dosis ermöglichen.
Die Kombination von Ciclosporin A (in Dosen von 1 mg/kg/Tag bis 5,5 mg/kg/Tag) und Ketoconazol (in Dosen von 5,1 mg/kg/Tag bis 11 mg/kg/Tag) hat sich in klinischen Studien als wirksam erwiesen, mit einer vollständigen Auflösung der Läsionen bei 93 % der Hunde innerhalb von 16 Wochen, bei 100 % der Hunde innerhalb von 3 bis 10 Wochen und bei 67 % der Hunde mit einer durchschnittlichen Auflösungszeit von 13,9 Wochen.
Rezidive können auftreten, wenn die immunmodulierende Behandlung abgesetzt wird. Aus diesem Grund wird nach vollständiger Auflösung der Läsionen (die in der Regel 8 bis 12 Wochen Behandlung erfordert) empfohlen, die Dosen von Ciclosporin A und Ketoconazol schrittweise auf die niedrigste wirksame Dosis und Verabreichungshäufigkeit zu reduzieren.
Tacrolimus
Tacrolimus-Salbe 0,1 % hat sich auch zur Behandlung von Perianalfisteln bei Hunden als wirksam erwiesen, obwohl randomisierte, kontrollierte klinische Studien nicht durchgeführt wurden. In einer Studie mit 10 Hunden, die über 16 Wochen zweimal täglich mit einer 0,1 %igen Tacrolimus-Salbe auf die perianale Haut behandelt wurden, erreichten 5 Hunde eine vollständige Auflösung der Läsionen.
Tacrolimus eignet sich aufgrund seines geringeren Molekulargewichts besser für die topische Anwendung als Ciclosporin A, da es besser durch die Epidermis absorbiert wird. Aufgrund der potenziell mit der Anwendung verbundenen Beschwerden wird Tacrolimus-Salbe in der Regel für Hunde mit leichten Läsionen oder für Hunde mit schwereren Läsionen nach vollständiger oder teilweiser Auflösung mit oralem Ciclosporin A (meist in Kombination mit Ketoconazol) empfohlen.
Einige Hunde können zur Erhaltung und Vorbeugung von erneuten perianalen Fisteln auf eine alleinige topische Tacrolimus-Salbe umgestellt werden. Der Hauptvorteil dieser topischen Behandlung ist die Vermeidung einer systemischen Immunsuppression.
Eine größere Studie zeigte eine vollständige Remission über 16 Wochen bei 15 von 19 Patienten (79 %) und eine deutliche Besserung bei den restlichen 4 Patienten, wenn Tacrolimus in Kombination mit Prednisolon, einer Proteinnahrung und einer kurzen Metronidazolkur angewendet wurde. Wenn Tacrolimus allein verabreicht wurde, wurde eine vollständige Remission nur bei 50 % der Patienten berichtet.
Glukokortikoide
Immunsuppressive Dosen von Prednisolon (2 bis 4 mg/kg PO alle 24 Stunden) wurden als wirksam beschrieben, wobei 33,3 % der Patienten eine vollständige Remission, 33,3 % eine Verbesserung der klinischen Symptome und 33,3 % keine Verbesserung zeigten. Ein Vorteil der Prednisolon-Therapie ist ihre schnelle Wirkung im Vergleich zu anderen immunsuppressiven Therapien; das Problem bei der Prednisolon-Therapie liegt in den Langzeitnebenwirkungen.
Aufgrund der Notwendigkeit einer kontinuierlichen Verabreichung immunmodulierender Wirkstoffe zur Behandlung sowie des Risikos von Nebenwirkungen bei langfristiger Verabreichung von Kortikosteroiden werden Kortikosteroide in der Regel nicht allein zur Behandlung von perianalen Fisteln bei Hunden eingesetzt. Sie können jedoch im Rahmen eines multimodalem Managements nützlich sein, insbesondere in der Anfangsphase aufgrund ihrer schnellen entzündungshemmenden Wirkung.
Andere Immunmodulatoren
Azathioprin
Azathioprin in Kombination mit Metronidazol hat sich als wirksam erwiesen, um die Größe von perianalen Fisteln vor der chirurgischen Entfernung des Restbefundes zu verringern. In den berichteten Fällen wurde Azathioprin 2 bis 6 Wochen nach der Operation fortgesetzt. Eine andere Studie zeigte, dass die Monotherapie mit Azathioprin bei etwas mehr als der Hälfte der Hunde zu einer vollständigen Remission führte. Azathioprin kann jedoch signifikante Nebenwirkungen (z. B. schwere Myelosuppression, Hepatotoxizität, Pankreatitis) verursachen, die bei der Anwendung dieses Medikaments berücksichtigt werden sollten.
In einer Studie von Harkin et al. wurden 14 Hunde mit perianalen Fisteln nur mit Azathioprin behandelt. Nach 16 Wochen Behandlung erreichten 8 von 14 Hunden (57 %) eine vollständige Auflösung der Läsionen.
Mycophenolat-Mofetil
Dem Autor ist nach bestem Wissen und Gewissen nur ein einziger Bericht über die Anwendung von Mycophenolat Mofetil zur Behandlung von Perianalfisteln in der Veterinärliteratur bekannt; dieser Hund wurde 4 Wochen lang ohne Verbesserung der Läsionen behandelt.
Alternative und aufkommende Therapien
Perianale Injektionen mit mesenchymalen Stammzellen
Injektionen von mesenchymalen Stammzellen, die direkt in die Fisteln verabreicht werden, haben sich beim Menschen mit fistulierendem Morbus Crohn als wirksam erwiesen. Mesenchymale Stammzellen haben eine immunmodulierende Aktivität, indem sie die Proliferation und Aktivierung von T-Lymphozyten und dendritischen Zellen reduzieren und die Produktion von regulatorischen T-Zellen erhöhen.
Die Wirksamkeit von Injektionen mesenchymaler Stammzellen bei Perianalfisteln bei Hunden wurde bei einer kleinen Anzahl von Hunden berichtet. Sechs Hunde mit Perianalfisteln, die auf die Standard-Ciclosporin-Therapie über mindestens 6 Monate nicht angesprochen hatten, wurden in eine offene Studie aufgenommen und erhielten eine Einzeldosis mesenchymaler Stammzellen, die aus humanen embryonalen Stammzellen gewonnen wurden, in die Perianalläsionen injiziert. Die Hunde wurden 6 Monate nach der Injektion überwacht; alle Hunde zeigten 3 Monate nach der Stammzellinjektion eine Auflösung der Sinusgänge oder Ulzera. Zwei Hunde zeigten 6 Monate nach der Injektion ein Rezidiv der Perianalfisteln.
Nach 1 bis 2 Monaten konnte die durchschnittliche Ciclosporin-Dosis auf 3,59 mg/kg/Tag (nach 3 Monaten) gegenüber den anfänglichen 8,22 mg/kg/Tag reduziert werden. Obwohl Injektionen mesenchymaler Stammzellen eine vielversprechende Behandlungsoption für Perianalfisteln bei Hunden darstellen, sind weitere kontrollierte Studien erforderlich, um diese Ergebnisse auf größere Populationen betroffener Hunde zu übertragen und die optimale Häufigkeit der Injektionen zu bestimmen.
Andere innovative Therapien
Mehrere alternative Therapien, die auf die Wundheilung abzielen, sind als Behandlungsoptionen für perianale Fisteln populär geworden.
-
Plättchenreiches Plasma: Eine Monotherapie mit plättchenreichem Plasma, das als intraläsionale Injektionen bei einem Hund verabreicht wurde, führte zu einer vollständigen Remission ohne Rezidiv nach einem Jahr.
-
Fluoreszierende Lichtenergie: Diese Therapie erfordert eine wöchentliche Behandlung, um Entzündungen zu reduzieren und die Wundheilung zu fördern. Eine Fallstudie mit 4 Fällen zeigte nach 6 Wochen eine Reduzierung der Läsionsfläche um 74,3 %, obwohl keine vollständige Heilung beobachtet wurde. Die jüngste Kommerzialisierung der fluoreszierenden Lichtenergie hat sie für Tierärzte leichter verfügbar gemacht.
-
Oclacitinib: Eine kürzlich veröffentlichte Fallserie berichtete über die Anwendung von Oclacitinib in höheren Dosen als bei atopischer Dermatitis (1,125 mg/kg BID und 0,88 mg/kg BID) mit einer vollständigen Heilung in beiden Fällen nach 1 Monat Behandlung. Dieses Medikament blockiert die Wirkung von Interferonen und den JAK-STAT-Signalweg, was es angesichts der Interferon-Aktivierung bei perianalen Fistelläsionen zu einer relevanten ätiologischen Behandlung machen könnte.
Adjuvante Behandlungen und ergänzende Überlegungen
Behandlung sekundärer Infektionen
Sekundärinfektionen können perianale Fisteln begleiten und müssen angemessen behandelt werden, entweder durch systemische Medikamente oder durch topische Anwendungen (Chlorhexidin). Eine routinemäßige Hygienepflege der perianalen Region kann vorteilhaft sein (z. B. antiseptische Bäder 2 bis 3 Mal pro Woche, je nach Schwere der Läsionen sogar täglich).
Es ist wichtig zu beachten, dass Antibiotika allein bei der Behandlung von perianalen Fisteln bei Hunden nicht wirksam zu sein scheinen. Viele Hunde werden zum Zeitpunkt des Auftretens klinischer Anzeichen von perianalen Fisteln mit Antimikrobika behandelt, zeigen aber weiterhin eine Krankheitsprogression.
Einige Studien berichteten über die Anwendung von Metronidazol in Kombination mit anderen Therapien (Azathioprin, Tacrolimus-Salbe, Prednisolon und eine Diät auf Basis neuer Proteine) zur Behandlung von Hunden mit perianalen Fisteln. Zusätzlich zu seiner Aktivität gegen anaerobe Bakterien und Protozoen kann Metronidazol auch eine entzündungshemmende Wirkung haben, insbesondere durch die Förderung der Differenzierung regulatorischer T-Zellen. Diese entzündungshemmende Wirkung kann zur Behandlung immunvermittelter Krankheiten beitragen, aber die Wirksamkeit von Metronidazol allein zur Behandlung von perianalen Fisteln ist bisher unbekannt.
Schmerz- und Komfortmanagement
Hunde mit aktiven perianalen Fisteln können Schmerzen haben, insbesondere beim Stuhlgang. Stuhlweichmacher sollten in Betracht gezogen werden, und in einigen Fällen können Einläufe zur Linderung des Tenesmus erforderlich sein. Die Analgesie sollte bei Hunden mit aktiven Läsionen oberste Priorität haben, aber das Potenzial für Verstopfung bei der Anwendung bestimmter Analgetika, wie z. B. Opioid-Agonisten, sollte bei der Erstellung eines Schmerzmanagementplans berücksichtigt werden.
Ernährungs Überlegungen
Ein Zusammenhang zwischen perianalen Fisteln und unerwünschten Futtermittelreaktionen wurde identifiziert. In einer Studie litten 18,8 % der Hunde mit perianalen Fisteln auch an Futtermittelallergien. Es ist unklar, ob ein direkter Zusammenhang zwischen diesen Krankheiten besteht oder ob die Hunde einfach zwei gleichzeitig auftretende Krankheiten hatten. Wie auch immer, die Verwendung einer Diät auf Basis neuer Proteine oder einer hydrolysierten Diät war für einige Patienten von Vorteil.
Drei Studien berichteten über eine positive klinische Reaktion auf eine neue Proteindiät bei Hunden mit Perianalfisteln. In einer Studie wurde eine Fisch- und Kartoffeldiät langfristig nach chirurgischer Exzision der Sinusgänge und bilateraler Analsakkulektomie verabreicht. In der zweiten Studie erhielten die Hunde eine exklusive Wild- und Kartoffel- oder Fisch- und Kartoffeldiät, erhielten aber anfangs auch Metronidazol sowie 0,1 % Tacrolimus-Salbe topisch und eine ausschleichende orale Prednisolonkur über 16 Wochen. In der dritten Studie erhielten die Hunde eine handelsübliche Lamm- und Reis- oder vegetarische Diät, erhielten aber gleichzeitig eine ausschleichende orale Prednisolonkur in einer anfänglichen immunsuppressiven Dosis.
Obwohl die Einführung einer Ausschlussdiät mit einem Futter auf Basis neuer Proteine oder hydrolysierter Proteine im Rahmen der diagnostischen Abklärung von Hunden mit perianalen Fisteln empfohlen wird, ist aus der verfügbaren Literatur nicht klar, wie viele Hunde mit alleiniger Ernährungskontrolle eine langfristige Remission erreichen können.
Konsensuale Empfehlungen für das Management von Perianalfisteln
Methodik der Konsensfindung
Angesichts des Mangels an Konsens über die Behandlung von Perianalfisteln hat der wissenschaftliche Beirat des GEDAC (Groupe d’Étude en Dermatologie des Animaux de Compagnie) eine Bestandsaufnahme der Literatur vorgenommen, um Empfehlungen für das medizinische Management zu erarbeiten.
Die gewählte Methodik basiert auf der Taxonomie der Empfehlungsstärke (SoRT), die von den Redakteuren von Fachzeitschriften für Allgemeinmedizin und Notfallmedizin in den Vereinigten Staaten entwickelt wurde. Das Evidenzniveau (LoE) wurde in einer dreistufigen Skala klassifiziert:
- LoE 1: Gute Evidenz (Metaanalyse, hochwertige randomisierte kontrollierte prospektive Studie)
- LoE 2: Begrenzte Evidenz (randomisierte kontrollierte prospektive Studie geringer Qualität, kontrollierte Studie, Fallstudie versus Kontrollgruppe, hochwertige prospektive Studie)
- LoE 3: Sonstige Evidenz, einschließlich Konsensrichtlinien, Meinungen, Fallstudien
Es wurde eine systematische Literaturrecherche in der PubMed-Datenbank für Artikel, die zwischen 1980 und Oktober 2023 veröffentlicht wurden, durchgeführt. Es wurden Artikel in Englisch und Französisch mit spezifischen Schlüsselwörtern gesucht, und folgende Studiengypen wurden anfänglich ausgewählt: randomisierte kontrollierte Studien, klinische Studien, Kohortenstudien und Fallserien.
Für die Erarbeitung der Empfehlungen wurde eine dreistufige Skala verwendet:
- Stufe A: Starke Empfehlung, basierend auf hochwertigen, konsistenten Beweisen
- Stufe B: Moderate Empfehlung, basierend auf inkonsistenten oder begrenzten Beweisen
- Stufe C: Schwache Empfehlung, hauptsächlich basierend auf Expertenmeinung
Wichtige therapeutische Empfehlungen
Ciclosporin A
- Die Wirksamkeit von Ciclosporin ist real (Empfehlungsniveau A)
- Die Wirksamkeit ist dosisabhängig und unabhängig vom klinischen Schweregrad
- Die empfohlene Mindestdosis beträgt 5 mg/kg/Tag, kann aber bis zu 10 mg/kg zweimal täglich betragen
- Die wirksame Dosis sollte bis zur klinischen Heilung beibehalten werden (Niveau C)
- Drei Monate können erforderlich sein, um die Heilung unter Ciclosporin zu beobachten
Kombination Ciclosporin-Ketoconazol
- Diese Kombination ist wirksam.
- Experten empfehlen diese Kombination jedoch nicht, um das Risiko von Antimykotika-Resistenzen und Leberschäden zu begrenzen.
Tacrolimus
In Frankreich erschwert die Entwicklung der Gesetzgebung die Anwendung von Tacrolimus.
Prednisolon
- Experten empfehlen die alleinige Anwendung von Prednisolon nicht.
- Die Kortikosteroidtherapie wird im Rahmen eines multimodalen Managements empfohlen.
- Es wird empfohlen, eine Anfangsdosis von 1 mg/kg/Tag nicht zu überschreiten, um Nebenwirkungen zu begrenzen.
- Die lokale Kortikosteroidtherapie könnte trotz fehlender solider wissenschaftlicher Daten in dieser Hinsicht interessant sein.
Andere Immunmodulatoren
Experten empfehlen die Anwendung von Azathioprin, Mycophenolat Mofetil, Oclacitinib, Photobiomodulation oder Stammzellen aufgrund fehlender zuverlässiger und wiederholter Daten nicht.
Antibiotikatherapie
- Eine Antibiotikatherapie ist zur Heilung nicht notwendig.
- Metronidazol wurde in Studien wenig eingesetzt, was es schwierig macht, seine Auswirkungen auf den Krankheitsverlauf zu beurteilen.
- Experten empfehlen den systematischen Einsatz von Antibiotika nicht.
- Eine Antibiotikatherapie wird nur bei rektalen Fisteln oder Infektionen der Analsäcke empfohlen, basierend auf den Ergebnissen einer Bakterienkultur.
Chirurgischer Ansatz
- Die Experten empfehlen den chirurgischen Eingriff als Zweitlinientherapie.
- Dieser Ansatz ist bei einem Tier angezeigt, das nach einer Besserung durch medizinische Behandlung weiterhin Beschwerden oder Schmerzen (beeinträchtigte Lebensqualität) hat.
- Der Einsatz der Chirurgie kann durch budgetäre Gründe oder eine Stagnation der klinischen Besserung bei einem Tier, dessen Lebensqualität unzureichend bleibt, bedingt sein.
Ernährung
- Es gibt keine wissenschaftlichen Belege, die die Verwendung von diätetischen Lebensmitteln auf Basis neuer oder hydrolysierter Proteine empfehlen.
- In Analogie zur Crohn-Krankheit beim Menschen und auf der Grundlage klinischer Erfahrung raten Experten zur Einführung einer hypoallergenen Ernährung (Niveau C).
Nachbehandlung und Therapieanpassung
- Es wird empfohlen, die medikamentöse Behandlung nach 6 bis 10 Wochen zu evaluieren und je nach Ansprechen anzupassen.
- Nach Erreichen der Heilung oder bei moderat persistierenden Läsionen mit guter Lebensqualität kann die Behandlung vereinfacht oder sogar abgesetzt werden.
- Mangels wissenschaftlicher Daten befürworten Experten eine schrittweise und angepasste Vereinfachung oder Beendigung der Behandlung.
Diskussion und Ausblick
Parallelen zu menschlichen Pathologien
Zwei menschliche Erkrankungen, die Hidradenitis suppurativa und die fistulierende Morbus Crohn, wurden als Entsprechungen von Perianalfisteln bei Hunden vorgeschlagen. Wie Perianalfisteln bei Hunden sind diese beiden Erkrankungen schmerzhaft, behindernd und können sich negativ auf die Lebensqualität der Patienten auswirken.
Hidradenitis suppurativa ist mit Knötchen, Abszessen, Sinusgängen und Narben verbunden, hauptsächlich in intertriginösen Regionen (Achselhöhle, Leiste, perianale Region und Brustregion). Sie wurde ursprünglich als potenzielles Korrelat von Perianalfisteln bei Hunden vorgeschlagen, da ähnliche histopathologische Merkmale vorliegen, darunter Furunkulose, Hidradenitis und die Bildung von mit Epithel ausgekleideten Sinusgängen. Die Pathogenese der Hidradenitis suppurativa ist noch nicht vollständig geklärt, aber es handelt sich wahrscheinlich um eine immunvermittelte Erkrankung mit einer genetischen Veranlagung. Veränderungen des Haut- oder Darmmikrobioms könnten eine Rolle in der Pathogenese spielen.
Perianale Manifestationen von Morbus Crohn sind häufig und betreffen schätzungsweise 25 % bis 33 % der Patienten mit Morbus Crohn. Perianale Fisteln sind häufiger bei Patienten mit kolischen oder rektalen Erkrankungen und können einfach (ein Fistelgang mit einer einzigen externen Öffnung) oder komplex (multiple Fistelgänge, perianale Abszesse oder anale/rektale Stenose) sein. Im Gegensatz zur typischen Erkrankung bei Hunden handelt es sich um echte Fisteln, die mit dem Darmlumen kommunizieren. Die Pathogenese von Perianalfisteln bei Morbus Crohn ist nicht vollständig verstanden, scheint aber eine epithelial-mesenchymale Transition und eine Hochregulierung von Matrix-Metalloproteinasen und proinflammatorischen Zytokinen zu beinhalten.
Ähnlichkeiten in der Pathogenese der Hidradenitis suppurativa und Morbus Crohn wurden aufgezeigt, insbesondere die Infiltration von erkranktem Gewebe durch T-Helferzellen vom Typ 17. Zukünftige Studien sollten sich auf eine bessere Charakterisierung der zugrunde liegenden Ätiologie dieser drei Erkrankungen konzentrieren und könnten dazu beitragen, die Entwicklung zukünftiger Therapien, wie z. B. Antikörper, die auf spezifische Zytokine abzielen, für perianale Fisteln bei Hunden zu lenken.
Zukünftige Perspektiven und Forschungsansätze
Mehrere Forschungsbereiche verdienen besondere Aufmerksamkeit, um die Behandlung von Perianalfisteln bei Hunden zu verbessern:
-
Vertiefte Untersuchung der Immunpathogenese: Ein besseres Verständnis der beteiligten immunvermittelten Mechanismen könnte zur Entwicklung gezielter Therapien führen, beispielsweise der Anwendung von JAK-Inhibitoren (Oclacitinib), deren Wirksamkeit durch einige vorläufige Studien nahegelegt wurde.
-
Charakterisierung des Haut- und Darmmikrobioms: Die Erforschung der Rolle des Mikrobioms bei der Entstehung und Persistenz von Perianalfisteln könnte neue therapeutische Ansätze eröffnen, wie die Anwendung von Probiotika oder die fäkale Transplantation.
-
Optimierung der Therapieprotokolle: Kontrollierte Studien sind erforderlich, um die optimalen Dosen, Behandlungsdauern und Absetzstrategien der verschiedenen Therapieoptionen zu bestimmen.
-
Standardisiertere Bewertung der Lebensqualität: Die Entwicklung spezifischer Instrumente zur Bewertung der Auswirkungen von Perianalfisteln und deren Behandlungen auf die Lebensqualität von Hunden würde einen tiergerechteren Ansatz ermöglichen.
-
Entwicklung innovativer Therapien: Die vielversprechenden vorläufigen Ergebnisse, die mit mesenchymalen Stammzellen, plättchenreichem Plasma oder fluoreszierender Lichtenergie erzielt wurden, müssen durch kontrollierte Studien an größeren Populationen weiter untersucht werden.
-
Untersuchung der Zusammenhänge mit Nahrungsmittelallergien: Die Klärung potenzieller Zusammenhänge zwischen Perianalfisteln und unerwünschten Nahrungsmittelreaktionen würde eine Optimierung der Ernährungsansätze ermöglichen.
- Identifizierung prädiktiver Biomarker: Die Suche nach biologischen Markern, die eine Vorhersage des Therapieansprechens oder des Rezidivrisikos ermöglichen, würde die personalisierte Therapie verbessern.
Bedeutung eines individualisierten Ansatzes
Die Behandlung von Perianalfisteln bei Hunden erfordert einen individualisierten Ansatz, der mehrere Faktoren berücksichtigt:
-
Therapeutisches Gleichgewicht: Das Finden eines Gleichgewichts zwischen Behandlungswirksamkeit, Kosten, Nebenwirkungen und Lebensqualität des Tieres ist unerlässlich.
-
Realistische Ziele: Obwohl die vollständige klinische Heilung das theoretische Ziel bleibt, kann eine klinische Verbesserung mit erhaltener Lebensqualität in einigen Fällen ein akzeptables Ziel darstellen.
-
Therapeutische Anpassungsfähigkeit: Die regelmäßige Bewertung des Therapieansprechens und die Anpassung der Protokolle an dieses Ansprechen sind entscheidend, um das Management zu optimieren.
-
Multimodaler Ansatz: Die Kombination verschiedener therapeutischer Modalitäten (immunmodulierende Medikamente, lokale Pflege, Schmerzmanagement, Ernährungsansatz) bietet oft die besten Erfolgsaussichten.
-
Berücksichtigung des Kontextes: Finanzielle Zwänge, die Fähigkeit des Besitzers, die Behandlungen zu verabreichen und die notwendigen Maßnahmen durchzuführen, sowie mögliche Komorbiditäten müssen in die therapeutische Strategie integriert werden.
Fazit
Perianale Fisteln bei Hunden stellen eine komplexe dermatologische Erkrankung mit immunvermittelter Pathogenese dar, deren Prävalenz bei Deutschen Schäferhunden besonders hoch ist. Diese potenziell invalidisierende Pathologie kann die Lebensqualität betroffener Tiere erheblich beeinträchtigen und erfordert eine schnelle und angepasste Behandlung.
Das Verständnis dieser Krankheit hat sich im Laufe der Jahrzehnte erheblich weiterentwickelt, mit einem Paradigmenwechsel von einer hauptsächlich anatomischen und chirurgischen Sichtweise hin zu einem immunvermittelten und medizinischen Ansatz. Immunmodulierende Therapien, insbesondere Ciclosporin A, bilden heute den Eckpfeiler der Behandlung und ermöglichen signifikante Heilungsraten.
Die methodische Analyse der wissenschaftlichen Literatur hat konsensuale Empfehlungen zur Orientierung für Kliniker bei ihren therapeutischen Entscheidungen ermöglicht. Diese Empfehlungen unterstreichen die Wirksamkeit von Ciclosporin A in angepassten Dosen (mindestens 5 mg/kg/Tag), die begrenzte, aber ergänzende Rolle der Kortikosteroidtherapie und das potenzielle Interesse einiger aufkommender Therapien wie Oclacitinib oder mesenchymale Stammzellen.
Die Chirurgie, einst als Referenzbehandlung angesehen, ist heute auf refraktäre Fälle oder als Ergänzung nach medizinischer Stabilisierung beschränkt. Der Ernährungsansatz, obwohl noch keine soliden wissenschaftlichen Beweise vorliegen, wird oft in die gesamte Therapiestrategie integriert.
Die festgestellten Parallelen zu menschlichen Pathologien wie Hidradenitis suppurativa oder fistulierendem Morbus Crohn eröffnen interessante Perspektiven für die translationale Forschung und die Entwicklung neuer gezielter Therapieansätze.
Das letztendliche Ziel der Behandlung bleibt die Verbesserung der Lebensqualität des Tieres, was manchmal auch ohne vollständige Heilung der Läsionen erreicht werden kann. Ein individualisierter Ansatz, der die Besonderheiten jedes Patienten, praktische Einschränkungen und die Erwartungen der Besitzer berücksichtigt, bleibt entscheidend, um die Erfolgschancen der langfristigen Therapie zu optimieren.
Häufig gestellte Fragen
1. Beeinflusst die anfängliche Schwere der Läsionen die Prognose und das Ansprechen auf die Behandlung?
Studien haben keine signifikante Korrelation zwischen der anfänglichen Schwere der Läsionen und dem Ansprechen auf die Behandlung, insbesondere mit Ciclosporin, gezeigt. Eine frühzeitige Diagnose und die rasche Einleitung einer geeigneten Behandlung verbessern jedoch im Allgemeinen die Prognose. Chronische Fälle mit etablierter Fibrose können therapieresistenter sein.
2. Wie geht man mit Rezidiven nach Absetzen der Behandlung um?
Im Falle eines Rezidivs nach Absetzen der Behandlung wird in der Regel die Fortsetzung des ursprünglich wirksamen Protokolls empfohlen. Sobald die Remission erreicht ist, kann ein schrittweiserer Entzug in Betracht gezogen werden, oder eine Erhaltungstherapie mit der niedrigsten wirksamen Dosis (z. B. Ciclosporin in reduzierter Dosis oder topisches Tacrolimus) kann langfristig aufrechterhalten werden. Die Identifizierung und Behandlung potenzieller Auslösefaktoren, wie z. B. Nahrungsmittelallergien, ist ebenfalls wichtig.
3. Beeinflussen Umweltfaktoren den Verlauf von Perianalfisteln?
Obwohl wenig spezifisch untersucht, scheint einige Umweltfaktoren den Krankheitsverlauf zu beeinflussen. Die perianale Hygiene, die Stuhlkonsistenz (beeinflusst durch die Ernährung), Stress und körperliche Aktivität können alle einen Einfluss auf die Heilung und den Komfort des Tieres haben. Eine saubere Umgebung und regelmäßige lokale Pflege tragen positiv zur Behandlung der Erkrankung bei.
4. Welche Risiken von Langzeitnebenwirkungen haben immunsuppressive Behandlungen?
Langfristige immunsuppressive Behandlungen bergen mehrere Risiken:
- Bei Ciclosporin: Verdauungsstörungen, Gingivahyperplasie, Hirsutismus, erhöhtes Risiko opportunistischer Infektionen und potenzielle (seltene) Neoplasieentwicklung
- Bei Kortikosteroiden: iatrogene Cushing-Syndrom, Diabetes mellitus, Hautatrophie, Immunsuppression, Risiko sekundärer Infektionen
- Bei Azathioprin: Myelosuppression, Hepatotoxizität, Pankreatitis
Eine regelmäßige Überwachung, einschließlich klinischer Untersuchung, Blutanalysen und Dosisanpassungen, ist unerlässlich, um diese Risiken zu minimieren.
5. Gibt es Möglichkeiten vorherzusagen, welche Deutschen Schäferhunde diese Erkrankung entwickeln werden?
Derzeit gibt es keinen validierten prädiktiven Test, der mit Sicherheit Deutsche Schäferhunde identifizieren kann, die ein Risiko für die Entwicklung von perianalen Fisteln haben. Es wurden jedoch einige Risikofaktoren identifiziert:
- Hunde, die homozygot für das Allel DLA-DRB1*00101 sind, könnten die Krankheit früher entwickeln.
- Eine Familienanamnese von perianalen Fisteln scheint das Risiko zu erhöhen.
- Bestimmte Linien scheinen stärker betroffen zu sein als andere.
Weitere Forschungen zu genetischen und immunologischen Markern könnten die Entwicklung prädiktiver Tests in Zukunft ermöglichen und den Weg für präventive Strategien bei Risikopersonen ebnen.