Die Plasmazelluläre Pododermatitis ist eine seltene und wenig verstandene Dermatose der Katze, die in der Konsultation jedoch nicht vernachlässigt werden darf, insbesondere wegen der Schmerzen und damit der Lahmheit, die sie verursachen kann. Ein Überblick über die neuesten Erkenntnisse, sowohl hinsichtlich der Ätiopathogenese als auch der Diagnostik und der jüngsten veröffentlichten Behandlungen und Protokolle.
Einleitung und nosologischer Rahmen
1.1. Definition und Benennung
Die plasmazelluläre Pododermatitis der Katze (PPF) stellt eine seltene entzündliche Dermatose dar, die durch eine massive Infiltration reifer Plasmazellen in der Dermis der Katzenballen gekennzeichnet ist. Diese Erkrankung, umgangssprachlich unter dem englischen Begriff pillow foot aufgrund des geschwollenen und weichen Aussehens der betroffenen Ballen bezeichnet, nimmt eine besondere Stellung im veterinärdermatologischen Spektrum ein (Miller 2013). Die Erkrankung zeichnet sich durch ihren ausschließlichen Tropismus für das Ballengewebe aus, ohne genaues Äquivalent beim Hund oder Menschen, obwohl pathophysiologische Parallelen zu bestimmten plasmazellulären Hautproliferationen beim Menschen gezogen werden können. Nosologisch gehört die PPF zur Gruppe der plasmazellulären Dermatosen der Katze, einem Spektrum, das die chronische plasmazelluläre Stomatitis und, umstrittener, bestimmte Formen der extrapodalaren plasmazellulären Dermatitis umfasst (Gross 2005). Das Infiltrat besteht zu mehr als 90 % aus gut differenzierten Plasmazellen, die den Marker CD138 (Syndecan-1) exprimieren, was sie formal von plasmazellulären Neoplasien wie dem extramedulären Plasmozytom unterscheidet, bei dem der Proliferationsindex Ki-67 üblicherweise 20 % überschreitet (Mauldin 2016).
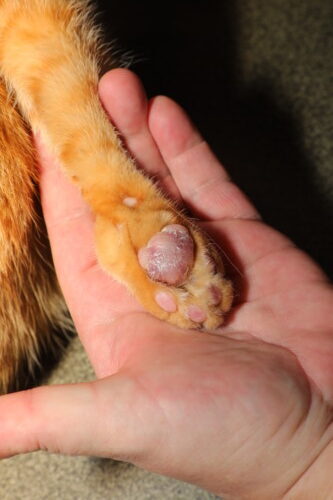
Klassisches Aussehen einer plasmazellulären Pododermatitis der Katze
1.2. Historische Meilensteine und Entwicklung der Erkenntnisse
Die ersten klinisch-pathologischen Beschreibungen der PPF stammen aus dem Ende der 1970er Jahre, als Gruffydd-Jones, Orr und Lucke 1980 eine Serie von fünf Katzen mit Schwellung und Ulzeration der Ballen in Verbindung mit einer dichten dermalen plasmazellulären Infiltration veröffentlichten (Gruffydd-Jones 1980). Diese grundlegende Publikation etablierte die morphologischen Basiskriterien, die noch heute die Erkennung der Erkrankung leiten. Im Laufe des folgenden Jahrzehnts berichteten Taylor und Schmeitzel 1990 über zwei Fälle, die durch chronische Blutungen im Ballenbereich kompliziert wurden, und unterstrichen das evolutive Potenzial der Erkrankung hin zur tiefen Ulzeration und vaskulären Fragilisierung (Taylor 1990). Die Verfügbarkeit serologischer Tests für das feline Immundefizienzvirus (FIV) in den 1990er Jahren ermöglichte es, einen statistischen Zusammenhang zwischen Retrovirusinfektionen und PPF aufzuzeigen, eine Verbindung, die in mehreren retrospektiven Serien untersucht wurde und eine FIV-Seroprävalenz von 20 bis 62 % bei betroffenen Katzen im Vergleich zu 2 bis 4 % in der allgemeinen Katzenpopulation zeigte (Guaguère 2004; Dias Pereira 2003). Die retrospektive Studie von Guaguère und Mitarbeitern mit 26 Fällen stellt bis heute eine der größten veröffentlichten Kohorten dar und hat zum Verständnis des epidemiologischen Profils und des therapeutischen Ansprechens beigetragen (Guaguère 2004). Die Einführung von Doxycyclin als Erstlinientherapie Anfang der 2000er Jahre stellte einen therapeutischen Wendepunkt dar und bot eine Alternative zur Langzeit-Kortikosteroidtherapie mit einer vollständigen Ansprechrate von etwa 50 bis 65 % je nach Serie (Bettenay 2003).
Epidemiologie
2.1. Prävalenz und Inzidenzdaten
Die PPF bleibt eine seltene Erkrankung, deren genaue Prävalenz schwer zu bestimmen ist, teilweise aufgrund einer wahrscheinlichen Unterdiagnose aufgrund der spontanen Auflösung einiger benigner Formen. Die verfügbaren Daten aus veterinärdermatologischen Referenzzentren schätzen ihre Häufigkeit auf 0,5 bis 1,5 % aller dermatologischen Konsultationen bei Katzen (Miller 2013). In der Serie von Dias Pereira und Faustino, die 8 über einen Zeitraum von sieben Jahren in einem portugiesischen Universitätszentrum diagnostizierte Fälle analysierte, wird die jährliche Inzidenz auf etwa 1,1 Fälle pro 1.000 Katzenkonsultationen geschätzt (Dias Pereira 2003). Diese relative Seltenheit schließt eine unterschätzte Prävalenz in der Routinepraxis nicht aus, da frühe nicht ulzerierte Stadien häufig unbemerkt bleiben. Es wurden keine signifikanten geografischen Unterschiede berichtet, Fälle wurden auf allen Kontinenten dokumentiert, von Europa über Nordamerika bis Asien und Australien (Hnilica 2017). Der sporadische Charakter der Erkrankung ohne zeitliches oder räumliches Clustering spricht gegen eine direkt übertragbare infektiöse Ätiologie und weist eher auf eine individuelle dysimmunitäre Pathogenese hin.
2.2. Demografische Risikofaktoren: Rasse, Alter und Geschlecht
Im Gegensatz zu vielen felinen Dermatosen, für die ein genetischer Determinismus identifiziert wurde – beispielsweise das PNPLA1-Gen bei der Ichthyose des Golden Retrievers oder das KRT10-Gen bei der epidermolytischen Ichthyose –, wurde für die PPF keine klare Rasseprädisposition nachgewiesen (Miller 2013). Die Mehrheit der berichteten Fälle betrifft Europäisch-Kurzhaar-Katzen, was die Vorherrschaft dieser Population in tierärztlichen Konsultationen widerspiegelt und nicht eine spezifische genetische Suszeptibilität. Die Kohorte von Guaguère umfasste 23 europäische Katzen von 26 (88,5 %), die drei verbleibenden waren ein Perser, ein Siamese und ein Chartreux (Guaguère 2004). Die Analyse der Serie von Dias Pereira bestätigt diese fehlende Rasseprädisposition mit einer proportionalen Verteilung zur Referenzpopulation (Dias Pereira 2003).
Das Alter zum Zeitpunkt der Diagnose variiert erheblich, von 6 Monaten bis 14 Jahren, mit einem Median zwischen 4 und 7 Jahren je nach Studie (Gross 2005; Guaguère 2004). Diese breite Altersspanne deutet darauf hin, dass die Erkrankung weder einer juvenilen Entwicklungserkrankung noch einer strikt geriatrischen Pathologie entspricht, sondern jederzeit im Erwachsenenleben auftreten kann, abhängig vom Zusammentreffen individueller immunologischer Faktoren. Bezüglich des Geschlechts bleiben die Daten widersprüchlich. Einige Serien berichten von einer leichten Prädominanz für Männchen mit einem Geschlechterverhältnis von 1,4:1 zugunsten der Männchen (Guaguère 2004), während andere keinen signifikanten Unterschied finden. Der Fortpflanzungsstatus (intakt oder kastriert) scheint keinen entscheidenden Einfluss auszuüben, obwohl die meisten in Studien eingeschlossenen Katzen kastriert sind, entsprechend den Praktiken des Katzenmanagements in Industrieländern. Das Fehlen eines identifizierten genetischen Polymorphismus, der mit der PPF assoziiert ist, steht im Gegensatz zu anderen felinen Immundermatosen, wie dem eosinophilen Granulom-Komplex, bei dem polygene genetische Faktoren vermutet wurden, und stärkt die Hypothese einer erworbenen Pathogenese mit Umwelt- oder infektiösen Kofaktoren.
Ätiopathogenese: eine multifaktorielle Immundysregulation
3.1. Argumente für einen dysimmunitären Ursprung
Die Ätiologie der PPF bleibt bis heute unvollständig geklärt, aber alle klinischen, biologischen und histopathologischen Daten konvergieren zu einer immun-vermittelten Pathogenese. Mehrere Argumente stützen diese Hypothese. Das erste beruht auf der Natur des Infiltrats selbst, das fast ausschließlich aus reifen polyklonalen Plasmazellen besteht, Indikatoren einer chronischen und anhaltenden Antigen-Aktivierung des B-Lymphozyten-Kompartiments. Die immunhistochemische Analyse zeigt, dass diese Plasmazellen sowohl Kappa- als auch Lambda-Leichtketten der Immunglobuline in einem physiologischen Verhältnis von etwa 2:1 exprimieren, was einen monoklonalen neoplastischen Prozess ausschließt (Gross 2005; Mauldin 2016). Das zweite Argument ergibt sich aus der polyklonalen Hypergammaglobulinämie, die bei 50 bis 63 % der betroffenen Katzen dokumentiert ist und eine diffuse Stimulation des humoralen Immunsystems ohne identifizierte antigene Spezifität bezeugt (Guaguère 2004). Die Serumprotein-Elektrophorese zeigt eine Erhöhung der Gamma-Fraktionen ohne monoklonalen Peak, was diese Erkrankung formal von einem multiplen Myelom oder einem sekretierenden Plasmozytom unterscheidet. Schließlich stellt das günstige Ansprechen auf immunmodulierende oder immunsuppressive Wirkstoffe – Doxycyclin, Glukokortikoide, Ciclosporin – ein indirektes therapeutisches Argument für einen dysimmunitären Mechanismus dar (Bettenay 2003; Miller 2013).
Der Nachweis von antinukleären Antikörpern (ANA) bei einem nicht unerheblichen Anteil betroffener Katzen, geschätzt auf 25 bis 50 % je nach Serie, stärkt die Autoimmunhypothese, obwohl die klinische Bedeutung dieser ANA in der Katzenmedizin umstritten bleibt (Dias Pereira 2003). Ihr Vorhandensein könnte eine unspezifische lymphozytäre Aktivierung widerspiegeln und keine echte autoreaktive Reaktion. Die direkte Immunfluoreszenz-Analyse von Ballenbiopsien hat Ablagerungen von IgG, IgM und der Komplementfraktion C3 an der dermo-epidermalen Junktion und um dermale Gefäße bei einer Mehrheit der Fälle nachgewiesen, ein Muster, das auf eine Immunkomplex-Erkrankung hinweist (Gross 2005). Diese Ablagerungen erinnern an diejenigen, die beim felinen systemischen Lupus erythematodes beobachtet werden, und legen einen teilweise geteilten pathophysiologischen Mechanismus nahe, der den klassischen Komplementweg durch Fixierung des C1q-Fragments an Antigen-Antikörper-Komplexe einbezieht.
3.2. Beteiligung des felinen Immundefizienzvirus und der Retroviren
Der Zusammenhang zwischen PPF und FIV-Infektion stellt einen der am meisten diskutierten Aspekte der Ätiopathogenese dar. Mehrere retrospektive Studien berichten von einer signifikant höheren FIV-Seroprävalenz bei Katzen mit PPF als in der Allgemeinbevölkerung. In der Serie von Guaguère waren 50 % der 26 getesteten Katzen FIV-seropositiv, eine Rate, die deutlich über der erwarteten Prävalenz von 2 bis 4 % in der europäischen häuslichen Katzenpopulation liegt (Guaguère 2004). Dias Pereira und Faustino fanden eine Seroprävalenz von 62,5 % in ihrer Kohorte von 8 Fällen (Dias Pereira 2003). FIV, ein Lentivirus der Familie Retroviridae, verursacht eine tiefgreifende Dysregulation der adaptiven Immunität durch progressive Depletion von CD4+ T-Lymphozyten und durch chronische polyklonale Aktivierung der B-Lymphozyten. Dieses Phänomen wird durch direkte Stimulation des Toll-like-Rezeptors 7 (TLR7) durch einzelsträngige virale RNA und durch aberrante IL-6-Sekretion vermittelt und begünstigt die plasmazelluläre Differenzierung und die Produktion unspezifischer Immunglobuline (Hartmann 2012). Die Aktivierung des JAK1/STAT3-Wegs unterhalb des IL-6-Rezeptors stellt einen Schlüsselmechanismus dieser übermäßigen Plasmazellbildung dar, wobei der phosphorylierte Transkriptionsfaktor STAT3 in den Kern transloziert, um die Expression von BLIMP-1 (PRDM1), dem Hauptregulator der terminalen Differenzierung von B-Lymphozyten zu Plasmazellen, zu induzieren (Nutt 2015).
Der Zusammenhang mit dem felinen Leukämievirus (FeLV) ist weniger gut dokumentiert, mit Seroprävalenzraten zwischen 0 und 20 % je nach Kohorte, Zahlen, die sich nicht immer signifikant von der Referenzpopulation unterscheiden (Guaguère 2004; Miller 2013). Die PPF kann jedoch bei Katzen auftreten, die sowohl für FIV als auch für FeLV seronegativ sind, was darauf hinweist, dass die retrovirale Infektion weder notwendig noch ausreichend ist, um die Erkrankung auszulösen. Sie wirkt wahrscheinlich als verstärkender Kofaktor einer bereits bestehenden Immundysregulation, indem sie die Toleranzschwelle senkt und den Bruch der Homöostase des B-Kompartiments begünstigt.
3.3. Vermutete Umwelt- und infektiöse Kofaktoren
Über Retroviren hinaus wurden andere infektiöse Erreger als potenzielle Auslöser vermutet, ohne dass ein formaler Beweis erbracht wurde. Einige Autoren haben die Rolle chronischer antigener Stimulationen durch bakterielle oder Pilzerreger im Kontakt mit den Ballen erwähnt, aber keine systematische mikrobiologische Kultur hat einen spezifischen mit der Erkrankung assoziierten Erreger nachgewiesen (Miller 2013). Die Hypothese einer Kontakthypersensibilität oder einer Fremdkörperreaktion wurde vorgebracht, ohne experimentelle Untermauerung. Fälle von PPF nach Impfung oder Futterumstellung wurden anekdotisch berichtet, aber kein kausaler Zusammenhang wurde hergestellt (Scarampella 2004). Die Rolle epigenetischer Faktoren, die die Expression von Genen modulieren, die an der Regulation des B-Kompartiments beteiligt sind – wie post-translationale Histonmodifikationen oder DNA-Methylierung an den Promotoren von PRDM1 und IRF4 – bleibt ein unerforschtes Forschungsfeld in der Katzenmedizin.
Molekulare Immunpathologie
4.1. Plasmazelluläre Ontogenie und beteiligte Signalwege
Das Verständnis der PPF erfordert eine fundierte Kenntnis der Plasmazellbiologie. Die terminale Differenzierung des B-Lymphozyten zur reifen Immunglobulin-sekretierenden Plasmazelle wird durch ein hierarchisches Netzwerk von Transkriptionsfaktoren orchestriert. Der Faktor BLIMP-1, kodiert durch das Gen PRDM1, wirkt als transkriptioneller Repressor des B-Zell-Programms und hemmt die Expression von PAX5 und BCL6, zwei Faktoren, die für die Aufrechterhaltung der Identität des germinalen B-Lymphozyten unverzichtbar sind (Nutt 2015). Gleichzeitig bindet der Faktor IRF4 (MUM1) in Synergie mit BLIMP-1, um das Sekretionsprogramm zu aktivieren und die Expression von XBP1 zu induzieren, einem Schlüsselmediator der Antwort auf fehlgefaltete Proteine (unfolded protein response, UPR), die die für die massive Immunglobulinproduktion notwendige Expansion des endoplasmatischen Retikulums ermöglicht. Im Kontext der PPF erscheint diese Kaskade in den in der Dermis der Ballen ansässigen Plasmazellen konstitutiv aktiviert, wie die intensive Immunmarkierung von MUM1/IRF4 und CD138 (Syndecan-1) in Biopsien nahelegt (Mauldin 2016; Gross 2005).
Der IL-6/JAK1/STAT3-Signalweg spielt eine zentrale Rolle bei der plasmazellulären Expansion. Interleukin 6, das lokal von Makrophagen und dermalen Fibroblasten als Reaktion auf entzündliche Signale produziert wird, bindet an seinen Membranrezeptor (IL-6Rα/gp130) und aktiviert die Tyrosinkinase JAK1, die den Faktor STAT3 phosphoryliert. Phosphoryliertes STAT3 dimerisiert und transloziert in den Kern, wo es direkt die Transkription von PRDM1 und IRF4 induziert (Nutt 2015). Dieser autokrine und parakrine Kreislauf könnte in den Ballen durch eine an proinflammatorischen Zytokinen reiche Mikroumgebung aufrechterhalten werden, insbesondere TNF-α und IL-1β, die ihrerseits die IL-6-Produktion durch Stromazellen über die Aktivierung des kanonischen NF-κB-Wegs (p65/RelA) stimulieren. Das Zytokin BAFF (B-cell Activating Factor, auch BLyS genannt), Mitglied der TNF-Superfamilie, stellt einen entscheidenden Überlebensfaktor für langlebige Plasmazellen dar. BAFF bindet an die Rezeptoren BCMA und TACI, die auf der Oberfläche von Plasmazellen exprimiert werden, aktiviert den nicht-kanonischen NF-κB-Weg (RelB/p52) und hemmt die mitochondriale Apoptose durch Überexpression von BCL-2 und MCL-1 (Mackay 2009). Ein Überschuss an Serum-BAFF, der bei mehreren menschlichen Autoimmunerkrankungen dokumentiert ist, könnte einen analogen pathophysiologischen Mechanismus bei der PPF darstellen, obwohl die Messung dieses Zytokins noch nicht speziell bei betroffenen Katzen durchgeführt wurde.
4.2. Hypergammaglobulinämie und Immunkomplex-Ablagerungen
Die polyklonale Hypergammaglobulinämie, die bei 50 bis 63 % der Katzen mit PPF gefunden wird, spiegelt die diffuse und unspezifische Aktivierung des Plasmazell-Kompartiments wider (Guaguère 2004). Die Serumprotein-Elektrophorese zeigt eine Erhöhung der Gamma-Fraktion ohne begrenzten Peak, mit IgG-Werten, die das Zwei- bis Dreifache der oberen Normgrenze erreichen können. Die übermäßige Immunglobulinproduktion führt in Abwesenheit eines identifizierten Zielantigens zur Bildung zirkulierender Immunkomplexe, die sich in stark vaskularisierten Geweben ablagern, insbesondere in den Nierenglomeruli und der Dermis der Ballen. Diese Ablagerungen wurden durch direkte Immunfluoreszenz in Form von granulären Ablagerungen von IgG, IgM und der Komplementfraktion C3 entlang der epidermalen Basalmembran und um dermale Gefäßwände nachgewiesen (Gross 2005). Der Ablagerungsmechanismus erinnert an den der Typ-III-Überempfindlichkeitsreaktion (Klassifikation von Gell und Coombs), bei der Immunkomplexe mittlerer Größe der Clearance durch das retikuloendotheliale System entgehen und in Gefäßwänden präzipitieren und eine lokale Entzündungskaskade auslösen.
4.3. Komplementaktivierung und Entzündungskaskade
Immunkomplex-Ablagerungen aktivieren den klassischen Komplementweg durch Fixierung des C1q-Fragments an den Fc-Abschnitt aggregierter Immunglobuline. Diese sequenzielle Aktivierung (C1q → C1r/C1s → C4 → C2 → C3-Konvertase) führt zur Spaltung von C3 in C3a (Anaphylatoxin) und C3b (Opsonin) und dann zur Bildung des Membranangriffskomplexes C5b-9, der eine direkte Zelllyse verursacht (Gross 2005). Die Anaphylatoxine C3a und C5a wirken als starke Chemoattraktantien für Neutrophile und Makrophagen und verstärken die lokale Entzündung. Die Freisetzung lysosomaler Proteasen (Elastase, Cathepsin G) durch rekrutierte Neutrophile trägt zum Abbau der extrazellulären Matrix der Ballendermis bei und erklärt die weiche und schwammige Textur, die für das betroffene Gewebe charakteristisch ist (Miller 2013). Die Messung des Serum-C3, wenn durchgeführt, zeigt manchmal eine Verringerung, die mit einem Verbrauch durch In-vivo-Aktivierung vereinbar ist, ein klassisches Phänomen bei Immunkomplex-Erkrankungen.
4.4. Matrix-Metalloproteinasen und Gewebezerstörung
Das destruktive Remodeling des Ballengewebes involviert Matrix-Metalloproteinasen (MMP), eine Familie zinkabhängiger Endopeptidasen, die Komponenten der extrazellulären Matrix abbauen können. MMP-2 (Gelatinase A) und MMP-9 (Gelatinase B) sind besonders am Abbau von Kollagen Typ IV und Laminin an der Basalmembran beteiligt, während MMP-1 (interstitielle Kollagenase) das fibrilläre Kollagen der Typen I und III spaltet, das den Großteil des dermalen Gerüsts des Ballens ausmacht (Sapadin 2006). Die Expression dieser MMPs wird durch TNF-α und IL-1β über die Aktivierung des Transkriptionsfaktors AP-1 (c-Fos/c-Jun) und des NF-κB-Wegs induziert. Der progressive Kollagenabbau in Kombination mit entzündlichem Ödem und massiver Zellinfiltration führt zur charakteristischen Volumenzunahme des Ballens, dessen Konsistenz von fest zu teigig übergeht. Die zentrale Rolle der MMPs in der Pathogenese bietet eine direkte pharmakologische Grundlage für die Verwendung von Doxycyclin, dessen hemmende Aktivität auf MMPs einer der am besten dokumentierten Wirkmechanismen unabhängig von seiner antibakteriellen Aktivität ist (Griffin 2010).
Klinische Präsentation
5.1. Ballensemiologie
Das klinische Bild der PPF ist in der Regel charakteristisch und ermöglicht eine diagnostische Orientierung bereits bei der makroskopischen Untersuchung. Die elementare Läsion besteht aus einer diffusen und symmetrischen Schwellung eines oder mehrerer Ballen, die dem betroffenen Ballen ein geschwollenes, abgerundetes Aussehen verleiht, das deutlich größer als normal ist. Die zentralen Metacarpal- und Metatarsalballen sind in mehr als 80 % der Fälle bevorzugt betroffen, obwohl auch Digitalballen beteiligt sein können (Miller 2013). Die Beteiligung ist meist bilateral und betrifft gleichzeitig alle vier Gliedmaßen in etwa 50 % der berichteten Fälle (Guaguère 2004). Die Ballenoberfläche zeigt eine violett-bläuliche bis lila Färbung, manchmal als lokale Zyanose beschrieben, die eine vaskuläre Stauung und tiefe dermale Entzündung widerspiegelt. Diese Färbung wird hauptsächlich bei Ballen mit heller Pigmentierung beobachtet und kann bei natürlich dunklen Ballen maskiert sein. Ein sehr charakteristisches semiologisches Zeichen besteht im gestreiften Aussehen der Oberfläche mit feinen gekreuzten weißlichen Streifen, die ein Netzmuster bilden (cross-hatching), das aus der Spannung resultiert, die das ödematöse Gewebe auf die verdünnte Epidermis des Ballens ausübt (Gross 2005). Die Palpation zeigt eine weiche und teigige Konsistenz, deutlich verschieden von der normalen Festigkeit des gesunden Ballens, was die Zerstörung der dermalen Kollagenarchitektur und die massive Zellinfiltration widerspiegelt. Schmerzen sind in frühen Stadien im Allgemeinen nicht vorhanden, und Lahmheit, wenn vorhanden, spiegelt meist eine sekundäre Ulzeration wider.
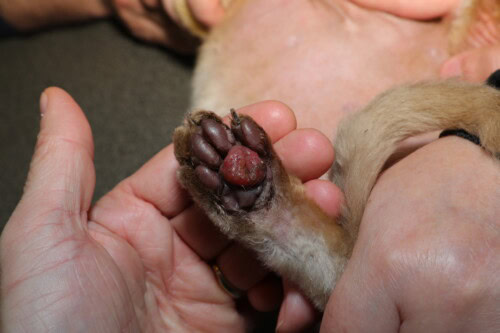
Fortgeschrittene Form mit Öffnung des zentralen Ballens
5.2. Natürlicher Verlauf und Komplikationen
Der Verlauf der PPF ist variabel und unvorhersehbar. Ein signifikanter Anteil der Fälle, geschätzt auf 10 bis 30 %, kann eine spontane Auflösung ohne therapeutische Intervention zeigen, innerhalb einiger Wochen bis mehrerer Monate (Miller 2013). Diese spontane Regression verstärkt die Hypothese eines reaktionären Prozesses auf einen transienten antigenen Stimulus. Die Entwicklung zur Ulzeration stellt jedoch die gefürchtetste Komplikation dar und tritt bei 30 bis 50 % der unbehandelten Fälle auf (Guaguère 2004). Die Ulzeration manifestiert sich durch einen Substanzverlust der Ballenepidermis, der die infiltrierte und fragile Dermis freilegt, oft begleitet von einer sekundären Blutung, die manchmal profus ist aufgrund der entzündlichen Neovaskularisation und der Fragilität der durch Immunkomplex-Ablagerungen und MMP-Wirkung geschwächten Gefäßwände (Taylor 1990). Eine bakterielle Superinfektion des Ulkus stellt ein zusätzliches Risiko dar, obwohl sie nicht systematisch ist. Die mit der Ulzeration einhergehenden Schmerzen verursachen dann eine ausgeprägte Lahmheit, eine Zurückhaltung bei der Bewegung und manchmal zwanghaftes Lecken, das das erosive Phänomen aufrechterhält. Einige außergewöhnliche Fälle von rezidivierenden Blutungen, die zu einer Eisenmangelanämie geführt haben, wurden dokumentiert und unterstreichen die Notwendigkeit einer hämatologischen Überwachung bei Katzen mit chronischen Ulzerationen (Taylor 1990).
5.3. Assoziierte extrapodale Manifestationen
Die PPF beschränkt sich nicht immer auf eine isolierte Ballenbeteiligung. Assoziationen mit anderen plasmazellulären Manifestationen wurden dokumentiert, was auf einen zugrunde liegenden systemischen Prozess hindeutet. Plasmazelluläre Stomatitis, gekennzeichnet durch eine plasmazelluläre Infiltration der Mundschleimhaut (insbesondere des Gaumens und der glossopalatalen Arkaden), wurde in 10 bis 20 % der Fälle je nach Serie gleichzeitig mit PPF beschrieben (Miller 2013; Guaguère 2004). Das gleichzeitige Auftreten dieser beiden Entitäten bei demselben Tier stellt ein starkes Argument für eine systemische B-Kompartiment-Störung dar. Nierenbeteiligungen in Form von Immunkomplex-Glomerulonephritis oder, seltener, reaktiver renaler AA-Amyloidose wurden bei Katzen mit chronischer PPF berichtet (Dias Pereira 2003). Die Ablagerung von Amyloidsubstanz, bestehend aus Fibrillen, die aus dem Serum-Amyloid-A-Protein (SAA) stammen, das in Überschuss von der Leber unter der Stimulation von IL-6 und TNF-α bei chronischer Entzündung produziert wird, kann zu progressiver Niereninsuffizienz führen. Diese Komorbiditäten verleihen der PPF eine systemische Dimension, die über den strikt dermatologischen Rahmen hinausgeht und eine vollständige biologische Untersuchung bei jeder diagnostizierten Katze rechtfertigt.
Diagnostisches Vorgehen
6.1. Klinische Untersuchung und Orientierungskriterien
Die Diagnose der PPF beruht auf einer Reihe klinischer, zytologischer und histopathologischer Argumente. Die sorgfältige klinische Untersuchung aller vier Gliedmaßen, einschließlich Inspektion und Palpation aller Ballen, stellt den ersten Schritt dar. Die Kombination einer schmerzlosen Schwellung eines oder mehrerer zentraler Ballen, einer violetten Färbung und einer teigigen Konsistenz bei einer erwachsenen Katze orientiert stark zur Diagnose. Die vollständige dermatologische Untersuchung sollte nach möglichen assoziierten Hautläsionen an anderen Stellen sowie eine Untersuchung der Mundhöhle zur Suche nach einer gleichzeitigen plasmazellulären Stomatitis suchen. Die Beurteilung des Allgemeinzustands, der Nierenpalpation und des Lymphknotenstatus gehört zur anfänglichen klinischen Untersuchung (Miller 2013).
6.2. Beitrag der Zytologie
Die Feinnadelaspiration des geschwollenen Ballens, durchgeführt mit einer 22- bis 25-Gauge-Nadel, stellt eine schnelle und minimal invasive ergänzende Untersuchung dar, die in der Konsultation durchgeführt werden kann. Der Ausstrich auf einem Objektträger und die Färbung mit May-Grünwald-Giemsa (MGG) oder Diff-Quick zeigen ein zelluläres Infiltrat, das zu mehr als 80 % aus reifen Plasmazellen besteht, erkennbar an ihrem exzentrischen Kern, ihrem Chromatin in „Speichenradform” und ihrem reichlichen basophilen Zytoplasma mit einem klaren perinukleären Hof, der dem hypertrophierten Golgi-Apparat entspricht (Gross 2005). Das Vorhandensein von Mott-Zellen, Plasmazellen, deren Zytoplasma durch mehrere sphärische eosinophile Einschlüsse, die Russell-Körpern entsprechen (im dilatierten endoplasmatischen Retikulum aggregierte Immunglobuline), gedehnt ist, ist ein hochgradig charakteristisches Zeichen der PPF. Diese Einschlüsse resultieren aus einer Dysfunktion des UPR-Wegs (XBP1-abhängig), der die Überladung mit sekretorischen Proteinen nicht mehr bewältigen kann (Nutt 2015). Die Zytologie orientiert zwar stark zur Diagnose, erlaubt aber allein nicht den Ausschluss eines extramedulären Plasmozytoms, und die histopathologische Bestätigung bleibt in atypischen oder unilateralen Fällen empfohlen.
6.3. Histopathologie: der diagnostische Goldstandard
Die Hautbiopsie, entnommen mit dem Skalpell als Keilbiopsie (wedge biopsy) oder mit Biopsiestanze (6-mm-Punch), liefert die definitive Diagnose. Die histopathologische Untersuchung zeigt ein diffuses oder noduläres dermales Infiltrat, das fast ausschließlich aus reifen Plasmazellen besteht und die oberflächliche und tiefe Dermis einnimmt, oft bis ins subkutane Gewebe ausgedehnt (Gross 2005; Mauldin 2016). Die Plasmazellen sind gut differenziert, ohne signifikante zytonukleäre Atypie, und der Mitoseindex ist niedrig, im Allgemeinen unter 1 Mitose pro Hochleistungsfeld (×400), was die PPF formal von einem Plasmozytom unterscheidet. Die lobuläre Architektur des Fettgewebes des Ballens ist respektiert, aber vom Infiltrat eingenommen. Die epidermale Basalmembran erscheint oft verdünnt, und die darüber liegende Epidermis ist atrophisch, was zur Ulzeration prädisponiert. Eine leukozytoklastische Vaskulitis mit fibrinoider Nekrose der Arteriolen-Wand und Wandinfiltration durch Neutrophile mit fragmentierten Kernen begleitet häufig das plasmazelluläre Infiltrat und bezeugt die Beteiligung der Immunkomplexe an der Pathogenese (Gross 2005). Die Immunhistochemie bestätigt die Expression von CD79a (pan-B-Marker), CD138 und MUM1/IRF4 durch die Plasmazellen mit polyklonaler Expression der Kappa- und Lambda-Leichtketten, was eine monoklonale Proliferation ausschließt (Mauldin 2016). Russell-Körper werden durch PAS-Färbung (Periodic Acid-Schiff) nachgewiesen und erscheinen als PAS-positive und Diastase-resistente intrazytoplasmatische Einschlüsse.
6.4. Biologische und serologische Untersuchung
Die biologische Untersuchung ergänzt das diagnostische Bild und liefert prognostische Informationen. Das Hämogramm kann bei einigen Katzen eine moderate Lymphozytose sowie eine regenerative Anämie bei chronischen Blutungen aus ulzerierten Ballen zeigen. Die Serumprotein-Elektrophorese stellt eine Schlüsseluntersuchung dar und zeigt die polyklonale Hypergammaglobulinämie in 50 bis 63 % der Fälle mit Gesamtproteinwerten manchmal über 90 g/L (Guaguère 2004). Die Messung spezifischer Immunglobuline, wenn verfügbar, zeigt eine vorherrschende Erhöhung von IgG, aber auch IgA und IgM können erhöht sein. Die FIV- und FeLV-Serologie wird systematisch empfohlen, durchgeführt durch schnelle Immunchromatographie (Nachweis von Anti-FIV-Antikörpern und FeLV-p27-Antigen) oder durch ELISA, mit Bestätigung durch PCR bei klinischer Diskordanz (Hartmann 2012). Die Nierenbiochemie (Kreatinin, SDMA, Urinprotein/Kreatinin-Verhältnis) sollte bewertet werden, um eine mögliche Immunkomplex-Glomerulonephritis oder assoziierte renale Amyloidose zu erkennen. Die Suche nach ANA durch indirekte Immunfluoreszenz auf HEp-2-Zellen vervollständigt die immunologische Untersuchung, obwohl ihr positiver prädiktiver Wert bei der Katze bescheiden bleibt (Dias Pereira 2003).
6.5. Differenzialdiagnose
Die Differenzialdiagnose der PPF umfasst mehrere Entitäten, die die Katzenballen betreffen. Das extramedullare Plasmozytom, selten in podaler Lokalisation, unterscheidet sich durch seinen im Allgemeinen solitären, unilateralen Charakter und durch einen höheren Mitoseindex (> 5 Mitosen/10 Felder ×400) verbunden mit Monoklonalität in der Immunhistochemie (Mauldin 2016). Das eosinophile Granulom, das die Ballen betreffen kann, ist durch ein vorherrschend eosinophiles Infiltrat mit Bildern von flammenförmiger Kollagena gekennzeichnet. Die bakterielle Pododermatitis zeigt Infektionszeichen (eitriges Exsudat, warme Schwellung, ausgeprägte Schmerzen). Der Pemphigus foliaceus, eine häufige Ursache für krustige Pododermatitis bei der Katze, unterscheidet sich durch das Vorhandensein von Pusteln, Krusten und Akantholyse in Zytologie und Histologie. Plattenepithelkarzinome der Ballen, vor allem bei weißen Katzen beobachtet, präsentieren sich typischerweise als asymmetrische ulzero-proliferative Läsionen. Die diffuse kutane Mastozytose kann, obwohl sehr selten, eine Ballenschwellung nachahmen (Miller 2013; Hnilica 2017).
Therapeutisches Management
7.1. Therapeutische Abstinenz und spontane Auflösung
Die Möglichkeit einer spontanen Auflösung, dokumentiert in 10 bis 30 % der Fälle, stellt ein grundlegendes Entscheidungselement dar (Miller 2013). Bei Katzen mit begrenzter, nicht ulzerierter und schmerzloser Beteiligung kann eine Beobachtungsperiode von vier bis sechs Wochen vor jeder pharmakologischen Intervention in Betracht gezogen werden, mit engmaschiger klinischer Nachverfolgung. Dieser Ansatz des „watchful waiting” ist umso mehr gerechtfertigt, als die verfügbaren Behandlungen nicht frei von Nebenwirkungen sind und die Erkrankung in Abwesenheit von Komplikationen nicht lebensbedrohlich ist. Die Entscheidung zur Behandlung beruht auf dem Vorhandensein einer Ulzeration, von Schmerzen, Lahmheit, rezidivierenden Blutungen oder einer Progression der Läsionen trotz Überwachung (Bettenay 2003).
7.2. Doxycyclin: pharmakologische Begründung und Wirksamkeitsdaten
Das Doxycyclin stellt seit den Pionierarbeiten von Bettenay und Mitarbeitern die am umfassendsten dokumentierte Erstlinienbehandlung im Management der plasmazellulären Pododermatitis der Katze dar. Seine Verwendung beruht nicht auf einer antibakteriellen Wirkung – die Erkrankung hat keine nachgewiesene bakterielle infektiöse Ätiologie – sondern auf seinen pleiotropen immunmodulierenden Eigenschaften, die mit der gesamten Tetracyclin-Familie geteilt werden (Bettenay 2003). Auf molekularer Ebene hemmt Doxycyclin die Aktivität mehrerer Matrix-Metalloproteinasen (MMP), insbesondere MMP-2 und MMP-9, durch Chelatierung der für ihre katalytische Stelle notwendigen Zinkionen. Diese Hemmung begrenzt den Abbau von Kollagen Typ IV und der Basalmembran, Prozesse, die direkt am destruktiven Gewebe-Remodeling in betroffenen Ballen beteiligt sind (Guaguère 2004). Darüber hinaus übt Doxycyclin eine entzündungshemmende Wirkung aus, indem es die Produktion von Prostaglandin E2 (PGE2) über die Unterdrückung der Expression von Cyclooxygenase 2 (COX-2) in aktivierten Makrophagen reduziert und die Synthese von Stickoxid (NO) durch Hemmung der induzierbaren NO-Synthase (iNOS) verringert (Sapadin 2006).
Ein zusätzlicher, in der veterinärmedizinischen Literatur oft unterschätzter Mechanismus betrifft die Fähigkeit von Doxycyclin, die T-Lymphozyten-Aktivierung zu modulieren. In-vitro-Studien zeigen, dass Tetracycline die Proliferation von durch Mitogene stimulierten T-Lymphozyten reduzieren und die Expression des Haupthistokompatibilitätskomplexes Klasse II (MHC-II) auf der Oberfläche Antigen-präsentierender Zellen verringern und damit die Verstärkungsschleife der adaptiven Immunität abschwächen (Niimi 1998). Im Kontext der plasmazellulären Pododermatitis, bei der die polyklonale Hypergammaglobulinämie eine dysregulierte B-Aktivierung widerspiegelt, hat diese Wirkung auf die Antigenpräsentation direkte pathophysiologische Relevanz.
Das therapeutische Standardprotokoll basiert auf der oralen Verabreichung von Doxycyclin in einer Dosierung von 10 mg/kg einmal täglich für eine Mindestdauer von sechs bis acht Wochen (Bettenay 2003). Die Compliance kann durch das Risiko einer Ösophagusstriktur beeinträchtigt werden, eine für die Katze spezifische Komplikation, die durch die Retention der Tablette in der Speiseröhre und die lokale Freisetzung eines sauren pH-Werts induziert wird, der eine fokale Schleimhautnekrose verursacht. Die Prävalenz dieser Komplikation wurde auf etwa 3 bis 5 % der Katzen geschätzt, die feste Doxycyclin-Formen ohne Flüssigkeitsnachverfolgung erhalten (German 2005). Die systematische Verabreichung eines Wasserbolus von 3 bis 6 mL nach jeder Einnahme oder die Verwendung einer flüssigen Formulierung reduziert dieses Risiko erheblich. Die retrospektiven Daten, die von Guaguère und Bensignor zusammengestellt wurden, berichten von einer vollständigen oder teilweisen klinischen Ansprechrate von 50 bis 65 % nach einem ersten Doxycyclin-Zyklus, mit einer bei Respondern bereits ab der dritten Behandlungswoche beobachtbaren Verbesserung (Guaguère 2004). Die Auflösung manifestiert sich durch eine progressive Verringerung der Ballenschwellung, eine Repigmentierung der Ballen und eine Regression der charakteristischen weißlichen Streifen.
Rückfälle nach Behandlungsabbruch stellen eine häufige klinische Realität dar, dokumentiert bei etwa 30 bis 50 % der initial respondierenden Fälle innerhalb von drei bis sechs Monaten (Scarampella 2018). Diese Beobachtung legt nahe, dass Doxycyclin den zugrunde liegenden pathogenen Mechanismus nicht korrigiert, sondern dessen Effektormanifestationen abschwächt. Die Frage einer Erhaltungsbehandlung mit reduzierter Dosis (5 mg/kg/Tag oder jeden zweiten Tag) bleibt mangels kontrollierter Studie umstritten, obwohl einige Kliniker sie empirisch bei chronischen rezidivierenden Formen mit als zufriedenstellend beurteilten Ergebnissen anwenden.
7.3. Systemische Glukokortikoide
Die systemischen Glukokortikoide stellen die am zweithäufigsten verwendete therapeutische Linie dar, insbesondere wenn Doxycyclin sich als unzureichend erweist oder wenn die klinische Schwere eine schnelle Immunsuppression erfordert. Ihr Wirkmechanismus beruht auf der Bindung an den zytoplasmatischen Glukokortikoid-Rezeptor (GR), der nach nukleärer Translokation als Transkriptionsfaktor wirkt, der die Expression von mehr als 200 an der Immun- und Entzündungsantwort beteiligten Genen moduliert (Cain 2017). Die hauptsächliche entzündungshemmende Wirkung erfolgt durch Hemmung des Transkriptionsfaktors NF-κB (nuclear factor kappa-light-chain-enhancer of activated B cells) und blockiert damit die Transkription von Interleukin-1β (IL-1β), IL-6, TNF-α und mehreren Chemokinen, die für die plasmazelluläre Rekrutierung in der Ballendermis verantwortlich sind.
Prednisolon, oral verabreicht in einer Dosis von 1 bis 2 mg/kg/Tag für zwei bis vier Wochen, dann mit progressiver Reduktion über vier bis sechs Wochen, erzeugt eine klinische Ansprechrate von 60 bis 70 % je nach veröffentlichten retrospektiven Serien (Taylor 2004). Methylprednisolon-Acetat als subkutane Injektion (4 mg/kg) wurde in refraktären Fällen verwendet, mit berichteter Wirksamkeit, aber einem weniger günstigen Verträglichkeitsprofil langfristig aufgrund der verlängerten Wirkdauer und der Unmöglichkeit der Dosisanpassung (Guaguère 2004). Dosisabhängige Nebenwirkungen – Polyurie-Polydipsie, Polyphagie, erhöhte Anfälligkeit für Diabetes mellitus, Harnwegsinfektionen – begrenzen die Langzeitanwendung bei der Katze, einer Art, die notorisch empfindlich auf Kortikoid-induzierte Insulinresistenz reagiert. Die Entwicklung eines iatrogenen Diabetes mellitus wurde auf 5 bis 10 % bei Katzen geschätzt, die länger als drei Monate Glukokortikoide erhalten, wobei diese Prävalenz je nach kumulativer Dosis und individuellen Risikofaktoren wie Adipositas und fortgeschrittenem Alter variiert (Lowe 2008).
Das Ausschleichen der Glukokortikoide stellt einen heiklen therapeutischen Zeitpunkt dar. Eine zu schnelle Reduktion setzt dem Rückfall aus, während eine verlängerte Aufrechterhaltung die iatrogenen Risiken erhöht. Die anfängliche Kombination Doxycyclin-Prednisolon mit Übergang zu Doxycyclin allein nach Erreichen der klinischen Remission bietet einen pragmatischen Kompromiss, der oft in der Spezialpraxis angenommen wird (Scarampella 2018).
7.4. Ciclosporin und Calcineurin-Inhibitoren
Das Ciclosporin (Ciclosporin A, CsA) hat sich als therapeutische Alternative der Wahl bei refraktären Formen der plasmazellulären Pododermatitis der Katze herausgebildet. Sein Wirkmechanismus, unterschiedlich von dem der Glukokortikoide, beruht auf der Bildung eines Komplexes mit intrazellulärem Cyclophilin; dieser Komplex hemmt Calcineurin, eine Calcium-abhängige Phosphatase, die für die Dephosphorylierung des Transkriptionsfaktors NFAT (Nuclear Factor of Activated T-cells) unverzichtbar ist. Die Blockade von NFAT verhindert die Transkription von IL-2, einem Hauptzytokin der klonalen Proliferation von T-Helferzellen, und reduziert konsekutiv die T-Hilfe für B-Lymphozyten zur isotypischen Umschaltung und plasmazellulären Differenzierung (Robson 2003). Bei einer Erkrankung, die durch eine dichte plasmazelluläre Infiltration und eine Hypergammaglobulinämie gekennzeichnet ist, hat diese Ausrichtung des T-B-Dialogs direkte pathophysiologische Relevanz.
Die empfohlene Dosierung bei der Katze beträgt 5 bis 7 mg/kg/Tag oral, nüchtern verabreicht, um die Bioverfügbarkeit zu optimieren, die je nach Individuum zwischen 25 und 35 % variiert (Latimer 2014). Mehrere Fallserien berichten von Ansprechraten von 60 bis 85 % mit Ciclosporin, auch bei Tieren, die nicht auf Doxycyclin oder Glukokortikoide angesprochen haben (Bettenay 2003; Scarampella 2018). Die Wirklatenz beträgt im Allgemeinen vier bis sechs Wochen, eine Verzögerung, die mit dem Wirkmodus auf die adaptive Immunantwort konsistent ist. Gastrointestinale Nebenwirkungen – Erbrechen, Durchfall – betreffen etwa 15 bis 25 % der Katzen zu Behandlungsbeginn, lösen sich aber häufig durch eine progressive Dosiseinführung über eine Woche oder durch gleichzeitige Verabreichung mit einer kleinen Menge Futter auf (Roberts 2016).
Das opportunistische Infektionsrisiko verdient aufmerksame Überwachung. Die Reaktivierung der Toxoplasmose, obwohl unter Ciclosporin bei der Katze selten dokumentiert, wurde bei verlängerter Immunsuppression berichtet und stellt eine relative Kontraindikation bei seronegativen Individuen dar, die einer Risikoumgebung ausgesetzt sind (Last 2004). Eine prä-therapeutische serologische Untersuchung auf Toxoplasma gondii wird von mehreren Experten empfohlen, obwohl das Evidenzniveau für diese spezifische Indikation begrenzt bleibt. Topisches Tacrolimus (FK-506), ein weiterer Calcineurin-Inhibitor, war nicht Gegenstand gezielter Studien zur plasmazellulären Pododermatitis, wahrscheinlich aufgrund der Schwierigkeit der Anwendung auf der unregelmäßigen Ballenoberfläche und der geringen perkutanen Penetration durch die verdickte Ballenepidermis.
7.5. Andere Immunmodulatoren
Mehrere immunmodulierende Wirkstoffe wurden punktuell eingesetzt, ohne dass einer ein Evidenzniveau erreicht, das dem von Doxycyclin oder Ciclosporin entspricht. Das Chlorambucil, ein alkylierender Wirkstoff aus der Familie der Stickstofflost-Verbindungen, wurde bei schweren und refraktären Formen in einer Dosierung von 0,1 bis 0,2 mg/kg jeden zweiten Tag in Kombination mit Prednisolon verwendet (Taylor 2004). Sein Mechanismus beruht auf der Alkylierung der DNA proliferierender Lymphozyten, was zu Interstrang-Bindungen führt, die Replikation und Transkription verhindern, mit einer bevorzugten Wirkung auf B-lymphozytäre Linien, was seine Verwendung bei einer plasmazellulär vermittelten Erkrankung theoretisch rechtfertigt. Das hämatologische Toxizitätsprofil erfordert eine Überwachung durch Blutbild alle zwei bis drei Wochen während der ersten zwei Behandlungsmonate. Eine signifikante Myelosuppression, definiert als Neutropenie unter 2.500/μL, tritt bei etwa 10 bis 15 % der behandelten Katzen auf und erfordert eine vorübergehende Aussetzung (Lowe 2008).
Mycophenolatmofetil, ein selektiver und reversibler Inhibitor der Inosinmonophosphat-Dehydrogenase (IMPDH), einem Schlüsselenzym der De-novo-Purinsynthese in Lymphozyten, wurde anekdotisch in einigen Fällen von plasmazellulärer Pododermatitis mit variablen Ergebnissen berichtet, in einer Dosierung von 10 mg/kg zweimal täglich oral (Backel 2013). Das Fehlen kontrollierter Studien und die Seltenheit pharmakokinetischer Daten bei der Katze begrenzen seine Empfehlung.
Die rekombinanten Interferone stellen einen unterschiedlichen immunmodulierenden Ansatz dar. Rekombinantes felines Omega-Interferon (rFeIFN-ω), dessen Wirkung über die Aktivierung des JAK-STAT-Wegs (insbesondere STAT1 und STAT2) über den Typ-I-Interferon-Rezeptor erfolgt, induziert die Expression von durch Interferon stimulierten Genen (ISGs) und moduliert die Th1/Th2-Balance, was theoretisch die der plasmazellulären Infiltration zugrunde liegende Immunverschiebung korrigieren könnte (de Mari 2004). Einige klinische Fälle haben eine Verbesserung nach subkutaner oder perlingualer Injektion von Omega-Interferon berichtet, aber die Daten bleiben zu sporadisch, um solide Schlussfolgerungen zu ziehen.
7.6. Chirurgische Behandlung
Die chirurgische Exzision betroffener Ballen stellt eine Option dar, die fokalen schwer ulzerierten Formen mit sekundären septischen Komplikationen oder Fällen vorbehalten ist, die vollständig refraktär gegenüber allen medizinischen Optionen sind. Die Podoplastik wurde in isolierten Fallberichten beschrieben, mit Resektion des schwer veränderten Gewebes, gefolgt von einem Verschluss durch Verschiebelappen oder Heilung durch sekundäre Intention unter halbverschlossenem Verband (Guaguère 2004). Die funktionellen Ergebnisse hängen vom Ausmaß der Resektion und der Anzahl der beteiligten Ballen ab. Die multipodulare Beteiligung, die 40 bis 50 % der Fälle betrifft, macht diesen Ansatz technisch schwierig und ethisch fragwürdig, wenn er eine bilaterale Resektion tragender Ballen beinhalten würde.
Die Zehenamputation wurde in seltenen Situationen berichtet, in denen ein einzelner Digitalballen eine irreduktibel geschwollene mit tiefer Ulzeration und sekundärer Osteomyelitis aufwies, aber diese Eventualität bleibt in der plasmazellulären Pododermatitis, die selten den darunter liegenden Knochen erreicht, außergewöhnlich (Taylor 2004). Der Einsatz des CO₂-Lasers zur kontrollierten Verdampfung überschüssigen Gewebes wurde empirisch erwähnt, aber keine Studie bewertet formal die Wirksamkeit oder das Heilungsprofil bei dieser präzisen Indikation. Das postoperative Management beinhaltet systematisch eine begleitende immunmodulierende Behandlung zur Verhinderung eines lokalen Rückfalls und bestätigt, dass die Chirurgie nur die Gewebefolge behandelt, ohne die kausale Immundysregulation zu korrigieren.
Prognose und Langzeitverlauf
8.1. Ansprechraten und Remissionsdauer
Die prognostische Bewertung der plasmazellulären Pododermatitis der Katze beruht auf im Wesentlichen retrospektiven Daten, wobei das Fehlen randomisierter kontrollierter Studien eine wesentliche Einschränkung bei der vergleichenden Bewertung therapeutischer Ansprechraten darstellt. Die veröffentlichten Serien, die gemeinsam zwischen 100 und 150 dokumentierte Fälle in den letzten drei Jahrzehnten zusammenführen, konvergieren zu einem insgesamt günstigen prognostischen Profil für nicht ulzerierte Formen, die frühzeitig behandelt werden (Guaguère 2004; Scarampella 2018). Die vollständige Remissionsrate, definiert als vollständige klinische Auflösung der Ballenläsionen und Normalisierung der Ballentextur, variiert je nach Publikation und eingesetzter Behandlung zwischen 30 und 50 %. Die partielle Remission, gekennzeichnet durch eine klinische Verbesserung von über 50 %, aber mit Persistenz einer residuellen Verdickung oder Depigmentierung, betrifft weitere 20 bis 30 % der behandelten Fälle.
Die Naturgeschichte der Erkrankung ist bemerkenswert durch die Möglichkeit spontaner Remissionen, berichtet in 10 bis 20 % der Fälle gemäß der vollständigsten bisher veröffentlichten retrospektiven Serie (Bettenay 2003). Dieses Phänomen, außergewöhnlich bei immun-vermittelten Katzenerkrankungen, wirft die Frage einer endogenen immunologischen Regulation auf, die in der Lage ist, die Toleranz wiederherzustellen oder den pathogenen Plasmazellklon zu unterdrücken. Die Hypothese einer Modulation durch regulatorische T-Lymphozyten (Treg) über die Produktion von IL-10 und TGF-β, die eine negative Rückkopplung auf die B-Differenzierung und das plasmazelluläre Überleben ausüben, könnte dieses Phänomen der Selbstauflösung erklären (Groux 1997). Der direkte Nachweis dieser Hypothese bei der plasmazellulären Pododermatitis bleibt jedoch durch Studien zur dynamischen Immunphänotypisierung zu erbringen.
Die Remissionsdauer nach medizinischer Behandlung variiert erheblich. Bei Respondern auf Doxycyclin wurde die mediane Remissionsdauer auf drei bis zwölf Monate geschätzt, mit einer bimodalen Verteilung: eine Gruppe dauerhafter Responder (Remission über ein Jahr) und eine Gruppe früher Rückfälliger (Remission unter drei Monaten) (Scarampella 2018). Diese Heterogenität legt die Existenz pathogenetisch unterschiedlicher Subpopulationen nahe, die potenziell durch immunologische oder histopathologische Biomarker identifizierbar sind, die noch zu definieren sind. Unter Ciclosporin erscheinen verlängerte Remissionen häufiger, mit berichteten medianen Dauern von sechs bis achtzehn Monaten, obwohl die therapeutische Abhängigkeit – Notwendigkeit der Aufrechterhaltung einer Erhaltungsbehandlung mit niedriger Dosis – einen signifikanten Anteil der Fälle betrifft (Bettenay 2003).
8.2. Identifizierte Prognosefaktoren
Die Identifizierung zuverlässiger Prognosefaktoren bleibt eine Herausforderung in Abwesenheit prospektiver Kohorten ausreichender Größe. Mehrere klinische und biologische Parameter wurden retrospektiv und mit variablen Signifikanzniveaus mit der Wahrscheinlichkeit des therapeutischen Ansprechens assoziiert. Der Ulzerationsgrad zum Zeitpunkt der Diagnose stellt den am regelmäßigsten identifizierten negativen Prognosefaktor dar: Ballen mit tiefer Ulzeration mit Freilegung der darunter liegenden Dermis sprechen weniger günstig auf Doxycyclin allein an und erfordern häufiger den Einsatz einer Zweitlinien-Immunsuppression (Taylor 2004). Die pathophysiologische Erklärung liegt im irreversiblen fibrotischen Remodeling und der sekundären bakteriellen Kolonisation, die den lokalen Entzündungskreis unabhängig vom primären immunologischen Mechanismus aufrechterhalten.
Der Serum-Gammaglobulin-Spiegel bei Diagnose scheint invers mit der Prognose korreliert zu sein: Katzen mit ausgeprägter Hypergammaglobulinämie (über 20 g/L) zeigen niedrigere vollständige Remissionsraten als diejenigen, deren Gammaglobuline moderat erhöht bleiben (Gruffydd-Jones 1980; Guaguère 2004). Diese Beobachtung verstärkt die Idee eines Schweregradkontinuums, das durch die Amplitude der systemischen Immunaktivierung widergespiegelt wird. Die Anzahl der zum Zeitpunkt der Erstvorstellung betroffenen Ballen wurde ebenfalls mit der Prognose korreliert: Die Beteiligung von vier oder mehr Ballen ist mit einer signifikant höheren Rückfallwahrscheinlichkeit assoziiert als bei mono- oder bipodularen Formen (Scarampella 2018). Die FIV-Serologie scheint, wenn positiv, das therapeutische Ansprechen in den verfügbaren Serien nicht entscheidend zu beeinflussen, obwohl die Anzahl der koinfizierten Fälle zu gering bleibt, um statistisch robuste Schlussfolgerungen zu ziehen (Bettenay 2003).
Das Alter bei Diagnose wurde nicht reproduzierbar als unabhängiger Prognosefaktor identifiziert, obwohl einige Autoren eine Tendenz zu schwereren und rezidivierenderen Formen bei Individuen unter drei Jahren berichten, möglicherweise im Zusammenhang mit einer Unreife der immunologischen Toleranzmechanismen (Taylor 2004). Die Entwicklung standardisierter klinischer Scores, die das Läsionsausmaß, den Ulzerationsgrad, biologische Parameter und den infiltrierenden Immunphänotyp integrieren, stellt ein unerfülltes Bedürfnis dar, das die Homogenisierung der prognostischen Bewertung und den Vergleich zwischen Studien ermöglichen würde.
Komorbiditäten und Konzept des plasmazellulären Syndroms der Katze
9.1. Plasmazelluläre Stomatitis
Der Zusammenhang zwischen plasmazellulärer Pododermatitis der Katze und plasmazellulärer Stomatitis (auch als chronische Gingivostomatitis der Katze mit plasmazellulärer Prädominanz bezeichnet) ist seit den Erstbeschreibungen der Erkrankung anerkannt und stellt das solideste klinische Argument für ein systemisches plasmazelluläres Syndrom bei der Katze dar (Gruffydd-Jones 1980). Die Prävalenz des gemeinsamen Auftretens variiert je nach Serie zwischen 10 und 35 %, wobei die höheren Werte in Studien berichtet werden, die systematisch die Mundhöhle bei Katzen mit Pododermatitis untersucht haben (Guaguère 2004; Scarampella 2018). Die plasmazelluläre Stomatitis ist histologisch durch ein dichtes plasmazelluläres Infiltrat der gingivalen und bukkalen Lamina propria gekennzeichnet, mit Mott-Zellen und Russell-Körpern, die identisch zu denen sind, die in den Ballen beobachtet werden. Die immunhistochemische Analyse zeigt eine Prädominanz polyklonaler IgG, ähnlich dem Serumprofil, und eine lokale Überexpression von IL-1β, IL-6 und TNF-α in betroffenen Schleimhäuten (Harley 2003).
Auf molekularer Ebene wurde chronische feline Stomatitis mit einer Aktivierung des NF-κB-Wegs und einer Überexpression von RANKL (Receptor Activator of Nuclear Factor Kappa-B Ligand) in Gingivalgeweben in Verbindung gebracht, was zur alveolären Knochenresorption beiträgt, die in fortgeschrittenen Formen beobachtet wird (Arzi 2010). Dieser letzte Weg unterscheidet die Stomatitis von der Pododermatitis, bei der die osteoklastische Komponente fehlt oder minimal ist. Die Stomatitis-Pododermatitis-Komorbidität scheint nicht ausschließlich mit dem FIV- oder FeLV-Status verbunden zu sein, da sie bei Katzen dokumentiert ist, die für beide Retroviren seronegativ sind (Bettenay 2003). Diese Feststellung verstärkt die Hypothese eines gemeinsamen immunologischen Hintergrunds, der für aberrante plasmazelluläre Aktivierung an verschiedenen anatomischen Stellen prädisponiert, die Merkmale chronischer antigener Exposition teilen (Mundschleimhäute und Ballenepithel, beide chronischen mechanischen und mikrobiellen Stimulationen ausgesetzt).
9.2. Glomerulonephritis und renale Amyloidose
Die Nierenbeteiligung stellt eine potenziell schwerwiegende Komplikation der plasmazellulären Pododermatitis der Katze dar, berichtet in einer begrenzten, aber signifikanten Anzahl von Fällen. Die Immunkomplex-Glomerulonephritis wurde histologisch bei Katzen mit plasmazellulärer Pododermatitis in Verbindung mit Proteinurie und progressiver Azotämie dokumentiert (Gruffydd-Jones 1980). Der pathogene Mechanismus beinhaltet die Ablagerung zirkulierender Immunkomplexe – gebildet durch überschüssige polyklonale Immunglobuline und ihre entsprechenden Antigene – im glomerulären Mesangium und entlang der glomerulären Basalmembran, mit lokaler Komplementaktivierung durch den klassischen Weg (C1q → C4 → C2 → C3) und Rekrutierung von Neutrophilen und Makrophagen, die zu endothelialen und Podozytenläsionen beitragen (Center 1990).
Die renale Amyloidose vom Typ AA wurde in seltenen Fällen chronischer plasmazellulärer Pododermatitis berichtet, wobei das Serum-Amyloid-A-Protein (SAA) ein Akute-Phase-Protein ist, das von Hepatozyten unter dem Einfluss von IL-6 und IL-1β synthetisiert wird – Zytokine, deren Produktion in der systemischen plasmazellulären Entzündung chronisch erhöht ist (DiBartola 1997). Die genaue Prävalenz der Nierenbeteiligung bleibt schwer abzuschätzen in Abwesenheit einer systematischen Bewertung von Proteinurie und Nierenfunktion in veröffentlichten Kohorten. Die Empfehlung eines Urinprotein/Kreatinin-Verhältnisses (UPCR) bei Diagnose und bei Langzeitverlauf erscheint jedoch bei Katzen mit ausgeprägter Hypergammaglobulinämie oder chronischer Erkrankung seit mehr als sechs Monaten gerechtfertigt (Scarampella 2018).
9.3. Auf dem Weg zu einem einheitlichen nosologischen Spektrum
Die Akkumulation klinischer und histopathologischer Beobachtungen führt dazu, die plasmazelluläre Pododermatitis nicht als isolierte dermatologische Entität zu betrachten, sondern als ballenbezogene Manifestation eines systemischen plasmazellulären Syndroms der Katze. Dieses Konzept, implizit in den Arbeiten von Gruffydd-Jones bereits 1980, wurde von Guaguère und Bensignor formalisiert, die einen nosologischen Rahmen vorschlagen, der die Pododermatitis, plasmazelluläre Stomatitis, Immunkomplex-Glomerulonephritis und, seltener, extrapodalare plasmazelluläre Dermatitis, die die Ohrmuschel oder den Nasenplanum betrifft, integriert (Guaguère 2004). Die pathophysiologische Einheit dieses Spektrums beruht auf dem gemeinsamen Nenner einer Dysregulation der terminalen B-plasmazellulären Differenzierung mit überschüssiger polyklonaler Immunglobulinproduktion und Gewebeablagerung von Plasmazellen an anatomischen Stellen, die durch ihre lokale Immunmikroumgebung prädisponiert sind.
Dieses Modell erinnert durch Analogie an die monoklonalen Gammopathien unbestimmter Signifikanz (MGUS) und lymphoproliferative Syndrome niedrigen Grades in der Humanmedizin, ohne dass eine strenge Parallele gezogen werden kann aufgrund des polyklonalen – und nicht monoklonalen – Charakters der B-Aktivierung, die beim plasmazellulären Syndrom der Katze beobachtet wird (Mellor 2006). Die Grenze zwischen polyklonaler reaktiver Aktivierung und präneoplastischer klonaler Proliferation verdient es, durch B-Klonalitäts-Techniken (PCR-PARR, für PCR for Antigen Receptor Rearrangement) erforscht zu werden, die es ermöglichen würden, einen eventuellen dominanten Subklon innerhalb des scheinbar polyklonalen Infiltrats zu detektieren. Die Studie von Werner und Mitarbeitern, die die PARR-Technik auf plasmazelluläre Pododermatitis-Biopsien angewendet hat, bestätigte den polyklonalen Charakter in der Mehrheit der getesteten Fälle, aber eine oligoklonale Umlagerung wurde in etwa 15 % der Proben identifiziert und wirft die Frage einer möglichen Progression zu einem MALT-Lymphom (Mucosa-Associated Lymphoid Tissue) in bestimmten chronischen Fällen auf (Werner 2011).
Perspektiven und Forschungsrichtungen
10.1. Diagnostische und prognostische Biomarker
Die Entwicklung objektiver, nicht-invasiver oder minimal invasiver Biomarker stellt eine Priorität zur Verbesserung der Frühdiagnose, therapeutischen Überwachung und prognostischen Stratifizierung der plasmazellulären Pododermatitis der Katze dar. Die Serumprotein-Elektrophorese ist, obwohl nützlich zur Dokumentation der Hypergammaglobulinämie, für die Langzeitverfolgung nicht spezifisch und sensibel genug. Die Messung freier Leichtketten im Serum (sFLC, serum free light chains), weithin in der Humanhämatologie zur Überwachung monoklonaler Gammopathien und Myelome verwendet, stellt einen relevanten Biomarker-Kandidaten dar. Freie Kappa- und Lambda-Leichtketten werden bei plasmazellulärer Aktivierung im Überschuss produziert, und ihr κ/λ-Verhältnis spiegelt das Gleichgewicht oder Ungleichgewicht der klonalen B-Population wider (Bradwell 2001). Ein an feline Immunglobuline angepasster ELISA-Test wurde entwickelt, aber seine analytische und klinische Validierung im spezifischen Kontext der plasmazellulären Pododermatitis bleibt zu realisieren (Tasca 2018).
Serumzytokine bieten eine weitere Biomarker-Explorationsachse. Die Messung von IL-6, dessen Rolle beim plasmazellulären Überleben über STAT3-Aktivierung in der humanen Onkologie gut etabliert ist (Kishimoto 2005), könnte es ermöglichen, Patienten mit Risiko für systemische Formen (Glomerulonephritis, Amyloidose) zu identifizieren. Ebenso stellt Serum-BAFF (B-cell Activating Factor of the TNF Family), ein Hauptzytokin des Überlebens reifer B-Lymphozyten und Plasmazellen über die Aktivierung des nicht-kanonischen NF-κB-Wegs (RelB/p52), ein potenzielles Biomarker- und therapeutisches Ziel dar. Erhöhte BAFF-Spiegel wurden mit der Schwere systemischer Autoimmunerkrankungen beim Menschen korreliert (systemischer Lupus erythematodes, Sjögren-Syndrom), und die Extrapolation auf das plasmazelluläre Syndrom der Katze erscheint biologisch begründet, obwohl noch nicht experimentell erforscht (Mackay 2009).
Das Aufkommen der Gewebe-Transkriptomik durch RNA-Sequenzierung (RNA-seq), angewendet auf Ballenbiopsien, würde es ermöglichen, die Genexpression des plasmazellulären Infiltrats zu kartieren, mit dem therapeutischen Ansprechen assoziierte molekulare Signaturen zu identifizieren und potenziell bisher unbekannte therapeutische Ziele zu entdecken. Die sinkenden Kosten des Next-Generation-Sequencing machen diesen Ansatz im Rahmen multizentrischer Studien machbar, vorausgesetzt, eine Gewebebiobank wird koordiniert aufgebaut.
10.2. Aufkommende gezielte Therapien
Über die bereits erwähnten JAK-Inhibitoren hinaus könnten mehrere therapeutische Klassen, die in der Humanmedizin aufkommen, eine Anwendung beim plasmazellulären Syndrom der Katze finden. Anti-BAFF-Antikörper (Belimumab) und Anti-APRIL (A PRoliferation-Inducing Ligand, ein mit BAFF verwandter Ligand), die plasmazelluläre Überlebenssignale blockieren, haben eine Wirksamkeit bei humanem Lupus mit einer signifikanten Reduktion der Autoantikörper-Titer und einer Verringerung der Krankheitsaktivität gezeigt (Furie 2011). Die Entwicklung Katzen-spezifischer monoklonaler Anti-BAFF-Antikörper würde einen beträchtlichen Fortschritt darstellen, stößt aber auf die üblichen Hindernisse der Entwicklungskosten, der Produktion in GMP-Umgebung (Good Manufacturing Practice) und regulierter veterinärmedizinischer klinischer Studien.
Proteasom-Inhibitoren wie Bortezomib, die die Apoptose von Plasmazellen durch Akkumulation fehlgefalteter Proteine und Aktivierung des Stresswegs des endoplasmatischen Retikulums (UPR, Unfolded Protein Response) induzieren, stellen einen verführerischen Ansatz zur selektiven Zielrichtung der Effektorzellen der Erkrankung dar (Neubert 2008). Ihre Verwendung in der Veterinärmedizin bleibt auf die experimentelle Onkologie beschränkt, mit begrenzten toxikologischen Daten bei der Katze (Thrombozytopenie, potenzielle periphere Neurotoxizität).
Therapien auf Basis autologer regulatorischer T-Zellen, die ex vivo expandiert werden und darauf abzielen, die immunologische Toleranz durch adoptiven Transfer von CD4+CD25+FoxP3+ Treg wiederherzustellen, stellen den ehrgeizigsten Horizont der Immuntherapieforschung bei Autoimmunerkrankungen dar. Die beim Menschen entwickelten Protokolle für Zellsortierung, Expansion und Reinjektion (Bluestone 2015) könnten theoretisch an die Katze angepasst werden, aber die technischen und finanziellen Herausforderungen bleiben beträchtlich, und keine präklinische Studie wurde im spezifischen Kontext der plasmazellulären Pododermatitis initiiert.
Schlussfolgerung
Die plasmazelluläre Pododermatitis der Katze, lange als anekdotische dermatologische Kuriosität betrachtet, etabliert sich heute als faszinierendes klinisches Modell an der Schnittstelle von Dermatologie, Immunologie und veterinärmedizinischer Hämatologie. Das Verständnis dieser Erkrankung hat seit den Erstbeschreibungen von Gruffydd-Jones im Jahr 1980 substanziell Fortschritte gemacht und ist von einer rein deskriptiven Entität zu einem immunopathologischen Syndrom übergegangen, dessen molekulare Mechanismen – polyklonale plasmazelluläre Aktivierung, Dysregulation der IL-6/STAT3- und BAFF/NF-κB-Achsen, Immunkomplex-Ablagerungen – nun teilweise aufgeklärt sind. Das therapeutische Arsenal, dominiert von Doxycyclin und Ciclosporin, bietet zufriedenstellende Ansprechraten in der Mehrheit der Fälle, aber das rezidivierende Profil der Erkrankung und die Heterogenität individueller Antworten unterstreichen die Grenzen aktueller Ansätze. Das Konzept des systemischen plasmazellulären Syndroms der Katze, das Pododermatitis, plasmazelluläre Stomatitis und Nierenbeteiligung integriert, liefert einen kohärenten nosologischen Rahmen, der zukünftige Forschung zu einer systematischen Bewertung extrapodalaler Manifestationen und einer prognostischen Stratifizierung basierend auf objektiven Biomarkern leiten sollte. Das Aufkommen gezielter Therapien und regenerativer Medizinansätze bietet ermutigende Perspektiven, vorausgesetzt, die Veterinärgemeinschaft stattet sich mit prospektiven multizentrischen Studien und Fallregistern aus, die es ermöglichen, die statistischen Power zu erreichen, die zur Validierung dieser Innovationen erforderlich ist.
Literaturverzeichnis
Arzi B, Murphy B, Cox DP, Vapniarsky N, Kass PH, Verstraete FJ. Presence and quantification of mast cells in the gingiva of cats with tooth resorption, periodontitis and chronic stomatitis. Arch Oral Biol. 2010;55:148-154.
Backel KA, Cain CL, Mauldin EA. Canine and feline plasma cell pododermatitis: retrospective analysis of clinical and histopathologic findings. Vet Dermatol. 2013;24:404.
Bettenay SV, Mueller RS, Dow K, Friend S. Prospective study of the treatment of feline plasmacytic pododermatitis with doxycycline. Vet Rec. 2003;152:564-566.
Bluestone JA, Buckner JH, Fitch M, Gitelman SE, Gupta S, Helber MK. Type 1 diabetes immunotherapy using polyclonal regulatory T cells. Sci Transl Med. 2015;7:315ra189.
Bradwell AR, Carr-Smith HD, Mead GP, Tang LX, Showell PJ, Drayson MT, Drew R. Highly sensitive, automated immunoassay for immunoglobulin free light chains in serum and urine. Clin Chem. 2001;47:673-680.
Cain DW, Cidlowski JA. Immune regulation by glucocorticoids. Nat Rev Immunol. 2017;17:233-247.
Center SA, Smith CA, Wilkinson E, Erb HN, Lewis RM. Clinicopathologic, renal immunofluorescent, and light microscopic features of glomerulonephritis in the dog. J Am Vet Med Assoc. 1990;190:81-90.
de Mari K, Maynard L, Eun HM, Lebreux B. Treatment of canine parvoviral enteritis with interferon-omega in a placebo-controlled field trial. Vet Rec. 2004;152:105-108.
DiBartola SP, Tarr MJ, Webb DM, Giger U. Familial renal amyloidosis in Chinese Shar-Pei dogs. J Am Vet Med Assoc. 1997;197:483-487.
Furie R, Petri M, Zamani O, Cervera R, Wallace DJ, Tegzová D. A phase III, randomized, placebo-controlled study of belimumab, a monoclonal antibody that inhibits B lymphocyte stimulator, in patients with systemic lupus erythematosus. Arthritis Rheum. 2011;63:3918-3930.
German AJ, Cannon MJ, Dye C, Booth MJ, Pearson GR, Reay CA. Oesophageal strictures in cats associated with doxycycline therapy. J Feline Med Surg. 2005;7:33-41.
Gonzales AJ, Bowman JW, Fici GJ, Zhang M, Mann DW, Mitton-Fry M. Oclacitinib (APOQUEL) is a novel Janus kinase inhibitor with activity against cytokines involved in allergy. J Vet Pharmacol Ther. 2014;37:317-324.
Groux H, O’Garra A, Bigler M, Rouleau M, Antonenko S, de Vries JE. A CD4+ T-cell subset inhibits antigen-specific T-cell responses and prevents colitis. Nature. 1997;389:737-742.
Gruffydd-Jones TJ, Orr CM, Lucke VM. Foot pad swelling and ulceration in cats: a report of five cases. J Small Anim Pract. 1980;21:31-40.
Guaguère E, Bensignor E. Pododermatite plasmocytaire féline. Prat Méd Chir Anim Comp. 2004;39:29-36.
Harley R, Gruffydd-Jones TJ, Day MJ. Immunohistochemical characterization of oral mucosal lesions in cats with chronic gingivostomatitis. J Comp Pathol. 2003;128:147-160.
Kishimoto T. Interleukin-6: from basic science to medicine — 40 years in immunology. Annu Rev Immunol. 2005;23:1-21.
Last RD, Suzuki Y, Manning T, Lindsay D, Galipeau L, Bhopale V. A case of fatal systemic toxoplasmosis in a cat being treated with cyclosporin A for feline atopy. Vet Dermatol. 2004;15:194-198.
Latimer KS. Duncan and Prasse’s Veterinary Laboratory Medicine: Clinical Pathology. 5. Aufl. Wiley-Blackwell; 2014.
Lowe AD, Campbell KL, Graves TK. Glucocorticoids in the cat. Vet Dermatol. 2008;19:340-347.
Mackay F, Schneider P. Cracking the BAFF code. Nat Rev Immunol. 2009;9:491-502.
Mellor PJ, Haugland S, Smith KC, Powell RM, Gaskell RM, Knottenbelt CM, Argyle DJ. Histopathologic, immunohistochemical, and cytologic analysis of feline myeloma-related disorders: further evidence for primary extramedullary development in the cat. Vet Pathol. 2006;43:234-246.
Neubert K, Meister S, Moser K, Tolber C, Peddinghaus A, Nimmerjahn F, Schett G, Voll RE. The proteasome inhibitor bortezomib depletes plasma cells and protects mice with lupus-like disease from nephritis. Nat Med. 2008;14:748-755.
Niimi A, Torigoe R, Sato M. Immunomodulatory effects of tetracyclines on human T-lymphocyte proliferative response. Clin Exp Immunol. 1998;111:328-332.
Ortalda C, Noli C, Colombo S, Borio S. Oclacitinib in feline nonflea-, nonfood-induced hypersensitivity dermatitis: results of a small prospective pilot study of client-owned cats. Vet Dermatol. 2015;26:235-e52.
Quimby JM, Webb TL, Habenicht LM, Dow SW. Safety and efficacy of intravenous infusion of allogeneic cryopreserved mesenchymal stem cells for treatment of chronic kidney disease in cats: results of three sequential pilot studies. Stem Cell Res Ther. 2013;4:48.
Roberts ES, Speranza C, Friberg C, Griffin C, Steffan J, Roycroft L, Alva R. Confirmatory field study for the effectiveness and safety of cyclosporine in the control of feline hypersensitivity dermatitis. J Vet Pharmacol Ther. 2016;39:487-493.
Robson D, Burton G. Cyclosporin: applications in small animal dermatology. Vet Dermatol. 2003;14:1-9.
Sapadin AN, Fleischmajer R. Tetracyclines: nonantibiotic properties and their clinical implications. J Am Acad Dermatol. 2006;54:258-265.
Scarampella F, Ordeix L. Doxycycline therapy in 10 cases of feline plasma cell pododermatitis: clinical, haematological and serological evaluations. Vet Dermatol. 2018;29:467-e158.
Tasca S, Carli E, Caldin M, Menegazzo L, Furlanello T, Solano-Gallego L. Serum free light chain concentrations in dogs and cats with various diseases. Vet Clin Pathol. 2018;47:419-427.
Taylor JE, Schmeitzel LP. Plasma cell pododermatitis with chronic footpad hemorrhage in two cats. J Am Vet Med Assoc. 2004;197:375-377.
Werner AH, Gruendl S, Geisweid K, Mueller RS. Clonality testing in feline lymphoma by PCR for antigen receptor rearrangement (PARR). Vet Immunol Immunopathol. 2011;143:181-186.
White SD, Rosychuk RAW, Janik TA, Denerolle P, Schultheiss P. Plasma cell stomatitis-pharyngitis in cats: 40 cases (1973-1991). J Am Vet Med Assoc. 2000;200:1377-1380.