I lieviti del genere Malassezia costituiscono agenti fungini lipofili evolutisi come commensali cutanei e patogeni opportunisti in diverse specie di mammiferi e uccelli. Il loro coinvolgimento nelle affezioni dermatologiche e otologiche canine e feline rappresenta una sfida clinica quotidiana per i medici veterinari a livello mondiale. Durante l’ultimo congresso NAVDF a Orlando, il nostro collega Ross Bond, specialista mondiale sull’argomento, ha avuto l’occasione di fare un punto completo, sia patogenico che diagnostico e terapeutico.
Storico e tassonomia dei lieviti Malassezia
L’associazione tra i lieviti Malassezia e l’otite esterna canina risale ai lavori pionieristici di Bengt Gustafson, che pubblicò nel 1955 la sua tesi a Stoccolma riguardante 201 casi di otite esterna principalmente acuta nel cane. Il Cocker Spaniel costituiva la razza più rappresentata in questo studio, ed è notevole che questa predisposizione razziale sia ancora riconoscibile nella pratica clinica contemporanea. Gustafson isolò i lieviti da soli in 108 casi e lieviti associati a stafilococchi nella maggioranza dei casi rimanenti, un’osservazione che i medici che effettuano quotidianamente citologia riconosceranno immediatamente come familiare.
Osservò che la frequenza dei lieviti diminuiva nei casi cronici, lasciando spazio a infezioni da Proteus e Pseudomonas, constatazione con la quale la comunità veterinaria contemporanea sarebbe unanimemente d’accordo. Su 97 orecchie sane esaminate, rilevò solo una debole crescita di lieviti in otto casi soltanto. Le caratteristiche morfologiche di questi lieviti — forma ovale, gemmazione polare, assenza di micelio, crescita lenta e assenza di fermentazione — condussero Gustafson a collegarli al genere Pityrosporum, oggi denominato Malassezia. Dopo consultazione del Bureau Central delle Culture Fungine nei Paesi Bassi, e di fronte all’assenza di ceppo di riferimento disponibile (l’isolato di rinoceronte degli anni 1930 essendo scomparso), propose temporaneamente l’appellativo Pityrosporum canis.
I suoi esperimenti dimostrarono che un’inoculazione di questo lievito in cani sani induceva un’otite transitoria leggera, e che l’applicazione di agar maltato addizionato di olio d’oliva nel condotto uditivo favoriva la proliferazione di Malassezia e la comparsa di un’otite. Queste osservazioni permisero a Gustafson di concludere che Pityrosporum canis rappresentava una causa di otite e che questa affezione poteva insorgere per attivazione di lieviti residenti normalmente nel condotto uditivo esterno.
Settant’anni dopo, il consenso scientifico conferma pienamente che M. pachydermatis costituisce un patogeno otico opportunista secondario che necessita di una forma di predisposizione o di un’anomalia auricolare preesistente per generare un’otite clinicamente significativa. Il Dr. Gustafson aveva quindi correttamente identificato i meccanismi fondamentali di questa patologia già dalla metà del ventesimo secolo.
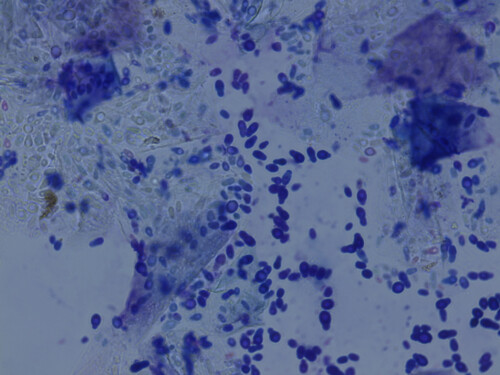
Aspetto classico di Malassezia pachydermatis
Storico della dermatite da Malassezia
Per quanto riguarda la dermatite da Malassezia nel cane, i primi rapporti sono attribuiti al medico belga Dufait, che pubblicò diversi articoli alla fine degli anni 1970 e all’inizio degli anni 1980 descrivendo questa affezione. Il professor Larson in Brasile contribuì ugualmente con la pubblicazione di serie di casi documentanti le manifestazioni cliniche di questa patologia emergente. Ken Mason riprese poi il testimone presentando queste osservazioni durante diverse riunioni scientifiche e conferenze professionali. La prima menzione di dermatite da Malassezia durante un congresso dell’AAVD/NAVDF risale probabilmente al 1987 a Phoenix, Arizona, dove Ken Mason presentò un riassunto descrivente tre casi canini.
Riconoscimento e accettazione clinica
Questa presentazione iniziale suscitò una ricezione contrastante in seno alla comunità scientifica, alcuni medici rimanendo scettici circa la pertinenza patogenica di questo lievito nel contesto dermatologico. L’accettazione progressiva della rilevanza clinica di questo lievito ne seguì, e la dermatite da Malassezia fa ormai parte integrante della pratica veterinaria quotidiana in medicina dei piccoli animali a livello mondiale.
Evoluzione tassonomica e complessità del genere
Origini della nomenclatura
Il genere Malassezia fu osservato per la prima volta nel 1846 e inizialmente denominato Cryptococcus. Malassez descrisse in seguito queste spore nelle cellule di forfora umana, stabilendo così il legame tra questi organismi e le affezioni desquamative del cuoio capelluto umano. Il nome di genere Malassezia fu proposto in riconoscimento dei lavori di questo ricercatore, poi modificato da Sabouraud in Pityrosporum, prima di essere ristabilito negli anni 1980 nella sua denominazione originale.
Classificazione lipidica e morfologica
La tassonomia iniziale era relativamente semplice e comprensibile: tutti i lieviti Malassezia erano riconosciuti come lipofili, e quelli strettamente dipendenti dai lipidi, necessitanti terreni di coltura speciali supplementati con sostanze grasse, erano raggruppati sotto la specie unica Malassezia furfur. I micologi eminenti dell’epoca, come Evelyn Guého e Gillian Midgley, sottolineavano tuttavia l’esistenza di una grande diversità morfologica in seno a questo gruppo, distinguendo diverse forme ovali designate come forma ovale 1, forma ovale 2, forma ovale 3, e così via. La diversità morfologica suggeriva fortemente l’esistenza di molteplici specie distinte in seno a questo raggruppamento tassonomico inizialmente considerato come monospecifico.
Specificità di Malassezia pachydermatis
Malassezia pachydermatis, la specie predominante nei carnivori e senza dubbio la più pertinente per la pratica veterinaria, era classificata come non-dipendente dai lipidi perché capace di crescere su agar Sabouraud Destrosio, il terreno di coltura micologico di routine. Le specie lipofile umane dimostrano la loro importanza clinica in diverse affezioni dermatologiche come la Pityriasis versicolor, caratterizzata in citologia dall’aspetto classico a “spaghetti e polpette” della fase pseudoifale di quello che era anticamente denominato M. orbiculare, così come nella dermatite seborroica del cuoio capelluto.
Apporto della micologia molecolare
L’avvento delle tecniche di micologia molecolare ha considerevolmente complicato la tassonomia del genere. Il sequenziamento completo del genoma di M. pachydermatis rivelò che essa appartiene in realtà al gruppo strettamente lipodipendente, poiché condivide con le altre specie l’assenza del gene codificante per la sintasi degli acidi grassi. La sua capacità apparentemente paradossale di crescere su agar Sabouraud si spiega con la presenza sufficiente di acido palmitico nel componente peptone di questo terreno, quantità adeguata per supportare la crescita di questa specie ma insufficiente per le altre specie più esigenti. Le altre specie necessitano una supplementazione lipidica marcata e sostanziale per la loro coltura in laboratorio.
Specie feline e diversità animale
Nei gatti, diverse specie strettamente lipofile sono state isolate in coltura con conferma molecolare susseguente dell’identificazione delle colonie, in particolare M. sympodialis, M. globosa, M. furfur, M. nana (particolarmente nel condotto uditivo) e M. slooffiae (in particolare a livello delle pieghe ungueali). Rui Kano fu il primo a descrivere M. nana nei gatti e nei bovini, stabilendo così l’importanza di questa specie in queste popolazioni animali. Altre specie sono principalmente associate alla pelle umana in coltura, mentre alcune sono legate a ospiti animali specifici: M. caprae nelle capre, M. equina nei cavalli, M. gallinae nei polli, e M. botryllophilus nei pipistrelli. La distinzione tra queste specie non può effettuarsi unicamente tramite coltura; un test molecolare di sequenziamento rimane necessario per un’identificazione precisa e definitiva. Questa complessità tassonomica crescente solleva questioni importanti riguardanti la pertinenza clinica di questa diversità di specie. La capacità di identificare precisamente la specie implicata in un caso clinico dato potrebbe potenzialmente influenzare le decisioni terapeutiche, particolarmente nel contesto dell’emergenza della resistenza agli antifungini.
Ecologia cutanea e distribuzione anatomica
Meccanismo della patogenicità
La transizione da uno stato commensale a quello di patogeno si osserva frequentemente quando l’equilibrio omeostatico tra l’immunità dell’ospite e la virulenza fungina si trova perturbato, necessitando un approccio terapeutico mirato associato all’identificazione e alla correzione dei fattori predisponenti sottostanti.
Colonizzazione commensale nel cane
Malassezia pachydermatis costituisce un abitante normale della cute e delle mucose sane del cane, facendo parte integrante del microbioma cutaneo commensale. Uno studio su 40 cani sani realizzato molti anni fa rivelò una frequenza di isolamento in coltura superiore al 30% a livello del condotto uditivo, confermando che questa localizzazione anatomica rappresenta un serbatoio maggiore di colonizzazione commensale. Al contrario, l’ascella, l’inguine e il dorso presentavano un tasso di isolamento inferiore o uguale al 10%, suggerendo una colonizzazione molto più sporadica e limitata di questi siti. Per rilevare questo lievito sulla pelle di un animale sano con metodo culturale, i siti di predilezione sono lo spazio interdigitale e la regione delle labbra, dove i tassi di recupero in coltura si rivelano significativamente superiori. Tra i siti mucosi, l’ano rappresenta la localizzazione privilegiata, con più del 50% degli animali che presentano una colonizzazione anale rilevabile tramite coltura. Uno studio temporale con prelievi settimanali confermò che l’ano rimane il sito dove il lievito persiste in modo più costante nel corso del tempo, gli altri siti mostrando una colonizzazione più intermittente e variabile.
Presenza nel tratto gastrointestinale
Osservazioni inattese e inizialmente sorprendenti sono emerse riguardo alla presenza di Malassezia nel tratto gastrointestinale. Uno studio ulteriore condotto in collaborazione con Arti Kathrani, internista specializzata, e Bart Theelen, che lavorava all’epoca all’Istituto di Biodiversità Fungina Westerdijk nei Paesi Bassi (attualmente in Minnesota), riguardante 45 cani affetti da enteropatia e sottoposti a endoscopia per diverse indagini diagnostiche, permise di coltivare Malassezia in otto di essi, confermando le osservazioni preliminari e stabilendo la presenza autentica di questi lieviti nell’intestino tenue canino.
Microbioma cutaneo e diversità delle specie
Gli studi di microbioma utilizzanti tecniche molecolari hanno rivelato una diversità inattesa di specie di Malassezia sulla cute canina, in particolare tramite rilevazione di DNA. Richard Harvey, clinico e ricercatore rinomato, pubblicò recentemente uno studio di microbioma realizzato in collaborazione con alcuni espositori presenti nell’esposizione commerciale di conferenze veterinarie. Uno studio che esaminava la regione ombelicale di 20 cani sani identificò Cladosporium in tutti gli individui e M. pachydermatis in solo due di essi, confermando i risultati degli studi culturali classici anteriori. Al contrario, DNA di M. sympodialis, M. restricta, M. slooffiae e M. arunalii fu ugualmente rilevato tramite metodi molecolari. Queste osservazioni contrastano in modo sorprendente con i risultati di coltura, costituendo un’osservazione particolarmente intrigante e scientificamente sconcertante. Su 31 anni di coltura sistematica di Malassezia a partire da cute canina su terreni supplementati con lipidi concepiti teoricamente per supportare la crescita di tutte le specie di Malassezia, una sola occasione permise di isolare altro che M. pachydermatis. Similmente, nello studio intestinale menzionato precedentemente, M. sympodialis fu coltivata una sola volta sull’insieme dei campioni.
Ipotesi sulla divergenza Molecolare/Coltura
Questa divergenza stupefacente tra rilevazione molecolare e coltura solleva diverse ipotesi esplicative fondamentali: i terreni di coltura potrebbero non essere ottimali per tutte le specie lipofile esigenti nonostante le supplementazioni lipidiche applicate, queste specie potrebbero essere presenti in numeri bassi sotto la soglia di rilevazione culturale rendendo il loro isolamento poco probabile, microcolonie miste potrebbero esistere con persistenza preferenziale di M. pachydermatis durante i subcoltivi successivi conducendo alla perdita delle altre specie più fragili, o il DNA rilevato potrebbe non corrispondere a organismi vitali ma piuttosto a materiale genetico proveniente da cellule morte o danneggiate. Una contaminazione della cute canina da parte di DNA di Malassezia umana trasferito tramite manipolazione e contatto rimane ugualmente ipotizzabile, particolarmente in un contesto dove le interazioni uomo-animale sono frequenti e intime.
Osservazioni ambientali
Una scoperta recente particolarmente sorprendente proviene da uno studio pubblicato riguardante le foglie di vite di vigneti italiani, dove Cladosporium e Malassezia furono identificati come i funghi più abbondanti in questo substrato vegetale. Questa osservazione si rivela inusuale poiché Malassezia non è generalmente considerata come un organismo vegetale ma piuttosto come un abitante obbligatorio della cute dei mammiferi, sollevando questioni intriganti riguardanti l’ecologia globale di questo genere fungino.
Microbioma e dermatite atopica
Cody Meason Smith, micologa eminente che lavora in collaborazione con il Dr. Hoffman, pubblicò una gamma notevole di studi sul microbioma cutaneo canino. Nei cani da laboratorio in buona salute, le analisi molecolari mostrano che M. restricta e M. globosa predominano, esattamente come nella cute umana sana. Al contrario, nei cani da laboratorio che subiscono episodi di dermatite atopica canina sperimentalmente indotta, M. pachydermatis e M. restricta diventano le più abbondanti nelle analisi molecolari, con rilevazione in sottofondo di specie più strettamente lipofile ugualmente.
La questione di Malassezia globosa
Questa osservazione riguardante M. globosa solleva interrogativi clinici importanti. M. globosa presenta una morfologia sferica caratteristica con una gemmazione spessa e prominente, distinta dal germoglio stretto osservato in alcune specie di Candida. Sebbene lieviti rotondi siano talvolta osservati in citologia, in particolare di origine auricolare, essi non corrispondono alle osservazioni citologiche di routine nella maggioranza delle cliniche veterinarie. La questione rimane quindi: se M. globosa è importante e presente secondo gli studi molecolari, perché non la si osserva in citologia di routine?
Limiti delle colture e contaminazione
Diverse spiegazioni possono essere proposte per questa discordanza apparente. I terreni di coltura attuali, anche quelli arricchiti con lipidi come l’agar Dixon modificato, potrebbero non essere sufficientemente ottimali per coltivare tutte queste diverse specie di Malassezia dalle esigenze nutrizionali strette e variate. Queste specie potrebbero essere presenti in numero insufficiente, al di sotto della soglia di rilevazione tramite coltura tradizionale, non generando sufficienti colonie per essere notate. Il fenomeno di microcolonie miste costituisce un’altra spiegazione plausibile. Durante i subcoltivi successivi di colonie miste, M. pachydermatis, specie facile da coltivare e a crescita rapida, potrebbe persistere mentre le specie lipofile più esigenti e a crescita lenta potrebbero progressivamente morire e scomparire. Il DNA molecolare rilevato indica la presenza di DNA ma non conferma necessariamente la presenza di organismi vitali e metabolicamente attivi. Materiale genetico proveniente da cellule morte o degradate potrebbe persistere nell’ambiente cutaneo ed essere rilevato tramite amplificazione PCR. La contaminazione della cute canina da parte di DNA di Malassezia umana trasferito tramite manipolazione, carezze e contatti stretti tra proprietari e animali potrebbe ugualmente contribuire ad alcuni dei risultati molecolari osservati. Problemi tecnici metodologici negli studi di microbioma, sebbene al di fuori del campo di competenza dermatologica, potrebbero ugualmente influenzare i risultati e la loro interpretazione.
Influenza climatica
I lieviti Malassezia risiedono nello strato corneo, a livello di ciò che Bart Theelen, micologo eminente, chiamerebbe la zona del mantello transizionale, dove subiscono l’influenza di fattori climatici come il calore e l’umidità ambientali. La pratica dermatologica a Londra, situata a 4.400 miglia a nord-est della localizzazione di questa conferenza, si effettua in un clima molto più fresco e molto meno umido rispetto a numerose regioni nordamericane. L’incubatore di laboratorio micologico funziona come un incubatore umido a 32 gradi Celsius, riproducendo le condizioni ottimali per la crescita dei lieviti. Numerosi cani nel mondo vivono in ambienti umidi e caldi, sia tutto l’anno nelle regioni tropicali e subtropicali, sia durante i mesi estivi nelle regioni temperate. I cani che vivono in tali condizioni climatiche, particolarmente quelli del sud-est degli Stati Uniti, presentano una frequenza aumentata di proliferazione di Malassezia secondo i rapporti di medici che esercitano in diverse zone geografiche e climatiche.
Interazioni con l’ospite e i batteri
I lieviti nello strato corneo sono influenzati dalla chimica dell’ospite e dai fattori immunitari in senso lato, includendo l’immunità innata e adattativa. Essi metabolizzano i lipidi sebacei prodotti dalle ghiandole sebacee e i lipidi derivati dai cheratinociti, substrati abbondanti nello strato corneo a causa della loro necessità per il metabolismo dei lieviti lipodipendente. Le loro interazioni con i batteri cutanei commensali e patogeni rimangono mal comprese e costituiscono un campo necessitante ricerche approfondite. Una pubblicazione recente indicava che alcune specie lipofile di Malassezia presenti sulla cute umana interagiscono con Staphylococcus aureus e riducono la sua tendenza alla formazione di biofilm, suggerendo un ruolo potenzialmente benefico nella regolazione della virulenza batterica e la modulazione dell’ecologia microbica cutanea. Questi lieviti commensali potrebbero quindi esercitare effetti protettivi limitando la patogenicità di altri microrganismi cutanei, aggiungendo una complessità supplementare alla nostra comprensione dell’ecologia microbica cutanea.
Patogenesi e meccanismi di virulenza
Produzione enzimatica e attività metabolica
I funghi, organismi nutrizionalmente assorbenti, liberano una vasta gamma di enzimi nel loro ambiente per creare substrati assimilabili dalla cellula fungina attraverso la parete cellulare e la membrana cellulare. Questi enzimi, particolarmente durante proliferazioni di lieviti marcate e massive, possiedono il potenziale di danneggiare le cellule epidermiche dell’ospite e di attivare i sistemi immunitari innati e specifici. La parete cellulare di Malassezia contiene molecole di adesione facilitanti l’aderenza alle squame cornee, un processo che può essere quantificato passando settimane a contare microscopicamente le cellule di Malassezia per determinare se aderiscono alle squame o no e a esaminare i fattori molecolari implicati in questo processo. Questi lieviti presentano epitopi di legame alle IgE responsabili di reazioni di ipersensibilità immediata e motivi molecolari associati ai patogeni (PAMPs), riconosciuti dalle cellule immunitarie tramite recettori di lectina di tipo C, così come dalle cellule T helper 17. L’importanza crescente dei linfociti T helper 17 nell’immunità fungina, sia innata che adattativa, è sempre più documentata nella letteratura scientifica contemporanea, sebbene i meccanismi immunologici dettagliati superino il campo di competenza dermatologica e necessitino consultazione della letteratura specializzata in immunologia per una comprensione approfondita.
Lipasi e biochimica cutanea
In medicina umana, le lipasi fungine svolgono un ruolo riconosciuto e ben stabilito nello sviluppo della forfora e della dermatite seborroica del cuoio capelluto. Aristea Velegraki e i suoi collaboratori hanno dimostrato che la lipoperossidazione dello squalene genera metaboliti riconosciuti come marcatori biochimici della cute con forfora, potenzialmente implicati nella patogenesi di questa affezione. Tuttavia, lo squalene non rappresenta un componente maggiore del sebo canino, contrariamente al sebo umano dove costituisce una frazione lipidica sostanziale.
Caratterizzazione enzimatica e fosfolipasi
Kit commerciali come API Zym permettono di caratterizzare le attività enzimatiche del surnatante di coltura e del pellet cellulare di una coltura in brodo. Dopo centrifugazione del pellet cellulare di una coltura in brodo, le attività enzimatiche possono essere rilevate nel kit di test. Alcuni enzimi appaiono associati al pellet cellulare piuttosto che al surnatante, mentre altri sono più abbondanti nel surnatante che nella cellula, e alcuni presentano livelli equivalenti nelle due frazioni. M. pachydermatis produce tutta una gamma di enzimi, includendo esterasi e lipasi. La produzione di fosfolipasi si rivela particolarmente importante in M. pachydermatis, con livelli più elevati nei ceppi associati alla cute lesionale comparativamente agli isolati di cute sana, e in certi genotipi maggiormente associati alle affezioni cutanee che alla colonizzazione commensale.
Virulenza ed espressione proteica
La compianta Claudia Cafarchia, sfortunatamente deceduta recentemente, e il suo gruppo di ricerca hanno dimostrato l’importanza della produzione di fosfolipasi, mostrando livelli enzimatici superiori nei ceppi patogeni. La somministrazione di azoli, farmaci fungistatici, disturba la produzione enzimatica dei lieviti, così come gli oli essenziali secondo alcune pubblicazioni. Una proliferazione importante di Malassezia genera quindi una produzione enzimatica massiva potenzialmente implicata nella patogenesi della dermatite e dell’otite. Lavori recenti che coinvolgono Thomas Dawson e diversi collaboratori hanno sottolineato l’importanza di studiare l’espressione delle proteine fungine in ambienti fisiologicamente pertinenti piuttosto che in condizioni artificiali di laboratorio. Una coltura in brodo non riproduce le condizioni fisiologiche dello strato corneo, e l’espressione proteica dei lieviti in questo ambiente naturale differisce sostanzialmente da quella ottenuta in brodo artificiale. Questi autori hanno sviluppato tecniche scientifiche sofisticate per dimostrare l’espressione proteica dei lieviti direttamente nello strato corneo, rivelando profili di espressione differenti da quelli osservati in coltura liquida.
Sperimentazioni animali e transizione commensale-patogeno
Sperimentazioni su beagle da laboratorio hanno mostrato che un’applicazione quotidiana di Malassezia sulla cute sotto occlusione durante una settimana permetteva di creare una placca locale di dermatite con essudato grasso bruno aggrovigliante i peli, simile alle lesioni osservate in clinica corrente. Tuttavia, l’interruzione dell’applicazione conduceva a una guarigione completa in una settimana, dimostrando che la cute normale controlla quindi efficacemente la sua popolazione di Malassezia e non sviluppa infezione tramite semplice applicazione esterna. Questi lavori furono realizzati nel quadro dell’Home Office Scientific Procedures Act, legislazione britannica rigorosa regolante l’utilizzo degli animali in un ambiente scientifico sperimentale e garantente il benessere animale. Un’alterazione sottostante si rivela necessaria per permettere la proliferazione dei lieviti patologica e lo sviluppo di segni clinici. Come i clinici riconoscono e comprendono bene, la cute normale non si infetta semplicemente tramite applicazione di lieviti. Qualcosa deve essere alterato fondamentalmente per permettere a questo lievito commensale di proliferare in modo opportunista e di generare una malattia clinicamente significativa.
Fattori predisponenti e affezioni sottostanti
Diversità dei fattori scatenanti
Le linee guida consensuali hanno stabilito una lista dei fattori predisponenti includendo la razza, l’allergia, i difetti di desquamazione, le endocrinopatie, le pieghe cutanee, il clima e i casi non identificati. Questa lista comporta implicazioni cliniche maggiori necessitanti una comprensione approfondita. Nei casi non identificati, rappresentanti la categoria più frustrante, l’assenza di comprensione del fattore scatenante iniziale impedisce qualsiasi correzione e conduce inevitabilmente a una malattia cronica ricorrente e recidivante, generando frustrazione intensa nel proprietario e necessità di trattamenti continui e ripetuti senza risoluzione definitiva.
Gestione delle allergie
In presenza di allergia come fattore predisponente, l’eliminazione completa dei lieviti tramite un antifungino, per quanto efficace sia e anche il miglior farmaco antifungino conosciuto dagli umani, non sopprime i segni allergici residui persistenti. Se l’unico criterio di successo terapeutico per il proprietario è la scomparsa completa dell’eritema e del prurito, il fallimento a breve termine è inevitabile e prevedibile, salvo se il proprietario è correttamente informato in modo trasparente della risposta parziale attesa in queste circostanze particolari. Il cane Westie Highland White Terrier classico fuori controllo con i farmaci convenzionali illustra perfettamente questa situazione: il trattamento di Malassezia e degli stafilococchi rivela una dermatite atopica sottostante che diventa allora controllabile con terapie appropriate. I difetti primari di cornificazione costituiscono una condizione permanente e irreversibile. Il cane possiede intrinsecamente questo disturbo di cheratinizzazione e ne rimane affetto in modo continuo. Le pieghe cutanee persistono salvo intervento dietetico permettente la loro riduzione tramite perdita di peso sostanziale o resezione chirurgica definitiva. Se gli animali presentano pieghe anatomiche, allora queste pieghe persistono indefinitamente a meno di essere rese più piccole tramite modificazione ponderale o rimosse chirurgicamente. I brachicefali costituiscono ugualmente una categoria particolarmente a rischio, in particolare nel Regno Unito, dove la prevalenza del Bouledogue Francese è fortemente aumentata.

Il Basset Hound è frequentemente interessato dalle dermatiti da Malassezia
Dermatite atopica e disturbi della cheratinizzazione
L’allergia, particolarmente la dermatite atopica, costituisce il fattore scatenante predominante in numerosi ospedali veterinari. In alcuni ospedali specializzati, il 50% dei casi di dermatite da Malassezia presentano una dermatite atopica come scatenante sottostante probabile. Uno studio utilizzante placche di contatto come metodo di coltura realizzato da studenti nel quadro di un progetto di ricerca dimostrò che gli animali sani presentavano una bassa frequenza di isolamento e popolazioni molto basse di Malassezia, mentre gli atopici mostravano una frequenza di isolamento e popolazioni significativamente più elevate sul piano statistico. La colonna verde-bluastra rappresentante gli animali sani sul grafico mostra una bassa frequenza e popolazioni molto basse, mentre gli atopici in rosso dimostrano isolamenti molto più frequenti e popolazioni considerevolmente più elevate ugualmente.
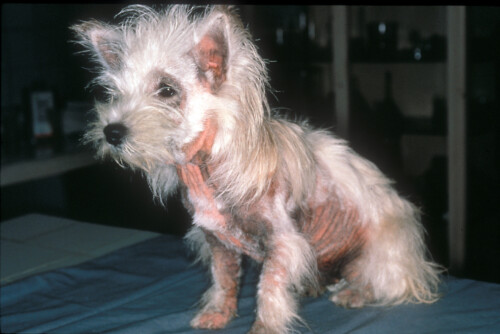
Westie atopico che presenta una dermatite da Malassezia
Complicazioni della dermatite atopica
I cani atopici complicati non presentano semplicemente una dermatite atopica pura e semplice. In numerosi casi, esiste ugualmente una dermatite secondaria da Malassezia che aggrava considerevolmente la severità clinica globale. Circa due terzi dei cani atopici sviluppano problemi di piodermite superficiale e un terzo sviluppa un problema di dermatite da Malassezia. Elizabeth Molterdin e i suoi colleghi hanno pubblicato uno studio molto bello e notevole in Veterinary Pathology qualche anno fa, facente riferimento all’ittiosi congenita autosomica recessiva osservata nei Bouledogue Americani. Questo studio dimostra elegantemente che i cuccioli squamosi affetti da questo disturbo di cheratinizzazione genetico diventano eritematosi e pruriginosi quando sono colonizzati da Malassezia, contrariamente ai cuccioli sani non affetti che non sviluppano segni clinici nonostante un’esposizione similare. Il disturbo della desquamazione influenza quindi l’epidermide in modo da favorire la proliferazione opportunista di Malassezia e la comparsa di segni clinici di infiammazione e prurito.
Predisposizione razziale e anatomica
Alcune razze presentano una predisposizione particolarmente marcata alla dermatite da Malassezia. Il Basset Hound seborroico costituisce l’esempio paradigmatico, mostrando una densità di popolazione mediana di Malassezia nell’ascella dell’ordine di 10^5, cioè 100.000 volte superiore a quella dei cani di razza mista sani utilizzati come gruppo controllo. I Basset Hound sani presentano popolazioni intermedie, con una sovrapposizione sostanziale tra individui sani e malati sui grafici di distribuzione. Una quantità sostanziale di Malassezia può quindi essere presente su una cute di apparenza clinicamente normale, secondo gli enzimi prodotti dai lieviti e la reattività immunologica cutanea dell’ospite.
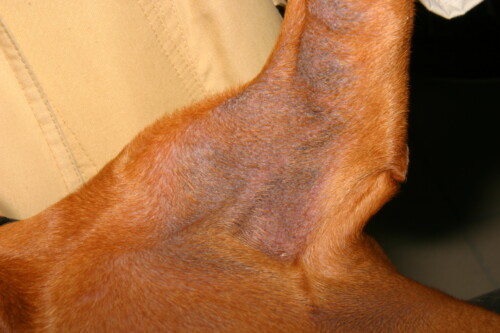
Le orecchie sono frequentemente interessate dalla dermatite da Malassezia
Predisposizione felina (Devon Rex, Sphinx)
Nei gatti, il Devon Rex si comporta come il Basset Hound nel mondo felino, rappresentando l’equivalente felino di questa razza canina predisposta. Questi gatti presentano una suscettibilità marcata a Malassezia. Uno studio su placca di contatto nell’ascella dei gatti dimostra che i gatti randagi non presentano molta Malassezia, i Cornish Rex non presentano Malassezia, mentre i Devon Rex seborroici con deposito seborroico nero mostrano una crescita sulla placca di contatto. I Devon Rex sani costituiscono un gruppo intermedio tra questi estremi. I gatti Sphinx, strettamente imparentati geneticamente ai Devon Rex ma sprovvisti di pelliccia, sviluppano frequentemente un’otite da Malassezia precocemente nella loro vita, spesso già in giovane età.
Zone anatomiche a rischio
Le pieghe cutanee costituiscono zone di predilezione anatomica per la proliferazione di Malassezia. La piega ombelicale dei Basset Hound femmine intere rappresenta una localizzazione frequentemente affetta, mostrando spesso un materiale aderente ai fusti piliferi. Le pieghe facciali dei brachicefali, in particolare i Bouledogue Francesi la cui prevalenza è esplosa nel Regno Unito e in America del Nord, rappresentano localizzazioni frequenti di dermatite da Malassezia. Sebbene questa situazione costituisca un disastro per il benessere animale a causa dei molteplici problemi di salute affliggenti queste razze brachicefale estreme, essa assicura paradossalmente la viabilità finanziaria di numerose cliniche veterinarie generando un volume importante di consultazioni e trattamenti.
Otite da Malassezia: patogenia ed ecologia microbica
Transizione dalla flora commensale a patogena
Nel contesto dell’otite, Malassezia agisce come patogeno secondario opportunista, e lo schema concettuale dell’otite distinguente fattori di predisposizione, primari, secondari e perpetuanti si rivela molto utile per delimitare tutti gli elementi spieganti i casi otologici problematici e refrattari.
Analisi quantitativa della flora auricolare
Dati provenienti da VP Hwang, uno degli antichi dottorandi di Peter Hill, mostrano la frequenza di isolamento di diverse specie microbiche nell’otite tramite coltura quantitativa. I coriniformi, gli stafilococchi coagulasi negativi e i micrococchi presenti negli animali sani scompaiono progressivamente nei casi di otite, mentre simultaneamente si osserva una transizione verso infezioni da stafilococchi coagulasi positivi e bacilli Gram negativi come Proteus e Pseudomonas e organismi similari. Nello studio di Hwee Peng Hwang, esisteva una frequenza abbastanza elevata di isolamento di Malassezia negli animali normali, circa il 25%, sebbene talvolta tassi inferiori siano riportati in altri studi. Gustafson nel suo lavoro originale riportava frequenze inferiori a questa percentuale. Un piccolo aumento di frequenza si osserva nei casi di otite comparativamente agli animali sani. L’analisi quantitativa rivela tuttavia una differenza maggiore e fondamentale riguardante la dimensione delle popolazioni di lieviti. Venti cani sani esaminati tramite metodo semi-quantitativo di lavaggio tramite tampone mostrarono due cani con una sola colonia di Malassezia e 18 cani senza Malassezia auricolare rilevabile. I cani malati provenienti da studi condotti recentemente con residenti precedenti e attuali presentano una dimensione mediana di popolazione dell’ordine di 10^5, rappresentante un aumento di 100.000 volte della densità di popolazione nei casi di otite con proliferazione di Malassezia comparativamente alle orecchie sane.
Disbiosi iatrogena e conseguenze terapeutiche
Da numerosi anni, si osserva che una monoterapia antibatterica potente, come l’enrofloxacina iniettabile o la piperacillina-tazobactam, elimina efficacemente Pseudomonas nei casi refrattari ai trattamenti convenzionali, ma crea regolarmente una proliferazione di Malassezia, o anche occasionalmente di Candida. La piperacillina, penicillina di terza generazione possedente un’attività estesa contro gli organismi Gram negativi, associata al tazobactam che blocca la penicillinasi come il clavulanato in altre formulazioni, permette di risolvere i casi di otite da Pseudomonas in fase terminale disperata, ma genera frequentemente un’otite da lieviti susseguente.
Impatto degli antibiotici sulla flora
Uno studio su 20 cani in follow-up attualmente tenta di prevenire questa complicazione iatrogena. I dati riguardanti la piperacillina-tazobactam dimostrano risultati similari sebbene ancora più marcati rispetto all’enrofloxacina iniettabile, quest’ultima essendo meno efficace contro Pseudomonas e generando meno frequentemente la disbiosi da lieviti susseguente. Questi animali stanno estremamente bene clinicamente quando viene somministrata la piperacillina e il tazobactam per la loro otite batterica, ma sviluppano regolarmente una proliferazione di Malassezia necessitante un trattamento antifungino addizionale.
Manifestazioni cliniche
Segni dermatologici nel cane
Le manifestazioni cliniche della dermatite da Malassezia canina sono variate e caratteristiche. Un giovane Scottish Terrier può iniziare la sua esistenza con una dermatite cronica caratterizzata da lesioni simmetriche a livello della coscia mediale e dell’inguine, sotto forma di placche di alopecia abbastanza ben delimitate. Un Jack Russell Terrier più avanzato nell’evoluzione della sua malattia presenta un’escoriazione marcata e una lichenificazione testimoniante la cronicità e la persistenza del processo infiammatorio.
I Basset Hound mostrano frequentemente un materiale aderente ai fusti piliferi a livello della piega ombelicale. Questo materiale brunastro o nerastro si ritrova ugualmente negli spazi interdigitali. Questa caratteristica clinica si rivela diagnosticamente utile, poiché se i cani atopici, i cani infestati da Trombicula (acari autunnali) o affetti da demodicosi presentano un eritema interdigitale, solo quelli portatori di lieviti o di stafilococchi sviluppano questa crosta cherato-sebacea caratteristica. La piega del collo dei Basset Hound molto maleodoranti e infiammati mostra depositi similari di materiale cherato-sebaceo.
Sintomatologia tipo: prurito e odore
I segni clinici comprendono prurito, eritema, squame e seborrea grassa, pigmentazione, lichenificazione, e certamente, il cattivo odore sgradevole caratteristico che accompagna alcuni di questi animali e impregna le sale di consultazione. Una paronichia con croste periungueali e decolorazione ungueale bruna può insorgere. Talvolta, il materiale colorato può essere superficiale e può essere rimosso meccanicamente, altre volte la macchia sembra essere in qualche modo impregnata profondamente nella cheratina dell’unghia in modo più permanente. Un prurito del chanfrein insolitamente frenetico costituisce un’altra manifestazione clinica intrigante.
Particolarità feline
I gatti non sono piccoli cani, e questa affermazione fondamentale rimane vera riguardo alla dermatite da Malassezia. I gatti allergici che presentano un prurito cervico-facciale intenso possono sviluppare una dermatite da Malassezia, sebbene meno frequentemente dei cani. Il gatto Rex rappresenta il Basset Hound del mondo felino in termini di predisposizione a Malassezia. I Devon Rex mostrano una suscettibilità marcata, con presenza di un materiale brunastro sull’addome e la coscia mediale, e di crosta nerastra negli spazi interdigitali e nelle pieghe ungueali. I gatti Sphinx, strettamente imparentati geneticamente ai Devon Rex ma sprovvisti di pelliccia, sviluppano precocemente un’otite da Malassezia.
Sindromi paraneoplastiche feline
Alcuni medici hanno incontrato l’alopecia paraneoplastica pancreatica nei gatti più anziani, sindrome drammatica e caratteristica. Perdita di peso improvvisa in un gatto anziano con comparsa improvvisa di un’alopecia drammatica, simmetrica e completa, talvolta accompagnata da un deposito nerastro. Un altro caso illustrativo mostra la cute brillante associata alla perdita di strato corneo, caratteristica abbastanza distintiva di questa sindrome, e il deposito bruno della dermatite secondaria da Malassezia.
Dermatite esfoliativa e timoma
Un altro gatto fu visto da diversi residenti specializzati qualche anno fa. Kathy Bortnick, residente in dermatologia, prelevò alcune placche di contatto per analisi micologica. Questo gatto presentava una dermatite esfoliativa causata da un timoma, tumore timico. Le colture su placca di contatto mostrarono una crescita di Malassezia. Rob, residente in chirurgia dei tessuti molli e chirurgo visivo pragmatico, rimosse chirurgicamente il timo. Kathy prescrisse due bagni di shampoo al solfuro di selenio. Tutta la Malassezia scomparve completamente. La resezione chirurgica del timo associata alla terapia topica semplice eliminò totalmente la proliferazione di lieviti. Il problema paraneoplastico e il disturbo di desquamazione essendo controllati, la dermatite da Malassezia scomparve. La differenza maggiore tra gatto e cane risiede nella frequenza di associazione con affezioni sistemiche gravi, in particolare neoplasie viscerali e malattie metaboliche, scatenanti Malassezia come manifestazione nuova in un animale anziano. Questa eventualità necessita una vigilanza particolare e un’indagine approfondita durante la comparsa improvvisa di proliferazione di Malassezia in un gatto precedentemente sano.
Approcci diagnostici
Metodi di quantificazione e di rilevazione
La quantificazione di Malassezia sulla cute e la comprensione della sua pertinenza clinica costituiscono sfide diagnostiche complesse.
Placca di contatto vs Spazzolamento tramite coppetta
Le placche di contatto rappresentano un metodo semplice ma largamente sottoutilizzato. Si fabbricano a partire da coperchi di bottiglie riempiti a ras di bordo di terreno di coltura, mantenuti in piastre di Petri sterili per preservare la sterilità. L’applicazione diretta su una lesione cutanea durante 10 secondi, seguita da un’incubazione di tre giorni a temperatura appropriata, permette di apprezzare l’abbondanza di lieviti tramite osservazione della crescita confluente o sparsa. Per i gatti, coperchi più piccoli di dimensioni ridotte si applicano facilmente negli spazi interdigitali e altri siti anatomici ristretti. Lo spazzolamento tramite coppetta costituisce definitivamente uno strumento essenzialmente di ricerca piuttosto che di routine clinica. Questa tecnica necessita una cute piatta e un paziente cooperativo, condizioni non sempre riunite in pratica. Una coppetta sterile in Teflon contenente 2 ml di siero fisiologico addizionato di detergente permette di strofinare delicatamente la cute mirata. Il liquido aspirato subisce diluizioni in serie fino all’ottenimento di un numero contabile di colonie dopo coltura, permettendo di estrapolare una densità di popolazione espressa in unità formanti colonie per centimetro quadrato. I lieviti muoiono rapidamente nel siero fisiologico con detergente, necessitando un trattamento immediato dei campioni, incompatibile con un invio postale o un ritardo di trasporto prolungato. I conteggi su placche di contatto e tramite spazzolamento in coppetta non sono ben correlati statisticamente. I conteggi tramite nastro adesivo non sono neppure correlati con lo spazzolamento tramite coppetta. Un problema metodologico esiste quindi. Il metodo di riferimento per la coltura di Malassezia, si potrebbe argomentare, rimane lo spazzolamento tramite coppetta in quanto gold standard, ma la pratica clinica quotidiana utilizza comunemente il nastro adesivo o tecniche similari più pratiche.
Citologia e interpretazione clinica
La tecnica del nastro adesivo, popolarizzata dalla pubblicazione storica di Keddie e Libis in Sabouraudia, permette di diagnosticare i microbi residenti nello strato corneo. Nel Regno Unito, lo Scotch o Sellotape Diamond Clear sono comunemente utilizzati, diverse marche commerciali sopravvivendo o no al processo di colorazione secondo la loro composizione. Un metodo pratico presentato dal nostro collega, consiste nel fissare un pezzo di nastro adesivo all’estremità di una lamina di vetro, creando un assemblaggio manipolabile con una mano. Questa mano può separare gli spazi interdigitali o separare la piega labiale o la piega facciale, permettendo l’inserzione della lamina, la raccolta delle squame, poi una colorazione Diff-Quik rapida dopo arrotolamento e appiattimento del nastro sulla lamina.
Fattori influenzanti i conteggi
Il significato dei conteggi dipende da molteplici fattori. Il metodo di campionamento influenza fondamentalmente i risultati. I raschiamenti a secco e l’impressione diretta non forniscono generalmente un trasferimento sufficiente di materiale comparato al ‘tape stripping‘, sebbene altri medici possano avere prospettive differenti. Il sito anatomico costituisce un fattore maggiore. I conteggi su placche di contatto delle labbra e del piede differiscono significativamente. Esistono maggiori lieviti in una piega labiale in un cane sano comparativamente allo spazio interdigitale. Come determinare quale soglia popolazionale costituisce una proliferazione patologica se la popolazione normale varia sostanzialmente da un sito anatomico all’altro?
Influenza della razza sulle popolazioni
La razza influenza considerevolmente le popolazioni normali. I cani di razza mista sani, presentano pochi lieviti, e quando ne possiedono, le popolazioni rimangono molto basse. I Basset Hound seborroici mostrano una densità di popolazione mediana molto più elevata dei cani di razza mista sani.
Soglie citologiche e ricerca
Nei gatti, uno studio su placca di contatto nell’ascella dimostra che i gatti randagi non possiedono molta Malassezia. I Cornish Rex non presentano Malassezia. I Devon Rex seborroici con deposito nerastro mostrano una crescita sulla placca di contatto. I Devon Rex sani costituiscono un gruppo intermedio tra questi estremi.
Stato immunitario e ipersensibilità
Lo stato immunitario dell’ospite svolge un ruolo cruciale nell’interpretazione dei conteggi. Alcuni animali presentano un’ipersensibilità immediata rilevabile tramite test IgE, tramite sierologia o test intradermici. Altri mostrano un’ipersensibilità ritardata durante il test intradermico. Nei Basset Hound, l’ipersensibilità di contatto correla bene con la malattia o la sua assenza. I Basset Hound sani non mostrano ipersensibilità di contatto, contrariamente ai malati che la sviluppano, se lo sforzo di realizzare patch-test sui cani è compiuto, procedura non adattata alla routine clinica quotidiana. Come per altri allergeni, il test IgE costituisce precisamente ciò: un test IgE. Se un test intradermico è effettuato, non è un test di malattia ma un test di sensibilità immunologica. Un Basset Hound sano presentante un’ipersensibilità immediata spettacolare e drammatica a Malassezia durante il test intradermico illustra questa dissociazione tra sensibilità e malattia clinica.
Istopatologia
L’istopatologia può essere effettuata per documentare le lesioni di dermatite da Malassezia. Non è senza dubbio il miglior metodo per cercare qualcosa che risiede nello strato corneo a causa della perturbazione sostanziale che si produce nelle sezioni normali fissate in formalina e incluse in paraffina secondo i protocolli istologici standard. Su una diapositiva comparativa, lo strato corneo normale mostra l’ortocheratosi comune a cestino intrecciato che i patologi osserverebbero in routine. Al contrario, in una sezione di criostato – tecnicamente difficile da realizzare, tagliare della cute in un criostato rappresentando una sfida tecnica – l’osservazione rivela quanto la buona barriera, lo strato corneo intatto, è densamente compattata con un grande impilamento di squame costituenti una barriera compatta. È un artefatto di trattamento, non è assolutamente così nella vita reale in vivo. In una micrografia elettronica a scansione, il grande impilamento di squame formante la barriera abituale è visibile. Il sigillo lipidico manca, rimosso ed eliminato dal trattamento di preparazione del campione, ma il grande impilamento di squame persiste.
Artefatti e osservazioni istologiche
Quando una biopsia di un cane è esaminata e mostra tutto questo strato corneo assente o tutto questo materiale lasso e disorganizzato, si tratta di un artefatto istologico e non di una rappresentazione fedele della struttura in vivo. Alcune caratteristiche importanti possono nondimeno essere osservate, includendo un’iperplasia epidermica irregolare dell’epidermide interfollicolare estendentesi nell’infundibolo follicolare. Una cheratosi è certamente presente. Un certo grado di edema e un infiltrato dermico superficiale perivascolare o interstiziale caratterizzano le lesioni. A causa della perturbazione sostanziale dello strato corneo di superficie durante il trattamento istologico, un buon posto per cercare la Malassezia risiede negli ostia o infundiboli follicolari, strutture meno perturbate dello strato corneo superficiale. In un campione colorato con ematossilina-eosina (H&E) standard, se questa zona è esaminata a più forte ingrandimento, i lieviti diventano visibili. Sebbene questi organismi possano essere visualizzati con la colorazione H&E standard, essi possono essere schiariti e resi più evidenti con una colorazione PAS (acido periodico di Schiff) e ancora meglio messi in evidenza con una colorazione all’argento se necessario per conferma.
Caratteristiche istopatologiche chiave
Le caratteristiche istopatologiche descritte da diversi autori e documentate sono abbastanza concise. Cheratosi, sia ortocheratosica sia paracheratosica, iperplasia epidermica, spongiosi. Esocitosi linfocitaria o neutrofila e un infiltrato dermico linfocitario o misto. L’istopatologia nei gatti rimane meno ben definita e documentata. L’ipercheratosi e l’iperplasia costituiscono caratteristiche importanti, ma le caratteristiche della malattia sottostante scatenante la proliferazione di Malassezia potrebbero ugualmente essere osservate nei campioni istologici.
Algoritmo diagnostico
Approccio passo-passo
L’approccio di un caso sospetto di dermatite da Malassezia inizia logicamente con un’anamnesi dettagliata e l’identificazione di segni clinici compatibili con questa affezione. La tappa successiva consiste nel dimostrare se il lievito è presente o no. Ciò si farà normalmente tramite citologia in pratica clinica quotidiana, sebbene in ambiente di ricerca ciò possa essere effettuato tramite coltura, coltura quantitativa permettente una valutazione precisa delle popolazioni. I conteggi non hanno necessariamente bisogno di essere elevati per giustificare un trattamento. Se i lieviti sono rilevati in numero ragionevole, una terapia di prova deve essere iniziata e la risposta osservata attentamente. In loro assenza durante il campionamento iniziale, un nuovo campionamento di siti supplementari o la considerazione di un’altra spiegazione diagnostica si impone.
Interpretazione della risposta terapeutica
Se i lieviti scompaiono totalmente e i segni clinici si risolvono completamente, la diagnosi di dermatite da Malassezia è stabilita con confidenza e la ricerca di una causa sottostante diventa prioritaria per prevenire le recidive. Se i lieviti scompaiono totalmente con miglioramento clinico parziale globale, la diagnosi di dermatite da Malassezia è confermata e l’investigazione poi il trattamento dell’allergia residua, del disturbo di desquamazione o del problema di piega anatomica devono essere intrapresi. Il Westie Highland White Terrier classico fuori controllo con i farmaci convenzionali illustra perfettamente questa situazione: il trattamento di Malassezia e degli stafilococchi rivela una dermatite atopica sottostante che diventa allora controllabile con terapie appropriate per la gestione allergica. Se i lieviti scompaiono senza alcun beneficio clinico, la loro presenza era incidentale e non causale. Una scomparsa parziale dei lieviti con miglioramento clinico parziale suggerisce una dermatite da Malassezia, necessitando revisione dell’osservanza terapeutica, estensione e intensificazione del trattamento per ottenere un’eliminazione completa dei lieviti. L’assenza totale di miglioramento clinico con persistenza dei lieviti impone la verifica rigorosa dell’osservanza del proprietario, la revisione e modifica del trattamento, e la considerazione seria di una resistenza potenziale agli antifungini, particolarmente nel contesto contemporaneo di emergenza di ceppi resistenti.
Strategie terapeutiche
Trattamento sistemico nel cane
Studi di efficacia sono riportati per il chetoconazolo, l’itraconazolo e il fluconazolo come azoli, così come la terbinafina come allilammina. Alcuni studi associavano la cefalexina concomitante a causa dell’importanza degli stafilococchi in alcune zone geografiche e regionali. La scelta finale dipenderà dalla disponibilità locale, dalle regole di prescrizione locali e regolamentazioni farmaceutiche, dai fattori individuali del paziente includendo comorbidità e controindicazioni, e dai costi che possono variare considerevolmente da un paese all’altro. L’itraconazolo e il chetoconazolo costituiscono opzioni valide da somministrare a un cane affetto da dermatite da Malassezia. Il fluconazolo possiede i suoi adepti e difensori. È il meno attivo in laboratorio in termini di microgrammi per millilitro durante i test di concentrazioni minime inibenti (MIC). La terbinafina necessita una valutazione più approfondita. Le concentrazioni nello strato corneo alle dosi attualmente utilizzate potrebbero non essere sufficientemente elevate secondo uno studio farmacocinetico pubblicato.
Trattamento topico nel cane
I dati di efficacia per i topici riguardano lo shampoo miconazolo-clorexidina, gli shampoo al 3% di clorexidina, i condizionatori al miconazolo, e un prodotto a base di oli essenziali chiamato MalAcetic. Due studi controllati randomizzati in cieco dimostrano una buona attività clinica dello shampoo miconazolo-clorexidina. Prove cliniche sul Malaseb (Miconazolo-Clorexidina) condotte nel luglio 1994 mostrarono risultati notevoli. Questi cani severamente affetti da dermatite da Malassezia, inizialmente giudicati necessitare chetoconazolo sistemico e cefalexina antibatterica secondo la valutazione clinica iniziale, ricevettero unicamente shampoo Malaseb come solo trattamento a intervalli di tre giorni durante tre settimane.
L’eliminazione simultanea degli stafilococchi e delle Malassezia con questo prodotto si rivela importante poiché alcune microscopie elettroniche di alcuni campioni di spazzolamento tramite coppetta rivelano i lieviti integrati ma circondati da numerosi cocchi batterici, sottolineando l’importanza di mirare simultaneamente stafilococchi e Malassezia in queste infezioni miste. Sulla base dell’esame metodico degli studi pubblicati, il miconazolo-clorexidina rappresenta il trattamento topico di prima scelta supponendo che l’animale lo accetti e tolleri i bagni e che il proprietario possa applicarlo correttamente e regolarmente.
Trattamento auricolare nel cane
Le otiti esterne da Malassezia pachydermatis nel cane costituiscono un’affezione frequente necessitante un trattamento topico antifungino adattato. Sul mercato, si trovano attualmente diverse specialità veterinarie basantesi principalmente su due famiglie di antifungini: i derivati azolici e le allilammine. Tra gli approcci terapeutici comunemente utilizzati, si ritrovano associazioni di miconazolo con gentamicina e aceponato di idrocortisone, indicate nel trattamento delle otiti esterne acute e ricorrenti dovute a funghi sensibili agli azoli. Altre formulazioni classiche combinano clotrimazolo, gentamicina e betametasone per le otiti di origine batterica e fungina. Le associazioni di florfenicolo e terbinafina mirano specificamente le infezioni miste da Staphylococcus pseudintermedius e Malassezia pachydermatis. Queste formulazioni polivalenti associano sistematicamente antibiotico, antifungino e corticoide, ciò che limita le possibilità di trattamento specifico.chvsm+3
Un’innovazione terapeutica recente sul mercato francese costituisce il primo topico auricolare lunga azione senza antibiotico specificamente sviluppato per le otiti da Malassezia pachydermatis. Questa formulazione originale associa 10 mg di terbinafina, un’allilammina fungicida inibente la sintesi dell’ergosterolo di membrana, e 1 mg di acetato di betametasone per la sua azione anti-infiammatoria. Il formato gel lunga azione permette un’applicazione unica facilitante l’osservanza terapeutica. Gli studi di sensibilità condotti tra 2021 e 2023 su isolati europei di Malassezia hanno stabilito MIC50 e MIC90 rispettivamente di 0,12 e 0,25 μg/ml per la terbinafina. Questa specialità si iscrive in un approccio di antibioticoterapia ragionata proponendo un’alternativa senza antibiotico sistematico, particolarmente pertinente durante otiti puramente fungine non necessitanti copertura antibatterica.
Trattamento nel gatto
Nel gatto, diversi studi aperti non controllati utilizzarono l’itraconazolo a dosi comprese tra 5 e 10 mg/kg una volta al giorno, sia in continuo quotidianamente, sia secondo un protocollo intermittente sette giorni con trattamento, sette giorni senza trattamento, sette giorni con trattamento, corrispondente alla licenza Itrafungol per la dermatofitosi nel Regno Unito. I dati rimangono limitati per i gatti in generale. L’azolo sistemico di prima scelta sarebbe l’itraconazolo secondo il consenso clinico. Il chetoconazolo non è verosimilmente somministrato ad alcun gatto a causa di preoccupazioni riguardanti la tolleranza e la sicurezza. La terapia topica manca ugualmente di dati scientifici rigorosi.
Prevenzione e gestione delle recidive
Immunoterapia specifica
La scoperta e la correzione delle malattie sottostanti costituiscono la pietra angolare assoluta della prevenzione delle recidive. Un dosaggio pulsato, sia topico sia sistemico, può essere considerato quando tutto il resto fallisce, con la preoccupazione costante della resistenza agli antifungini. Le prove per l’immunoterapia specifica agli allergeni per Malassezia mancano, sebbene numerosi medici la utilizzino comunemente. Durante una discussione anteriore, fu stabilito che molti partecipanti includono Malassezia nei loro pannelli di test intradermici e l’incorporano nelle loro formulazioni di immunoterapia durante reattività positiva. In assenza di prove convincenti e rigorose, l’inclusione di Malassezia nell’immunoterapia specifica agli allergeni riposa maggiormente su un consenso di esperti che su dati probanti robusti.
Strategie di mantenimento
L’approccio razionale per un animale ipersensibile a Malassezia consiste nel minimizzare la sfida antigenica mantenendo le popolazioni di lieviti basse, il più basse possibile. Ciò potrebbe significare una terapia topica molto regolare e assidua se gli animali possono essere bagnati e che i proprietari possono compiere questo compito ripetitivamente. Ciò potrebbe significare azoli pulsati somministrati in modo intermittente, ma certamente, la preoccupazione legittima esiste riguardante la promozione della resistenza agli antifungini.
Resistenza agli antifungini: meccanismi e sfide
Esistono rapporti crescenti e preoccupanti dello sviluppo di resistenza ai farmaci antifungini ma a distribuzione eterogenea, principalmente descritti con la classe degli azoli, che sono utilizzati routinariamente e globalmente nel trattamento delle infezioni canine da Malassezia. Essa è endemica e frequente in alcune regioni dell’Asia orientale, ma rimane sporadica in Europa e in America del Nord. Sfortunatamente, la sorveglianza della resistenza agli antifungini accusa un ritardo sostanziale rispetto a quella effettuata per i patogeni batterici. Questa situazione deriva in parte da una mancanza di metodi di laboratorio standardizzati e da sottomissioni poco frequenti di campioni per coltura e test di sensibilità. La resistenza in Malassezia e altri funghi, così come nei patogeni umani, costituisce una preoccupazione maggiore assoluta. I metodi standard per test di sensibilità dei lieviti sono ottimizzati da organizzazioni come il CLSI (Clinical and Laboratory Standards Institute) negli Stati Uniti e l’EUCAST (European Committee on Antimicrobial Susceptibility Testing) in Europa, ottimizzati specificamente per Candida e Cryptococcus. Questa focalizzazione, tenuto conto dell’importanza considerevole di questi patogeni in medicina umana, è del tutto giustificata e comprensibile. Tuttavia, il terreno di coltura tissutale RPMI 1640 che raccomandano per questo processo di test non supporta la crescita di Malassezia. A partire da questo punto fondamentale, tutto diventa improvvisato e non standardizzato. Non esiste protocollo appropriato validato per Malassezia.
Alternative terapeutiche e ricerche in corso
Prodotti innovativi e naturali
Le preoccupazioni legittime riguardanti la resistenza farmacologica stimolano gli sforzi per identificare trattamenti efficaci al di là degli antifungini convenzionali azoli e allilammine. Oggigiorno, nel corso degli ultimi sette-otto anni, molti studi sono stati realizzati utilizzando tutti i tipi di cose differenti non-azoli, non-terbinafina per tentare di uccidere Malassezia in vitro. La maggioranza di questi approcci sono stati effettuati in vitro e non sono stati estesi a una prova clinica controllata randomizzata rigorosa su pazienti reali. Studi recenti sull’otite esaminano diversi prodotti innovativi: un detergente auricolare contenente melograno come principio attivo, un prodotto a base di piante per trattare l’otite, un risciacquo auricolare a base di resina di abete di Norvegia, poi un prodotto più convenzionale contenente posaconazolo, che è certamente un antifungino azolico di grosso calibro e molto potente. Alcuni studi sulla dermatite esaminano shampoo contenenti argento colloidale e spray contenenti perossido di benzoile e alcol e oli botanici diversi. Uno shampoo alle nanoparticelle d’argento mostrò risultati promettenti in uno studio aperto non randomizzato metodologicamente limitato. Rapporti in vitro descrivono l’efficacia contro M. pachydermatis di un gel a base di miele, della monensina e, in minor misura, della narasina. Questi ionofori polieteri furono originalmente commercializzati come anticoccidici per il pollame e come modificatori promotori di crescita della flora ruminale bovina, e presentano apparentemente un’attività antifungina in vitro.
Oli essenziali e limiti
Molteplici pubblicazioni recenti esplorano l’utilità antifungina potenziale degli oli essenziali, miscele complesse di oli aromatici altamente concentrati (principalmente terpeni e/o fenilpropanoidi) estratti da piante tramite distillazione a vapore, idrodiffusione o pressione meccanica. La maggioranza delle investigazioni sono state condotte in vitro e la loro utilità reale in pratica clinica rimane largamente non testata clinicamente. I confronti tra studi sono ostacolati e resi difficili dall’assenza di metodi di test standard ottimizzati e validati, l’attribuzione arbitraria di criteri interpretativi senza validazione rigorosa, e la variazione probabile tra lotti differenti di attività degli oli essenziali preparati tramite differenti metodi di estrazione e provenienti da fonti vegetali variabili. La maggioranza schiacciante di questi approcci alternativi sono stati realizzati in vitro in provette senza estensione a prove cliniche controllate randomizzate su pazienti reali con valutazione rigorosa dell’efficacia clinica.
Raccomandazioni pratiche e prospettive
La citologia dovrebbe essere effettuata sistematicamente in pratica canina corrente per cercare questi lieviti opportunisti e stabilire o infirmare il loro coinvolgimento nel quadro clinico.
Se il lievito è trattato, il conteggio preciso non è probabilmente necessario. Trovatelo semplicemente in numero ragionevole con segni clinici compatibili, trattatelo e osservate la risposta clinica. Seguite i pazienti con rivalutazioni regolari e rifate la citologia e vedete se il lievito è scomparso e valutate ciò in rapporto alla risposta clinica osservata. Il trattamento deve essere individualizzato in funzione delle differenti circostanze del paziente includendo comorbidità e controindicazioni, e delle circostanze del proprietario includendo capacità finanziaria e compliance probabile. Certamente un azolo sistemico costituisce un’opzione valida per i casi che non possono essere shampoonati e altre situazioni dove i topici sono impraticabili. Durante tutto il processo terapeutico, bisogna costantemente tentare di trovare e di correggere il fattore scatenante sottostante poiché se ciò può essere compiuto, le infezioni recidivanti possono essere ridotte, il bisogno di farmaci antifungini può essere ridotto, e quindi la pressione di selezione che potrebbe condurre verso l’emergenza e la propagazione di resistenza può essere minimizzata.
Conclusione
Nel corso degli ultimi 35 anni, un’espansione notevole delle conoscenze riguardanti le affezioni cutanee legate a Malassezia nei cani e gatti è stata realizzata. La maggioranza dei medici veterinari sono ormai a proprio agio nel riconoscere le presentazioni cliniche variate della dermatite e dell’otite da Malassezia e nell’osservare i lieviti caratteristici in citologia di routine. La necessità di valutare e di correggere, nella misura del possibile, i fattori predisponenti e affezioni sottostanti è ben compresa dalla comunità veterinaria contemporanea.
L’emergenza preoccupante della resistenza agli azoli tra le specie di Malassezia necessita una sorveglianza attenta e continua così come una gestione rigorosa di questi prodotti farmaceutici per garantire l’utilità continua di questa classe medicamentosa importante per i decenni a venire. Lo sviluppo di test di sensibilità antifungina standardizzati appropriati e validati per utilizzo da parte dei laboratori commerciali e clinici di microbiologia è assolutamente critico e urgente. Dati supplementari sono urgentemente necessari per stabilire definitivamente se le terapie topiche sono preferibili ai trattamenti sistemici nel contesto della prevenzione della resistenza, e per guidare le politiche di gestione antimicrobica (antimicrobial stewardship policies) riguardanti la terapia antifungina in pratica veterinaria dei piccoli animali.
Bond R. Malassezia review Parts i and ii: Clinical signs, Diagnosis, therapy and resistance. NAVDF 2025 Meeting