Les tests allergologiques intradermiques et l’immunothérapie spécifique d’allergène demeurent encore insuffisamment exploités dans la prise en charge thérapeutique des affections dermatologiques félines. Cette situation persiste malgré l’efficacité démontrée de ces approches dans la gestion du syndrome atopique cutané félin.
L’étude rétrospective multicentrique menée par six cliniciens spécialisés apporte un éclairage fondamental sur l’efficacité de l’immunothérapie spécifique dans la réduction des besoins médicamenteux chez les félins atteints de syndrome atopique cutané.
Méthodologie et Population Étudiée
L’investigation porte sur une cohorte de 158 félins domestiques présentant des manifestations cutanées chroniques ou récurrentes évoluant depuis au moins une année. La population étudiée comprend majoritairement des chats européens à poil court (132 individus), avec une prédominance femelle notable (92 femelles contre 66 mâles). L’âge médian s’établit à quatre années, avec des variations s’étendant de un à treize ans.
Critères Diagnostiques du Syndrome Atopique Cutané Félin
Le diagnostic repose sur l’identification de patterns cliniques caractéristiques incluant l’alopécie auto-induite (63 cas), le prurit céphalique et cervical (81 cas), les lésions du complexe granulome éosinophilique (50 cas), la dermatite miliaire (18 cas) et le prurit diffus (8 cas). Plus du tiers des animaux présentent simultanément plusieurs patterns cliniques, témoignant de la complexité physiopathologique de cette affection.
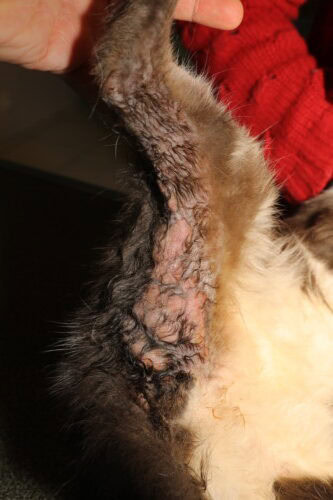
Sévère granulome éosinophilique félin
L’établissement du diagnostic nécessite l’exclusion rigoureuse des autres affections prurigineuses. Les protocoles d’éviction comprennent un traitement antiparasitaire d’au moins huit semaines pour éliminer l’hypersensibilité aux piqûres de puces, un régime d’éviction alimentaire utilisant des protéines hydrolysées pendant huit semaines minimum, et l’exclusion des infections bactériennes ou fongiques par des examens complémentaires appropriés.
Protocole des Tests Intradermiques
La réalisation des tests intradermiques s’effectue sous sédation ou anesthésie générale, utilisant des agents pharmacologiques dont l’innocuité sur les réactions cutanées a été préalablement validée. L’innovation méthodologique réside dans l’utilisation de fluorescéine sodique intraveineuse (5 mg/kg) chez 136 animaux, associée à l’examen sous lampe de Wood pour optimiser l’interprétation des réactions cutanées.
Panel Allergénique et Concentrations
Les extraits allergéniques testés comprennent les pollens (1/1000 p/v ou 1000 NU/mL), les phanères (1/2000 p/v ou 100 μg/mL), les levures et moisissures (1/2000 p/v ou 100 μg/mL), les acariens domestiques et de stockage (1/2000 p/v ou 100 NU/mL), et les insectes (1/2000 p/v ou 1000 NU/mL). Chaque injection de 0,05 mL est évaluée après 10 à 20 minutes selon des critères précis d’érythème, de taille et de turgescence papulaire.
La positivité des réactions se définit par une fluorescence homogène et des contours papulaires bien délimités, avec une taille égale ou supérieure à la moyenne des diamètres des témoins négatif et positif.
Résultats des Tests Allergologiques
L’interprétabilité des tests atteint 97% de la population testée (153 sur 158 félins). L’absence de sensibilisation spécifique concerne 35% des animaux testés (53 cas), tandis que 65% présentent des réactions positives (100 cas). Parmi ces derniers, la polysensibilisation prédomine largement avec 78 cas contre 22 monosensibilisations.
Profil de Sensibilisation Allergénique
Les acariens domestiques représentent la catégorie allergénique majeure avec 74% de sensibilisations positives. Dermatophagoides farinae constitue l’allergène prédominant (67% des cas positifs), suivi de Dermatophagoides pteronyssinus (27%). Les acariens de stockage affectent 44% des animaux sensibilisés, principalement Acarus siro (32%), Tyrophagus putrescentiae (27%) et Lepidoglyphus destructor (8%).
Les sensibilisations polliniques touchent respectivement 18% des cas pour les graminées, 19% pour les herbacées et 19% pour les pollens d’arbres. Les puces induisent des réactions positives chez 17% des animaux testés, tandis que les moisissures ne concernent que 7% de la population étudiée.
Protocoles d’Immunothérapie Spécifique
L’immunothérapie spécifique s’initie chez 78 des 100 félins présentant des sensibilisations compatibles avec leur anamnèse. Les protocoles utilisent des allergènes adjuvantés au phosphate de calcium ou à l’aluminium, administrés par voie sous-cutanée selon des schémas posologiques progressifs. Le nombre d’allergènes inclus varie de un à cinq par formulation, avec une moyenne de trois allergènes par traitement.
La sélection allergénique s’appuie sur les résultats des tests intradermiques et les proximités phylogénétiques, particulièrement pour les acariens. Les extraits contenant des protéases ne sont pas mélangés aux extraits polliniques pour éviter les interactions enzymatiques délétères.
Évaluation de l’Efficacité Thérapeutique
Système de Scoring Médicamenteux
L’efficacité thérapeutique s’évalue par un système de scoring validé attribuant des points aux différentes catégories médicamenteuses : antihistaminiques (10 points), corticostéroïdes selon la posologie (10 à 40 points), ciclosporine (5 à 30 points) et oclacitinib (10 à 40 points). Une réduction significative se définit par une diminution d’au moins 30% du score médicamenteux.
Résultats Comparatifs sur Douze Mois
Quarante-deux félins traités par immunothérapie spécifique bénéficient d’un suivi complet sur douze mois, comparés à 36 animaux témoins non traités. Les groupes présentent des caractéristiques épidémiologiques et cliniques homogènes, validant la pertinence comparative.
Le score médicamenteux initial s’avère significativement plus élevé dans le groupe traité (38 points en moyenne, amplitude 30-70) comparé au groupe témoin (33 points, amplitude 10-60). Cette différence initiale renforce la robustesse de l’évaluation ultérieure.
Évolution des Besoins Médicamenteux
L’immunothérapie spécifique génère une réduction médicamenteuse significative chez 74% des félins traités (31 sur 42 animaux) avec une diminution moyenne de 58% du score initial après douze mois (score final moyen : 16 points, amplitude 0-40). Parallèlement, seuls 28% des animaux témoins (10 sur 36) présentent une amélioration spontanée avec une réduction moyenne de 19% (score final moyen : 27 points, amplitude 0-50).
Cinétique d’Amélioration Thérapeutique
La différenciation statistique entre les groupes devient significative après six mois de traitement. Les réductions moyennes s’établissent progressivement à 13%, 38%, 43% et 58% respectivement à 3, 6, 9 et 12 mois dans le groupe traité, contre 5%, 9%, 10% et 19% dans le groupe témoin aux mêmes échéances.
L’analyse statistique confirme l’absence de corrélation entre le score médicamenteux initial et la réponse thérapeutique, suggérant une efficacité indépendante de la sévérité initiale des symptômes.
Signification Clinique et Perspectives Thérapeutiques
Cette investigation constitue la plus vaste étude contrôlée évaluant l’efficacité de l’immunothérapie spécifique féline. Les résultats démontrent un effet d’épargne médicamenteuse statistiquement significatif et cliniquement pertinent, avec un arrêt complet des traitements chez 26% des animaux traités.
L’utilisation de fluorescéine intraveineuse représente une innovation méthodologique sécurisée optimisant l’interprétation des tests intradermiques, particulièrement pour les extraits acariens traditionnellement difficiles à évaluer.
La prédominance des sensibilisations aux acariens domestiques et de stockage oriente vers des stratégies thérapeutiques ciblées, tout en questionnant les phénomènes de réactivité croisée déjà documentés dans l’espèce canine.
Les limites inhérentes au caractère rétrospectif de l’étude n’altèrent pas la robustesse des conclusions, compte tenu de l’homogénéité protocolaire entre les centres investigateurs et de la significativité statistique des résultats obtenus.
Brément T, Bensignor E, Drevon-Gaillot EV, Sanchez M-D, Pariente S, Viaud S. A retrospective, multicentric controlled study of the effect of specific allergen immunotherapy on medication needs in cats with atopic skin syndrome. Vet Dermatol. 2025;36:332–342.